名校
1 . A、B、C、D为原子序数依次增大的短周期元素,A元素气态氢化物的水溶液呈碱性,B为最活泼的非金属元素,C元素原子的电子层数是最外层电子数的3倍,D元素最高化合价为+6价。
(1)A元素气态氢化物的电子式为______ ;B在元素周期表中的位置为________ 。
(2)DBn做制冷剂替代氟利昂,对臭氧层完全没有破坏作用,是一种很有发展潜力的制冷剂。该物质的摩尔质量为146 g·mol-1,则该物质的化学式为_____ 。已知DBn在温度高于45℃时为气态,DBn属于____ 晶体。该物质被称为人造惰性气体,目前广泛应用于电器工业,在空气中不能燃烧,请从氧化还原角度分析不能燃烧的理由_________ 。
(3)C与氢元素组成1∶1的化合物,与水发生剧烈反应生成碱和一种气体,写出该反应的化学反应方程式____________ ,生成1mol气体转移的电子的数目为______ 个。
(4)A和C两元素可形成离子化合物甲。取13.0g化合物甲,加热使其完全分解,生成A的单质和C的单质,生成的A单质气体折合成标准状况下的体积为6.72L。化合物甲分解的化学方程式为______________________________ 。
(5)D元素的+4价含氧酸钠盐在空气中容易变质,设计实验方案证明该盐已经变质____ 。
(1)A元素气态氢化物的电子式为
(2)DBn做制冷剂替代氟利昂,对臭氧层完全没有破坏作用,是一种很有发展潜力的制冷剂。该物质的摩尔质量为146 g·mol-1,则该物质的化学式为
(3)C与氢元素组成1∶1的化合物,与水发生剧烈反应生成碱和一种气体,写出该反应的化学反应方程式
(4)A和C两元素可形成离子化合物甲。取13.0g化合物甲,加热使其完全分解,生成A的单质和C的单质,生成的A单质气体折合成标准状况下的体积为6.72L。化合物甲分解的化学方程式为
(5)D元素的+4价含氧酸钠盐在空气中容易变质,设计实验方案证明该盐已经变质
您最近一年使用:0次
名校
2 . A~F六种元素中,除F外其他均为短周期元素,它们的原子结构或性质如下表所示。
请回答下列问题:
(1)A在元素周期表中的位置是_____________ ;A与C形成的化合物AC2的电子式是___________ 。
(2)下列事实能证明C和E的非金属性强弱的是_____________ 。(填序号)
①常温下,C的单质呈气态,E的单质呈固态
②C的气态氢化物的稳定性强于E的气态氢化物的稳定性
③C与E形成的化合物中,E呈正价
④E的氢化物的沸点高于C的氢化物的沸点
(3) 由A、B、C和氢元素四种元素所形成的阴、阳离子数目之比为1:1的离子化合物是_________ (填化学式),它与足量NaOH溶液在加热时反应的离子方程为:_______________ 。
(4) FC与足量B的最高价氧化物的水化物的稀溶液反应的离子方程式_________________ 。若有标准状况下5.6L的BC生成,则转移的电子数为_______________ 。
(5) A的氢化物有多种,1 mol A的某种氢化物分子中含有14 mol电子,已知在25℃、101kPa下,1g该氢化物在足量氧气中完全燃烧生成液态水时放出的热量为40 kJ,写出表示该氢化物燃烧热的热化学方程式:_____________________ 。
| 元素 | 原子结构或性质 |
| A | 其形成的一种同位素原子在考古中可推测化石的年代 |
| B | 与A同周期,其最高价氧化物的水化物无论浓、稀溶液均有强氧化性 |
| C | 地壳中含量最多的元素 |
| D | D原子的内层电子数是最外层电子数的5倍 |
| E | 其单质主要存在于火山口附近 |
| F | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
(1)A在元素周期表中的位置是
(2)下列事实能证明C和E的非金属性强弱的是
①常温下,C的单质呈气态,E的单质呈固态
②C的气态氢化物的稳定性强于E的气态氢化物的稳定性
③C与E形成的化合物中,E呈正价
④E的氢化物的沸点高于C的氢化物的沸点
(3) 由A、B、C和氢元素四种元素所形成的阴、阳离子数目之比为1:1的离子化合物是
(4) FC与足量B的最高价氧化物的水化物的稀溶液反应的离子方程式
(5) A的氢化物有多种,1 mol A的某种氢化物分子中含有14 mol电子,已知在25℃、101kPa下,1g该氢化物在足量氧气中完全燃烧生成液态水时放出的热量为40 kJ,写出表示该氢化物燃烧热的热化学方程式:
您最近一年使用:0次
2016-12-09更新
|
350次组卷
|
3卷引用:2017届江西省赣州市十四校高三上期中联考化学试卷
解题方法
3 . 根据表中短周期元素的有关信息判断,下列说法错误的是
| 元素编号 | E | F | G | H | I | J | K | L |
| 原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.160 | 0.186 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +2 | +1 |
| A.最高价氧化物对应水化物的酸性:H>I |
| B.简单离子半径:K>F |
| C.同温下,形状、大小相同的单质与等浓度、等体积的稀硫酸反应的速率:L>K>J |
| D.J、K、L的单质可以通过电解法冶炼获得 |
您最近一年使用:0次
解题方法
4 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W、X同主族,Y原子的最外层电子数等于X原子的电子总数。Z原子的电子总数等于W、X、Y原子的电子数之和,Z的最高价氧化物对应水化物的化学式为 。W、X、Y三种元素组成的一种化合物的结构如图所示。下列说法错误的是
。W、X、Y三种元素组成的一种化合物的结构如图所示。下列说法错误的是
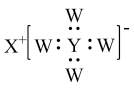
 。W、X、Y三种元素组成的一种化合物的结构如图所示。下列说法错误的是
。W、X、Y三种元素组成的一种化合物的结构如图所示。下列说法错误的是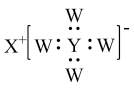
| A.W的最高正价和最低负价的代数和为0 |
| B.W的离子半径一定小于X的简单离子半径 |
| C.Y的最高价氧化物对应的水化物属于两性化合物 |
| D.Z的单质的水溶液需保存在棕色试剂瓶中 |
您最近一年使用:0次
解题方法
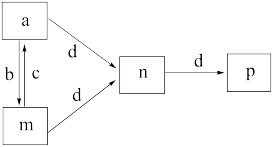
5 . X、Y、Z、W为原子序数依次增大的四种短周期元素,b、a、d、c为上述四种元素形成的单质,m、n、p为四种元素形成的二元化合物,其转化关系如图所示。W与同周期原子半径最大的元素组成的化合物溶液呈中性,n为一种传递神经信息的“信使分子”。下列说法错误的是

| A.a的熔点比d的熔点低 |
| B.Y、Z、W的简单离子半径大小顺序为:Y<Z<W |
| C.X、Z组成的分子可能既含有极性键,又含有非极性键 |
| D.在工业上c可大量用于制造有机溶剂和杀菌消毒剂 |
您最近一年使用:0次
2020-07-27更新
|
663次组卷
|
2卷引用:山东省枣庄市2019-2020学年高二下学期期末考试化学试题
名校
解题方法
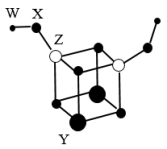
6 . 短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素可以组成一种分子簇,其分子结构如图所示(球大小表示原子半径的相对大小),W、X位于不同周期,X原子的最外层电子数是次外层电子数的3倍,Z的族序数等于其周期数,下列说法中一定正确的是

| A.X可以分别与W、Y可形成化合物W2X2、Y2X2 |
| B.工业上获得Y、Z单质均可采用电解它们的熔融氯化物 |
| C.简单离子半径: Z>Y>X>W |
| D.相同条件下,Y单质的沸点比Z单质的低 |
您最近一年使用:0次
2020-12-17更新
|
2440次组卷
|
9卷引用:四川省成都市石室中学2021届高三一诊模拟化学试题
四川省成都市石室中学2021届高三一诊模拟化学试题江西省新余市第四中学2021届高三上学期第五次段考化学试题(已下线)解密05 物质结构元素周期律(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密05 物质结构元素周期律(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练山东省新泰市第一中学2020-2021学年高二下学期第一次阶段性考试化学试题山东省泰安市宁阳县第四中学2021-2022学年高二下学期第一次段考化学试题河南省洛阳市2022届高三第二次统一考试(二模)理综化学试题(已下线)第五章 物质结构 元素周期律(测)-2023年高考化学一轮复习讲练测(全国通用)山东省新泰市第一中学东校2022-2023学年高二下学期第一次质量检测化学试题
名校
7 . 短周期主族元素X、Y、Z和W的原子序数依次增大,X、Y、W位于不同周期,Y、Z、W的原子最外层电子数之和为14,Z的原子半径在短周期主族元素中最大。下列说法错误的是( )
| A.简单离子半径:W>Z>X |
| B.W的最高价氧化物对应的水化物为强酸 |
| C.Y与Z形成的化合物溶于水所得溶液呈碱性 |
| D.与X形成的简单化合物的还原性:Y>Z>W |
您最近一年使用:0次
2020-04-03更新
|
2682次组卷
|
4卷引用:福建省泉州市2020届高三下学期3月适应性线上测试卷理综化学试题
福建省泉州市2020届高三下学期3月适应性线上测试卷理综化学试题解题达人.化学选择题(2021全国卷)提升小卷16(已下线)押新高考卷06题 元素周期表元素周期律-备战2022年高考化学临考题号押题(新高考通版)江西省安义中学2022-2023学年高三上学期中考试化学试题



