10-11高二下·山东烟台·期末
1 . “人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂。某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是
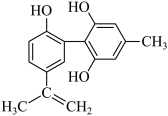
A.遇 溶液显紫色,因为该物质与苯酚属于同系物 溶液显紫色,因为该物质与苯酚属于同系物 |
B.滴入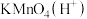 溶液,观察紫色褪去,能证明结构中存在碳碳双键 溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
C. 该物质与浓溴水和 该物质与浓溴水和 反应最多消耗 反应最多消耗 和 和 分别为 分别为 、 、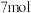 |
| D.该分子中的所有碳原子不可能共平面 |
您最近一年使用:0次
2023-03-26更新
|
264次组卷
|
11卷引用:2010—2011学年山东省烟台市高二下学期期末模块检测化学试卷
(已下线)2010—2011学年山东省烟台市高二下学期期末模块检测化学试卷(已下线)2011-2012学年浙江省温州八校高二上学期期末联考化学试卷(已下线)2012-2013学年浙江省杭州地区七校高二期中联考化学试卷(已下线)2012-2013学年山东省聊城市某重点中学高二第四次模块检测化学试卷(已下线)2013-2014学年湖南省衡阳市八中高二上学期期中考试化学试卷(已下线)2013-2014湖南省衡阳市八中上学期期中考试高二化学试卷2014-2015学年辽宁省沈阳市沈阳二中高二下期中化学试卷山西省怀仁县第八中学2016-2017学年高二(普通班)下学期期末考试化学试题陕西省渭南市尚德中学2018-2019学年高二下学期期中考试化学试题北京市海淀区教师进修学校2022-2023学年高二下学期3月月考化学试题河南省商丘市十校联考2023-2024学年高二下学期期末考试化学试题
名校
解题方法
2 . 富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如图:

已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
(1)上述流程中能加快反应速率的措施有__ 、__ 等。
(2)酸浸时发生反应:2MgO·SiO2+2H2SO4=2MgSO4+SiO2+2H2O,2MgO·B2O3+2H2SO4+H2O=2H3BO3+2MgSO4。
①酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式:__ 、__ 。
②已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3+OH-=B(OH) 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是___ (填序号)。
a.硼酸是一元酸
b.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
c.硼酸的电离方程式可表示为:H3BO3+H2O B(OH)
B(OH) +H+
+H+
(3)检验褐色浸出液中的杂质离子:取少量浸出液,__ (填操作和现象),证明溶液中含有Fe2+。
(4)除去浸出液中的杂质离子:用MgO调节溶液的pH至__ 以上,使杂质离子转化为__ (填化学式)沉淀,过滤。

已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
| 完全沉淀时 | 3.2 | 4.7 | 9.0 | 11.1 |
(2)酸浸时发生反应:2MgO·SiO2+2H2SO4=2MgSO4+SiO2+2H2O,2MgO·B2O3+2H2SO4+H2O=2H3BO3+2MgSO4。
①酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式:
②已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3+OH-=B(OH)
 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是a.硼酸是一元酸
b.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
c.硼酸的电离方程式可表示为:H3BO3+H2O
 B(OH)
B(OH) +H+
+H+(3)检验褐色浸出液中的杂质离子:取少量浸出液,
(4)除去浸出液中的杂质离子:用MgO调节溶液的pH至
您最近一年使用:0次
2020-12-25更新
|
176次组卷
|
2卷引用:福建省福州市福清西山学校高中部2021届高三12月月考化学试题
20-21高三上·浙江绍兴·期中
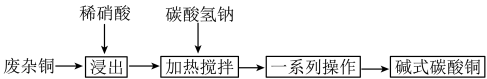
3 . 碱式碳酸铜的应用范围非常广泛,可以用来制备各种铜化合物,也可以用来制备催化剂等。现以印刷电路板废杂铜为原料制取碱式碳酸铜流程如下:
已知:
a.2Cu(NO3)2 + 4NaHCO3= Cu2(OH)2CO3↓+ 4NaNO3+ 3CO2↑+ H2O
2Cu + 6NH3 + 2NH4HCO3+ O2 2Cu(NH3)4CO3+ 2H2O
2Cu(NH3)4CO3+ 2H2O
2Cu(NH3)4CO3+ H2O Cu2(OH)2CO3↓+ CO2↑+ 8NH3↑
Cu2(OH)2CO3↓+ CO2↑+ 8NH3↑
b.碱式碳酸铜在沸水中易分解,在空气中200 ℃分解。
c.碱性条件下有利于大颗粒碱式碳酸铜的生成。
d.Cu(NH3)4CO3 溶液显蓝色,Cu2(OH)2CO3 固体显草绿色。
请回答:
(1)为了得到较大颗粒的碱式碳酸铜,混合碳酸氢钠和硝酸铜的操作方法是___________ 。
(2)下列有关“一系列操作”说法正确的是___________ 。
A.为了更好的洗去产品表面杂质,应用沸水洗涤
B.抽滤时用倾析法先转移溶液,开大水龙头,待溶液快流尽时再转移沉淀
C.烘干时,若温度过低,则干燥速率太慢,温度过高则易使产品分解
D.洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀物
(3)由于上述方法反应时间长、污染环境、资源浪费,现用“氨浸一脱氨一干燥”工艺制备碱式碳酸铜,氨浸过程装置如下:
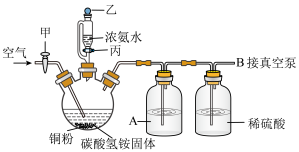
①氨浸过程的正确操作步骤为(选出正确的操作并按序排列):___________ →在三颈烧瓶中加入废杂铜和碳酸氢铵固体→___________ →三颈烧瓶用水浴加热至55-60 ℃___________ →___________ →关闭真空泵,关闭活塞甲,停止加热。
A.打开活塞乙,打开旋塞丙,加入浓氨水,关闭旋塞丙,关闭活塞乙
B.打开活塞甲
C.开启真空泵。
D.打开旋塞丙,加入浓氨水,关闭旋塞丙
E.检查装置气密性
②为实现氨的循环,装置A中试剂是___________ 。
③鼓入空气的作用除提供氧化剂以外,还可以是___________ 。
④脱氨过程需要105±5℃, 采用适宜的加热方式是___________ 。设计一个能证明脱氨已经完成的实验方案。___________ 。

已知:
a.2Cu(NO3)2 + 4NaHCO3= Cu2(OH)2CO3↓+ 4NaNO3+ 3CO2↑+ H2O
2Cu + 6NH3 + 2NH4HCO3+ O2
 2Cu(NH3)4CO3+ 2H2O
2Cu(NH3)4CO3+ 2H2O2Cu(NH3)4CO3+ H2O
 Cu2(OH)2CO3↓+ CO2↑+ 8NH3↑
Cu2(OH)2CO3↓+ CO2↑+ 8NH3↑b.碱式碳酸铜在沸水中易分解,在空气中200 ℃分解。
c.碱性条件下有利于大颗粒碱式碳酸铜的生成。
d.Cu(NH3)4CO3 溶液显蓝色,Cu2(OH)2CO3 固体显草绿色。
请回答:
(1)为了得到较大颗粒的碱式碳酸铜,混合碳酸氢钠和硝酸铜的操作方法是
(2)下列有关“一系列操作”说法正确的是
A.为了更好的洗去产品表面杂质,应用沸水洗涤
B.抽滤时用倾析法先转移溶液,开大水龙头,待溶液快流尽时再转移沉淀
C.烘干时,若温度过低,则干燥速率太慢,温度过高则易使产品分解
D.洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀物
(3)由于上述方法反应时间长、污染环境、资源浪费,现用“氨浸一脱氨一干燥”工艺制备碱式碳酸铜,氨浸过程装置如下:

①氨浸过程的正确操作步骤为(选出正确的操作并按序排列):
A.打开活塞乙,打开旋塞丙,加入浓氨水,关闭旋塞丙,关闭活塞乙
B.打开活塞甲
C.开启真空泵。
D.打开旋塞丙,加入浓氨水,关闭旋塞丙
E.检查装置气密性
②为实现氨的循环,装置A中试剂是
③鼓入空气的作用除提供氧化剂以外,还可以是
④脱氨过程需要105±5℃, 采用适宜的加热方式是
您最近一年使用:0次
解题方法
4 . 富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:
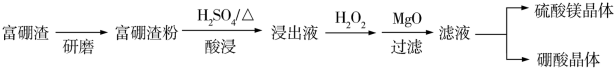
已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
(1)上述流程中能加快反应速率的措施有______ 、_______ 等。
(2)酸浸时发生反应:2MgO·SiO2 + 2H2SO4=2MgSO4 + SiO2 + 2H2O,2MgO·B2O3+ 2H2SO4 + H2O=2H3BO3 + 2MgSO4。
①上述反应体现出酸性强弱:H2SO4______ H3BO3(填“>”或“<”)。
②酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式:______ 、____________________ 。
③ 已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3 + OH- =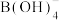 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是__________ (填序号)。
a. 硼酸是一元酸
b. 向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
c. 硼酸的电离方程式可表示为:H3BO3 + H2O B(OH)4-+H+
B(OH)4-+H+
(3)检验褐色浸出液中的杂质离子:取少量浸出液,________________________ (填操作和现象),证明溶液中含有Fe2+。
(4)除去浸出液中的杂质离子: 用MgO调节溶液的pH至______ 以上,使杂质离子转化为____________________ (填化学式)沉淀,过滤。
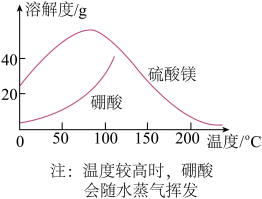
(5)获取晶体:ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;ⅱ.控制温度使两种晶体分别从溶液中结晶。结合如图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中,升温结晶得到___________ 晶体,分离后,再将母液降温结晶,分离得到_____________ 晶体。
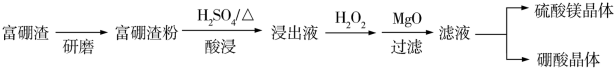
已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
| 完全沉淀时 | 3.2 | 4.7 | 9.0 | 11.1 |
(2)酸浸时发生反应:2MgO·SiO2 + 2H2SO4=2MgSO4 + SiO2 + 2H2O,2MgO·B2O3+ 2H2SO4 + H2O=2H3BO3 + 2MgSO4。
①上述反应体现出酸性强弱:H2SO4
②酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式:
③ 已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3 + OH- =
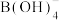 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是a. 硼酸是一元酸
b. 向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
c. 硼酸的电离方程式可表示为:H3BO3 + H2O
 B(OH)4-+H+
B(OH)4-+H+(3)检验褐色浸出液中的杂质离子:取少量浸出液,
(4)除去浸出液中的杂质离子: 用MgO调节溶液的pH至
(5)获取晶体:ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;ⅱ.控制温度使两种晶体分别从溶液中结晶。结合如图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中,升温结晶得到

您最近一年使用:0次
名校
解题方法
5 . 铁是日常生活中最常见的金属,某班同学在学习铁的知识时,有下列问题:
问题1:铁为何称为黑色金属?
问题2:CuO在高温下可分解为Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?
(1)对于问题1,同学们上网查找,有两种解释:
A.因为在铁表面上有黑色的铁的氧化物,所以叫黑色金属
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属
①你认为正确的说法是__________ 。
②若有一黑色粉末,如何鉴别是铁粉,还是Fe3O4?______________________________________ 。
③若有一黑色粉末,为铁和四氧化三铁的混合物,如何证明其中有Fe3O4(只要求简述实验方法)?____________________________________ 。
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A.将三氧化二铁高温灼烧,看灼烧前后颜色是否变化。
B.将三氧化二铁高温灼烧,看灼烧前后质量是否变化。
①实验中应将Fe2O3放在__________ (填仪器名称)中灼烧。
②方法A中,如果高温灼烧后颜色由__________ 变为__________ ,说明Fe2O3确实发生了变化。能说明生成的一定为FeO吗?__________ ,理由是________________________ 。
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为________ ,但是,实验结果固体灼烧前后质量比为30∶29,则高温灼烧后生成物是____________________ 。
④比较两种方法,你认为较好的方法是__________ 。
问题1:铁为何称为黑色金属?
问题2:CuO在高温下可分解为Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?
(1)对于问题1,同学们上网查找,有两种解释:
A.因为在铁表面上有黑色的铁的氧化物,所以叫黑色金属
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属
①你认为正确的说法是
②若有一黑色粉末,如何鉴别是铁粉,还是Fe3O4?
③若有一黑色粉末,为铁和四氧化三铁的混合物,如何证明其中有Fe3O4(只要求简述实验方法)?
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A.将三氧化二铁高温灼烧,看灼烧前后颜色是否变化。
B.将三氧化二铁高温灼烧,看灼烧前后质量是否变化。
①实验中应将Fe2O3放在
②方法A中,如果高温灼烧后颜色由
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为
④比较两种方法,你认为较好的方法是
您最近一年使用:0次
解题方法
6 .
(1)下列有关说法正确的是____ 。
A.用pH试纸测得新制氯水的pH为4
B.碳酸钠和硫酸钡可按溶解、过滤、蒸发的操作顺序分离
C.除去C2H5OH中的CH3COOH,先加足量的氢氧化钠溶液,再分液
D.溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则该溶液中一定存在
E.将乙醇与浓硫酸共热制得的气体通入酸性 溶液中,检验气体中是否含有乙烯
溶液中,检验气体中是否含有乙烯
F.用铂丝灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,没有K+
G.金属氧化物不一定是碱性氧化物,但碱性氧化物一定是金属氧化物;非金属氧化物不一定是酸性氧化物,酸性氧化物也不一定是非金属氧化物
H.在两个容积相同的容器中,一盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器内的气体一定具有相同的原子数
I.实验室配制1mol/L盐酸250mL,需要的仪器只有:250mL容量瓶、胶头滴管、量筒和烧杯
J.在NH4Al(SO4)2(一种复盐)的溶液中加入Ba(OH)2溶液至沉淀的质量达到最大时:

K.硝酸钡溶液中通入足量的SO2: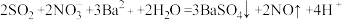
(2)ClO2的制备方法比较实用的有数十种,下列是几种常见的方法.
①方法一: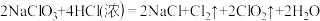
对于该反应,下列说法中正确的是_____ 。
A.该反应中Cl2是氧化产物
B.该反应中NaCl、ClO2是还原产物
C.在反应中HCl既作氧化剂又具有酸的作用
D.1mol NaClO3参加反应时,有1mol电子发生转移
E.1mol NaClO3参加反应,理论上能得到33.6L气体
方法二:氯化钠电解法
该法工艺原理如图。

②其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。指出工艺中方框中物质为______ (填化学式),理由为_______ 。
③将NCl3与NaClO2(亚氯酸钠)按物质的量之比1:6混合,在碱性溶液中恰好反应生成ClO2,试写出该反应的离子方程式____ 。
(1)下列有关说法正确的是
A.用pH试纸测得新制氯水的pH为4
B.碳酸钠和硫酸钡可按溶解、过滤、蒸发的操作顺序分离
C.除去C2H5OH中的CH3COOH,先加足量的氢氧化钠溶液,再分液
D.溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则该溶液中一定存在

E.将乙醇与浓硫酸共热制得的气体通入酸性
 溶液中,检验气体中是否含有乙烯
溶液中,检验气体中是否含有乙烯F.用铂丝灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,没有K+
G.金属氧化物不一定是碱性氧化物,但碱性氧化物一定是金属氧化物;非金属氧化物不一定是酸性氧化物,酸性氧化物也不一定是非金属氧化物
H.在两个容积相同的容器中,一盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器内的气体一定具有相同的原子数
I.实验室配制1mol/L盐酸250mL,需要的仪器只有:250mL容量瓶、胶头滴管、量筒和烧杯
J.在NH4Al(SO4)2(一种复盐)的溶液中加入Ba(OH)2溶液至沉淀的质量达到最大时:

K.硝酸钡溶液中通入足量的SO2:
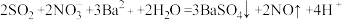
(2)ClO2的制备方法比较实用的有数十种,下列是几种常见的方法.
①方法一:
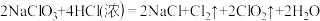
对于该反应,下列说法中正确的是
A.该反应中Cl2是氧化产物
B.该反应中NaCl、ClO2是还原产物
C.在反应中HCl既作氧化剂又具有酸的作用
D.1mol NaClO3参加反应时,有1mol电子发生转移
E.1mol NaClO3参加反应,理论上能得到33.6L气体
方法二:氯化钠电解法
该法工艺原理如图。

②其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。指出工艺中方框中物质为
③将NCl3与NaClO2(亚氯酸钠)按物质的量之比1:6混合,在碱性溶液中恰好反应生成ClO2,试写出该反应的离子方程式
您最近一年使用:0次
7 . 将SO2分别通入下列4种溶液中,有关说法不正确的是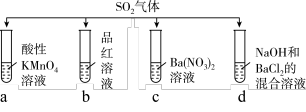
| A.试管a中实验可以证明SO2具有还原性 | B.试管b中溶液褪色,说明SO2具有漂白性 |
| C.试管c中能产生白色沉淀,说明SO2具有氧化性 | D.试管d中能产生白色沉淀,该沉淀不溶于稀硝酸 |
您最近一年使用:0次
2018-03-03更新
|
581次组卷
|
10卷引用:黑龙江省大庆实验中学2017-2018学年高一上学期期末考试化学试题
黑龙江省大庆实验中学2017-2018学年高一上学期期末考试化学试题鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第2节 硫的转化 课时1 硫、二氧化硫和三氧化硫高一必修第二册(人教2019版)第五章 第一节 硫及其化合物 课时1 硫和二氧化硫重庆实验中学2021届高三第一学月测试化学试题(已下线)4.1.1 二氧化硫的性质和应用(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)黑龙江省肇东市第四中学2021-2022学年高一下学期期中考试化学试题山东省枣庄市滕州市第五中学2022-2023学年高一上学期第二次线上考试化学试题广东省广州科学城中学2022-2023学年高一下学期期中考试化学试题作业(二十一) 实验室里研究不同价态硫元素之间的转化四川省华蓥中学2023-2024学年高一下学期5月期中化学试题
8 . 学兴趣小组同学在探究SO2与新制Cu(OH)2悬浊液反应,实验时发现了如下问题并展开实验探究,装置如图1:
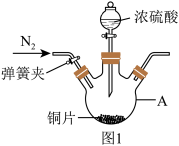
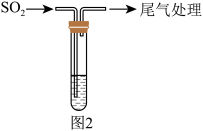
实验一:SO2的制备
(1)仪器A的名称是___ 。
(2)仪器A中加入浓硫酸加热产生的实验现象为___ 。实验前通入N2的目的是___ 。
实验二:探究SO2与新制Cu(OH)2悬浊液的反应
甲同学进行实验Ⅰ:在图2试管中滴加1.5mL1mol•L-1CuSO4溶液和3.5mL1mol•L-1NaOH溶液混合,开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,试管底部有少量紫红色固体,溶液呈蓝色。
乙同学进行实验Ⅱ:在试管中滴加1.5mL1mol•L-1CuCl2溶液和3.5mL1mol•L-1NaOH溶液混合,开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈蓝色。
(3)甲同学设计如下实验探究砖红色沉淀的主要成分。
取少量砖红色沉淀于试管中,加5mL蒸馏水,滴加少量稀硫酸,静置后观察到试管底部有少量紫红色固体,溶液呈蓝色,证明砖红色沉淀是___ (填“化学式”),发生的离子方程式为___ 。
(4)乙同学设计下列实验探究白色沉淀的主要成分。
向得到的19.9g白色沉淀中加入足量的稀硝酸,得到蓝色溶液;再向溶解后的溶液中加入足量的AgNO3溶液,过滤、洗涤、干燥,得到固体的质量为28.7g,则白色沉淀的化学式为___ ,加入足量的稀硝酸反应的离子方程式为___ 。
(5)丙同学针对实验和Ⅱ中出现的实验现象,重新用实验Ⅱ的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净,再向洗净后的Cu(OH)2中加入5mL蒸馏水,再持续通入SO2气体,得到的现象与实验Ⅰ相同,说明实验Ⅰ和Ⅱ现象不同的原因是___ 。


实验一:SO2的制备
(1)仪器A的名称是
(2)仪器A中加入浓硫酸加热产生的实验现象为
实验二:探究SO2与新制Cu(OH)2悬浊液的反应
甲同学进行实验Ⅰ:在图2试管中滴加1.5mL1mol•L-1CuSO4溶液和3.5mL1mol•L-1NaOH溶液混合,开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,试管底部有少量紫红色固体,溶液呈蓝色。
乙同学进行实验Ⅱ:在试管中滴加1.5mL1mol•L-1CuCl2溶液和3.5mL1mol•L-1NaOH溶液混合,开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈蓝色。
(3)甲同学设计如下实验探究砖红色沉淀的主要成分。
取少量砖红色沉淀于试管中,加5mL蒸馏水,滴加少量稀硫酸,静置后观察到试管底部有少量紫红色固体,溶液呈蓝色,证明砖红色沉淀是
(4)乙同学设计下列实验探究白色沉淀的主要成分。
向得到的19.9g白色沉淀中加入足量的稀硝酸,得到蓝色溶液;再向溶解后的溶液中加入足量的AgNO3溶液,过滤、洗涤、干燥,得到固体的质量为28.7g,则白色沉淀的化学式为
(5)丙同学针对实验和Ⅱ中出现的实验现象,重新用实验Ⅱ的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净,再向洗净后的Cu(OH)2中加入5mL蒸馏水,再持续通入SO2气体,得到的现象与实验Ⅰ相同,说明实验Ⅰ和Ⅱ现象不同的原因是
您最近一年使用:0次
9 . 高温超导材料的研究是21世纪材料领域的热点问题,YBaCuO体系一直是此领域的研究重点之一。将钇(Y)、钡、铜的氧化物按一定的物质的量之比混合(Y为ⅢB族元素),再经高温煅烧可得到复合氧化物YBa2Cu3O6.5+δ,实验证明:该物质具有超导性能,其零电阻温度可达90K,化学式中的δ大小与超导性能密切相关。有一种观点认为δ的产生源于体系中产生了Cu3+。
(1)经测定δ一般不大于0.50,按此推算,Cu3+ 占物质中总铜量的质量分数最大为_______ 。
(2)已知可用间接碘量法测出体系中Cu3+ 的质量分数,该法涉及的化学反应有:4Cu3++2H2O=4Cu2++O2+4H+,2Cu2++4I-=Cu2I2+I2,2S2O +I2=S4O
+I2=S4O +2I-等。现有两份质量都为m的该氧化物,其中一份加过量的KI固体,溶解后用浓度为0.1568mol/L的Na2S2O3 滴定至终点,消耗Na2S2O3 的体积为30.26mL,另一份先完全溶解,再加和第一份等量的KI固体,用同样浓度的Na2S2O3 滴定至终点,消耗的体积为23.89mL,该氧化物中Cu3+ 的质量分数为
+2I-等。现有两份质量都为m的该氧化物,其中一份加过量的KI固体,溶解后用浓度为0.1568mol/L的Na2S2O3 滴定至终点,消耗Na2S2O3 的体积为30.26mL,另一份先完全溶解,再加和第一份等量的KI固体,用同样浓度的Na2S2O3 滴定至终点,消耗的体积为23.89mL,该氧化物中Cu3+ 的质量分数为_______ ,m值为_______ 。
(1)经测定δ一般不大于0.50,按此推算,Cu3+ 占物质中总铜量的质量分数最大为
(2)已知可用间接碘量法测出体系中Cu3+ 的质量分数,该法涉及的化学反应有:4Cu3++2H2O=4Cu2++O2+4H+,2Cu2++4I-=Cu2I2+I2,2S2O
 +I2=S4O
+I2=S4O +2I-等。现有两份质量都为m的该氧化物,其中一份加过量的KI固体,溶解后用浓度为0.1568mol/L的Na2S2O3 滴定至终点,消耗Na2S2O3 的体积为30.26mL,另一份先完全溶解,再加和第一份等量的KI固体,用同样浓度的Na2S2O3 滴定至终点,消耗的体积为23.89mL,该氧化物中Cu3+ 的质量分数为
+2I-等。现有两份质量都为m的该氧化物,其中一份加过量的KI固体,溶解后用浓度为0.1568mol/L的Na2S2O3 滴定至终点,消耗Na2S2O3 的体积为30.26mL,另一份先完全溶解,再加和第一份等量的KI固体,用同样浓度的Na2S2O3 滴定至终点,消耗的体积为23.89mL,该氧化物中Cu3+ 的质量分数为
您最近一年使用:0次
名校
解题方法
10 . 如图所示,根据实验室制取氯气的原理制备氯气并进行性质验证,回答下列问题:
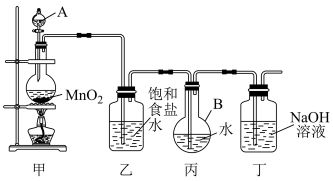
(1)写出装置甲中发生反应的化学方程式:___________ 。装置甲中的仪器使用前需要检漏的是___________ (写名称)。
(2)利用装置丙制取饱和氯水并测其pH。
①证明氯水已饱和的现象是___________ 。
②若撤去装置乙,直接将装置甲和丙相连,这样做对实验测定结果的影响是___________ 。
(3)饱和氯水与石灰石的反应是制取较浓的HClO溶液的方法之一、某同学运用这一方法,尝试制取HClO溶液并进行了如下定性实验:
ⅰ.在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量无色气泡产生,溶液的黄绿色褪去;
ⅱ.过滤,将滤液滴在有色布条上,发现其漂白性比饱和氯水更强;
ⅲ.为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与澄清石灰水混合,立即产生白色沉淀。
第二份与稀盐酸混合,立刻产生大量无色气体。
第三份加热,看到溶液变浑浊且有无色气体产生。
经检测,上述实验中产生的无色气体均为CO2气体。
①试根据所学知识推测,在ⅱ的滤液中除了溶解的极少量氯气外,还含有的其他溶质为___________ (写化学式)。
②写出步骤ⅲ中第一份滤液发生反应的离子方程式:___________ 。

(1)写出装置甲中发生反应的化学方程式:
(2)利用装置丙制取饱和氯水并测其pH。
①证明氯水已饱和的现象是
②若撤去装置乙,直接将装置甲和丙相连,这样做对实验测定结果的影响是
(3)饱和氯水与石灰石的反应是制取较浓的HClO溶液的方法之一、某同学运用这一方法,尝试制取HClO溶液并进行了如下定性实验:
ⅰ.在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量无色气泡产生,溶液的黄绿色褪去;
ⅱ.过滤,将滤液滴在有色布条上,发现其漂白性比饱和氯水更强;
ⅲ.为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与澄清石灰水混合,立即产生白色沉淀。
第二份与稀盐酸混合,立刻产生大量无色气体。
第三份加热,看到溶液变浑浊且有无色气体产生。
经检测,上述实验中产生的无色气体均为CO2气体。
①试根据所学知识推测,在ⅱ的滤液中除了溶解的极少量氯气外,还含有的其他溶质为
②写出步骤ⅲ中第一份滤液发生反应的离子方程式:
您最近一年使用:0次
2021-11-13更新
|
193次组卷
|
4卷引用:山东省济宁市任城区2020-2021学年高一上学期期中考试化学试题
山东省济宁市任城区2020-2021学年高一上学期期中考试化学试题(已下线)练习7 氧化还原反应-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)河南省商丘名校2021-2022学年高一上学期期中联考化学试题河南省虞城县高级中学2021-2022学年高一上学期中考试化学试题



