名校
解题方法
1 . W、X、Y、Z为原子序数依次增大的短周期主族元素,其原子的最外层电子数之和为18,W和Y同主族,X、Y、Z同周期,X原子的电子层数与最外层电子数相等,Z元素最高正价与最低负价的代数和为6.下列说法不正确的是
| A.Z的氧化物的水化物酸性一定大于W | B.W的某种单质的沸点比X高 |
| C.W与Y可形成一种硬度很大的化合物 | D.W、X、Y均能与Z形成共价化合物 |
您最近一年使用:0次
名校
解题方法
2 . 已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数为D的2倍。F元素在地壳中含量位于金属元素的第二位。试回答下列问题:
(1)F元素价层电子排布式为___________________ 。
(2)关于B2A2的下列说法中正确的是________________ 。
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中σ键和π键数目比为1∶1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的B-A键属于s—spσ键
(3) B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是________________ 。
(4) C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因__________ 。
(5) A与D可以形成原子个数比分别为2∶1,1∶1的两种化合物X和Y,其中 Y含有____________ 键(填“极性键”“非极性键”),A与C组成的两种化合物M和N所含的电子数分别与X、Y相 等,N的 结构式为________ 。
(6) E的氢化物的价层电子对互斥理论模型为________ ,E 原子的杂化方式为________ 杂化。
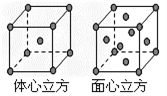
(7) F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为_________ ,F原子配位数之比为__________________ 。
(1)F元素价层电子排布式为
(2)关于B2A2的下列说法中正确的是
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中σ键和π键数目比为1∶1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的B-A键属于s—spσ键
(3) B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是
(4) C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因
(5) A与D可以形成原子个数比分别为2∶1,1∶1的两种化合物X和Y,其中 Y含有
(6) E的氢化物的价层电子对互斥理论模型为
(7) F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为

您最近一年使用:0次
2017-05-18更新
|
511次组卷
|
2卷引用:黑龙江省大庆实验中学2017届高三考前得分训练(一)理科综合化学试题2



