名校
1 . 在元素周期表中,应用于计算机芯片的硅元素如图所示,下列有关硅的说法正确


| A.原子核外有14个电子 | B.原子个数是14 |
| C.硅原子的相对原子质量是28.09 | D.质量数是28.09 |
您最近一年使用:0次
名校
解题方法
2 . 下列说法正确的是
| A.质子数相同的粒子一定属于同一种元素 |
| B.不同元素原子的质量数一定不等 |
| C.质子数决定元素的种类,质子数和中子数决定原子的种类 |
| D.质子数相同的微粒,核外电子数一定相同,但化学性质不一定相同 |
您最近一年使用:0次
3 . 硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(1) 是硅的一种同位素,其原子核内质子数为
是硅的一种同位素,其原子核内质子数为_______ ,Si原子的电子式为_______ 。Si与C的化学性质相似,由此猜想二者在原子结构上的相似之处是_______ 。
(2)如图中,“28.09”的含义是指_______ 。
(3)硅元素在自然界中通常以石英石( )和硅酸盐的形式存在。已知
)和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式_______ 。0.1mol的硅酸根离子( )中含有质子
)中含有质子_______ mol,电子_______ 个。
(4)高纯硅单质可由石英砂(主要成分是SiO2)制得,制备高纯硅的主要工艺流程如图所示:

i.硅元素有无定形硅和晶体硅两种单质,他们互为_______ ;
ii.流程①焦炭体现了_______ (填“氧化性”或“还原性”)。
iii.流程④的化学反应为置换反应,写出其化学方程式:_______ 。
(1)
 是硅的一种同位素,其原子核内质子数为
是硅的一种同位素,其原子核内质子数为(2)如图中,“28.09”的含义是指
| 14 Si 硅 28.09 |
 )和硅酸盐的形式存在。已知
)和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式 )中含有质子
)中含有质子(4)高纯硅单质可由石英砂(主要成分是SiO2)制得,制备高纯硅的主要工艺流程如图所示:

i.硅元素有无定形硅和晶体硅两种单质,他们互为
ii.流程①焦炭体现了
iii.流程④的化学反应为置换反应,写出其化学方程式:
您最近一年使用:0次
名校
解题方法
4 . 2021年日本将核废水主要辐射物质“氚(T)”做成卡通形象,以合理化将放射性核废水排入太平洋的行为,进而引发国内外民众的严重不满。下列有关氚的说法正确的是


| A.卡通形象中标+号的小球表示中子 |
B.氚的核素符号为 |
| C.氚和及其同位素性质完全相同 |
D.11g氚水(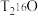 )所含中子数为6NA )所含中子数为6NA |
您最近一年使用:0次
5 . 对于1mol  和CO的混合气体,下列说法错误的是
和CO的混合气体,下列说法错误的是
 和CO的混合气体,下列说法错误的是
和CO的混合气体,下列说法错误的是| A.密度为1.25g/L | B.含有14mol质子 | C.质量为28g | D.共有NA个分子 |
您最近一年使用:0次
6 . 发现了电子的科学家是
| A.道尔顿 | B.卢瑟福 | C.汤姆孙 | D.玻尔 |
您最近一年使用:0次
名校
7 . 有A、B、C、D、E五种单核微粒:A原子核内有7个质子,7个中子,核外有7个电子;B微粒其电子层结构与氖原子相同,但其电子数比质子数多2个;C微粒核电荷数为11,并带有一个单位的正电荷;D微粒核外有10个电子,当得到2个电子后微粒呈电中性;E微粒呈电中性且核内无中子。
(1)依次写出A、B、C、D四种微粒的符号:_______ 、_______ 、_______ 、_______ 。
(2)写出两种由上述元素组成的含有10个电子的多核微粒的符号_______ 、_______ 。
(1)依次写出A、B、C、D四种微粒的符号:
(2)写出两种由上述元素组成的含有10个电子的多核微粒的符号
您最近一年使用:0次
名校
解题方法
8 . 研究人员在地壳深处的热液中发现能稳定存在的 离子,下列关于
离子,下列关于 说法正确的是
说法正确的是
 离子,下列关于
离子,下列关于 说法正确的是
说法正确的是A.一个 含有47个电子 含有47个电子 | B.一个 含有48个质子 含有48个质子 |
C.与 (硫磺)互为同素异形体 (硫磺)互为同素异形体 | D.通常状况下, 在水中能稳定存在 在水中能稳定存在 |
您最近一年使用:0次
名校
解题方法
9 . 原子的种类决定于
| A.质子数 | B.中子数和电子数 |
| C.质子数和中子数 | D.质量数 |
您最近一年使用:0次
名校
解题方法
10 . 人类认识原子结构的历史中,科学家汤姆孙做出的重要贡献是
| A.创立了近代原子论 | B.提出了原子结构的有核模型 |
| C.创立了现代原子论 | D.提出了葡萄干面包原子模型 |
您最近一年使用:0次



