解题方法
1 . 有A、B、C、X四种微粒。请根据已知信息,回答下列问题:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后,其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④X微粒不带电,原子核中只有一个质子,两个中子。
(1)写出以下微粒的化学符号:A___________ ,B___________ ,C___________ 。
(2)B微粒的结构示意图为___________ ,11g的X2O含有的中子数目为___________ 。(用NA表示阿伏伽德罗常数)
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后,其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④X微粒不带电,原子核中只有一个质子,两个中子。
(1)写出以下微粒的化学符号:A
(2)B微粒的结构示意图为
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题:
(1)填表,完成下列表格
(2)某微粒的结构示意图可表示为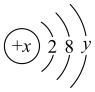 。
。
①当x=10+y时,该粒子为___________ (填“原子”“正离子”或“负离子”),当x<10+y时,该粒子为___________ 。
②当y=8时,若该微粒带有一个单位负电荷,则x=___________ ,该微粒的离子符号为___________ 。
③当y=5时,若该微粒为中性原子R,其质量数为31,则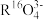 中含有的中子数为
中含有的中子数为___________ 。
(1)填表,完成下列表格
| 微粒名称 | 微粒结构示意图 | 电子式 |
| 硫离子 | ||
| 氩原子 | ||
| 镁离子 |
(2)某微粒的结构示意图可表示为
 。
。①当x=10+y时,该粒子为
②当y=8时,若该微粒带有一个单位负电荷,则x=
③当y=5时,若该微粒为中性原子R,其质量数为31,则
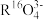 中含有的中子数为
中含有的中子数为
您最近一年使用:0次
名校
解题方法
3 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期类”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)请补全汞的原子结构示意图___________ 。
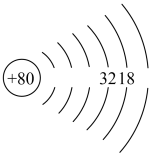
(2)自然界的水银内含7种核素: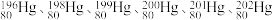 和
和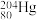 ,其中,
,其中,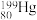 和
和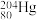 的中子数之比为
的中子数之比为___________ 。
(3)硫磺可用于制作黑火药,爆炸时的反应为: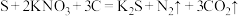 。
。
①上述反应所涉及元素中,某元素原子得到两个电子即可形成2、8的电子层结构,该元素的名称是___________ ,它与氢形成的10电子微粒有___________ 种;某元素的 层电子数是其电子总数的
层电子数是其电子总数的 ,则其简单离子的电子式为
,则其简单离子的电子式为___________ 。
②已知一般情况下原子核外最外层电子数相等的元素具有相似的化学性质。下列原子中与钾元素原子的化学性质相似的是___________ 。
(4)高纯度陶瓷氮化硅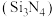 可由石英与焦炭在高温的氮气流中通过所给反应得到:
可由石英与焦炭在高温的氮气流中通过所给反应得到:
①反应后恢复至室温,得到混合气体的平均相对分子质量为___________ 。
②若反应生成 气体(标准状况),则生成的
气体(标准状况),则生成的 质量为
质量为___________ (保留两位小数)。
(1)请补全汞的原子结构示意图

(2)自然界的水银内含7种核素:
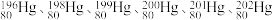 和
和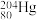 ,其中,
,其中,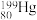 和
和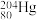 的中子数之比为
的中子数之比为(3)硫磺可用于制作黑火药,爆炸时的反应为:
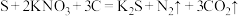 。
。①上述反应所涉及元素中,某元素原子得到两个电子即可形成2、8的电子层结构,该元素的名称是
 层电子数是其电子总数的
层电子数是其电子总数的 ,则其简单离子的电子式为
,则其简单离子的电子式为②已知一般情况下原子核外最外层电子数相等的元素具有相似的化学性质。下列原子中与钾元素原子的化学性质相似的是
 |  | 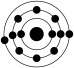 | 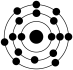 |
| A. | B. | C. | D. |
(4)高纯度陶瓷氮化硅
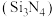 可由石英与焦炭在高温的氮气流中通过所给反应得到:
可由石英与焦炭在高温的氮气流中通过所给反应得到:
①反应后恢复至室温,得到混合气体的平均相对分子质量为
②若反应生成
 气体(标准状况),则生成的
气体(标准状况),则生成的 质量为
质量为
您最近一年使用:0次
名校
4 . 完成下列填空
(1)微粒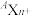 核外有18个电子,则它的核电荷数为
核外有18个电子,则它的核电荷数为__________ ,核内中子数为__________ 。
(2)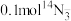 中共含
中共含__________ mol中子,含__________ 个电子。
(1)微粒
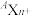 核外有18个电子,则它的核电荷数为
核外有18个电子,则它的核电荷数为(2)
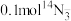 中共含
中共含
您最近一年使用:0次
5 . 填表:
| 微粒 | 核外电子数 | 中子数 | 质量数 | 最外层电子数 |
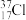 | ||||
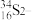 |
您最近一年使用:0次
名校
6 . 日本决定于2023年8月23日将福岛核电站的核污水排入大海,引起了国际上的关注和担忧。其中含有大量的放射性元素如角( ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。
(1)碘( )的质量数是
)的质量数是___________ ,中子数是___________ 。在生活中,我们也会摄入含碘( )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为___________ 。
(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
(3)碳( )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式___________ 。
(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图___________ ,___________ ,___________ 。
 ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。(1)碘(
 )的质量数是
)的质量数是 )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
| A.一种氢原子的质量数 | B.氢元素的近似相对原子质量 |
| C.三种氢原子的平均相对原子质量 | D.氢元素的相对原子质量 |
 )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图
您最近一年使用:0次
7 . 回答下列问题。
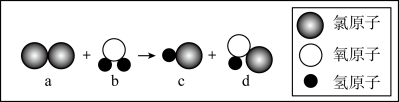
(1)仔细观察下图的微观反应过程,写出该化学反应方程式___________ 。
(2)画出氧原子的结构示意图___________ 。
(3)电解水时,为增强水的导电性,通常向纯水中加入适量的NaOH(NaOH不参加反应)。
①某电解水实验开始时,向180g纯水中溶解了4g NaOH.此时溶液中 和水分子的个数比是
和水分子的个数比是___________ 。
②当实验进行到一段时间,两个电极共收集到的气体折合成标准状况约是6.72L(不考虑气体溶解)。计算此时被电解的水的物质的量是___________ 。
③实际收集气体的外界条件并非标况。假如该条件下气体摩尔体积是C L/mol,阿伏伽德罗常数的值是 ,当收集到氢气的体积是V L时,则同时收集到的氧气分子的个数是
,当收集到氢气的体积是V L时,则同时收集到的氧气分子的个数是___________ 。
(1)仔细观察下图的微观反应过程,写出该化学反应方程式

(2)画出氧原子的结构示意图
(3)电解水时,为增强水的导电性,通常向纯水中加入适量的NaOH(NaOH不参加反应)。
①某电解水实验开始时,向180g纯水中溶解了4g NaOH.此时溶液中
 和水分子的个数比是
和水分子的个数比是②当实验进行到一段时间,两个电极共收集到的气体折合成标准状况约是6.72L(不考虑气体溶解)。计算此时被电解的水的物质的量是
③实际收集气体的外界条件并非标况。假如该条件下气体摩尔体积是C L/mol,阿伏伽德罗常数的值是
 ,当收集到氢气的体积是V L时,则同时收集到的氧气分子的个数是
,当收集到氢气的体积是V L时,则同时收集到的氧气分子的个数是
您最近一年使用:0次
8 . 2l.在①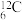 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 等核素中:(填序号)
等核素中:(填序号)
(1)___________ 和___________ 互为同位素。
(2)___________ 和___________ 质量数相等,但不属于同一种元素。
(3)___________ 和___________ 中子数相等,但质子数不相等。
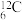 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 等核素中:(填序号)
等核素中:(填序号)(1)
(2)
(3)
您最近一年使用:0次
名校
解题方法
9 . 钠是一种非常活泼、具有广泛应用的金属
(1)钠与水反应的化学方程式是___________ 。
(2)钠的原子结构示意图为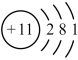 ,钠在反应中容易
,钠在反应中容易_______ 电子(填“得到”或“失去”)。
(3)金属钠非常活泼,通常保存在___________ 里,以隔绝空气。
(4)汽车安全气囊的气体发生剂 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。
①当汽车发生较严重的碰撞时,引发 分解:
分解: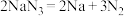 ,从而为气囊充气,该反应属于
,从而为气囊充气,该反应属于___________ 反应(填基本反应类型)。
②产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是___________ 。
③ 是冷却剂,受热过程中发生反应,同时吸收安全气囊的气体发生剂释放的热量。
是冷却剂,受热过程中发生反应,同时吸收安全气囊的气体发生剂释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为___________ 。
(1)钠与水反应的化学方程式是
(2)钠的原子结构示意图为
 ,钠在反应中容易
,钠在反应中容易(3)金属钠非常活泼,通常保存在
(4)汽车安全气囊的气体发生剂
 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。①当汽车发生较严重的碰撞时,引发
 分解:
分解: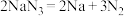 ,从而为气囊充气,该反应属于
,从而为气囊充气,该反应属于②产生的Na立即与
 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是③
 是冷却剂,受热过程中发生反应,同时吸收安全气囊的气体发生剂释放的热量。
是冷却剂,受热过程中发生反应,同时吸收安全气囊的气体发生剂释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为
您最近一年使用:0次
名校
10 . 按要求填空。
(1)33.3g某金属氯化物 中含有
中含有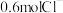 ,则M的相对原子质量为
,则M的相对原子质量为_______ 。
(2)标准状况下,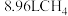 和
和 的混合气体,其质量为7.6g,则混合气体中
的混合气体,其质量为7.6g,则混合气体中 的体积为
的体积为_______ L, 的质量为
的质量为_______ g。
(3) 个
个 约含
约含_______ 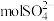 ,其质量为
,其质量为_______ g。
(4)中子数为18的硫原子,其微粒符号可表示为_______ 。
(5)质量数为37、中子数为20的原子,其结构示意图可表示为_______ 。
(6)已知Mm+的电子数为a,M的质量数为A,则 的M的中子数为
的M的中子数为_______ 。
(1)33.3g某金属氯化物
 中含有
中含有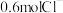 ,则M的相对原子质量为
,则M的相对原子质量为(2)标准状况下,
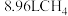 和
和 的混合气体,其质量为7.6g,则混合气体中
的混合气体,其质量为7.6g,则混合气体中 的体积为
的体积为 的质量为
的质量为(3)
 个
个 约含
约含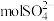 ,其质量为
,其质量为(4)中子数为18的硫原子,其微粒符号可表示为
(5)质量数为37、中子数为20的原子,其结构示意图可表示为
(6)已知Mm+的电子数为a,M的质量数为A,则
 的M的中子数为
的M的中子数为
您最近一年使用:0次
2023-08-08更新
|
152次组卷
|
2卷引用:福建省福州市八县市协作校2022-2023学年高一上学期期中联考化学试题



