名校
解题方法
1 . 按要求填空
(1) 中有
中有_______  质子,
质子,_______  中子,
中子,_______ 个电子。
(2)同温同压下,两种气体A和B的体积比为2∶1,质量比为8∶5,摩尔质量之比为_______ 。
(3)同温同压下,同体积的氨气和硫化氢气体的质量比是_______ ;同质量的氨气和硫化氢气体的体积比是_______ ;若两者所含氢原子个数相同,它们的物质的量之比为_______ 。
(4)某混合气体中,各气体的体积分数为: 、
、 、
、 、
、 ,则此混合气体的平均相对分子质量为
,则此混合气体的平均相对分子质量为_______ ,其对于氢气的密度为_______ 。
(5)在 、
、 下,有
下,有 和
和 混合气体共
混合气体共 ,经点燃后恢复到原状态时,混合气体的体积减少为
,经点燃后恢复到原状态时,混合气体的体积减少为 ,则原混合气体中
,则原混合气体中 的体积为
的体积为_______  。
。
(6)将某文献资料上记载的相对原子质量数据摘录如表所示:
则 的相对原子质量=
的相对原子质量=_______ (保留三位小数)。
(7)在 、
、 、
、 、
、 、
、 等物质中,只存在离子键的是
等物质中,只存在离子键的是_______ ;只存在共价键的是_______ ;既存在离子键又存在共价键的是_______ ;不存在化学键的是_______ 。
(8)下列变化中:①碘的升华;②烧碱熔化;③氯化钠溶于水;④氧气溶于水;⑤氯化氢溶于水;⑥氯化铵受热分解为氯化氢和氨气。(填序号)。化学键没有被破坏的是_______ ;仅发生离子键破坏的是_______ ;仅发生共价键破坏的是_______ ;既发生离子键又发生共价键破坏的是_______ 。
(1)
 中有
中有 质子,
质子, 中子,
中子,(2)同温同压下,两种气体A和B的体积比为2∶1,质量比为8∶5,摩尔质量之比为
(3)同温同压下,同体积的氨气和硫化氢气体的质量比是
(4)某混合气体中,各气体的体积分数为:
 、
、 、
、 、
、 ,则此混合气体的平均相对分子质量为
,则此混合气体的平均相对分子质量为(5)在
 、
、 下,有
下,有 和
和 混合气体共
混合气体共 ,经点燃后恢复到原状态时,混合气体的体积减少为
,经点燃后恢复到原状态时,混合气体的体积减少为 ,则原混合气体中
,则原混合气体中 的体积为
的体积为 。
。(6)将某文献资料上记载的相对原子质量数据摘录如表所示:
| 原子 | 相对原子质量 | 质量数 | 丰度 | 元素的相对原子质量 | 元素的近似相对原子质量 |
 | 62.928 | 63 | 69.15% | 63.546 | 63.618 |
 | _______ | 65 | 30.85% |
则
 的相对原子质量=
的相对原子质量=(7)在
 、
、 、
、 、
、 、
、 等物质中,只存在离子键的是
等物质中,只存在离子键的是(8)下列变化中:①碘的升华;②烧碱熔化;③氯化钠溶于水;④氧气溶于水;⑤氯化氢溶于水;⑥氯化铵受热分解为氯化氢和氨气。(填序号)。化学键没有被破坏的是
您最近一年使用:0次
名校
解题方法
2 . 按要求填空
(1)写出溴原子的核外电子排布式_______
(2)写出氮原子的轨道表示式_________
(3)请解释Fe3+比Fe2+稳定的原因________
(4)由23Na、35Cl、37Cl构成的15g氯化钠中,37Cl的质量为_______
(1)写出溴原子的核外电子排布式
(2)写出氮原子的轨道表示式
(3)请解释Fe3+比Fe2+稳定的原因
(4)由23Na、35Cl、37Cl构成的15g氯化钠中,37Cl的质量为
您最近一年使用:0次
20-21高一上·全国·课时练习
解题方法
3 . 据推测,哈雷彗星上碳的两种同位素12C和13C的原子个数比为65:1,而地球上12C和13C的原子个数比为89:1,地球上碳元素的相对原子质量是12.011,那么哈雷彗星上碳元素的相对原子质量是________ 。
您最近一年使用:0次
解题方法
4 . 某废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图。
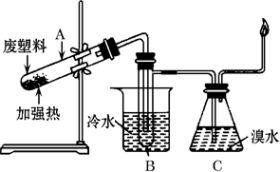
加热聚丙烯废塑料得到的产物如下表:
(1)试管A 中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
A 中残留物 电石
电石 乙炔
乙炔 聚乙炔
聚乙炔
写出反应③的化学方程式______
(2)试管B 收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,其一氯代物有___________ 种。
(3)经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为___________ 。

加热聚丙烯废塑料得到的产物如下表:
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
(1)试管A 中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
A 中残留物
 电石
电石 乙炔
乙炔 聚乙炔
聚乙炔写出反应③的化学方程式
(2)试管B 收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,其一氯代物有
(3)经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为
您最近一年使用:0次
名校
解题方法
5 . (1)第ⅢB族有___________ 种元素;
(2)第5周期第ⅤA族元素的元素名称为___________ ,原子序数为___________ ;
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为___________ ;
(4) 和
和 是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则
是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则 的相对原子质量为
的相对原子质量为___________ ,元素X的近似相对原子质量为___________ 。
(2)第5周期第ⅤA族元素的元素名称为
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为
(4)
 和
和 是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则
是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则 的相对原子质量为
的相对原子质量为
您最近一年使用:0次
2018高二·全国·专题练习
解题方法
6 . 现有下列粒子:1H、2H、3H、1H+、234U、235U、238U、40K、40Ca、37Cl、14N、14C,请回答下列问题:
(1)它们分属_____ 种元素,属于氢元素的核素有_____ 种,属于铀元素的核素有_____ 种。互为同位素的原子分别为__________ 。
(2)质量数相等的粒子为_______ 、_______ 、_______ 。
(3)氢的同位素1H、2H、3H与氧的同位素16O、17O、18O相互结合成水,所得水分子的种数为__________ ;可得相对分子质量不同的水分子的种数为__________ 。
(1)它们分属
(2)质量数相等的粒子为
(3)氢的同位素1H、2H、3H与氧的同位素16O、17O、18O相互结合成水,所得水分子的种数为
您最近一年使用:0次



