1 . 下列物质中既存在离子键又存在共价键的是
A. | B. | C. | D. |
您最近一年使用:0次
2023-02-06更新
|
378次组卷
|
2卷引用:江苏省丹阳高级中学2022-2023学年高二下学期合格性考试模拟化学试题
名校
解题方法
2 . 下图为NaCl在不同状态下的导电实验(X、Y均为石墨电极),下列说法错误的是
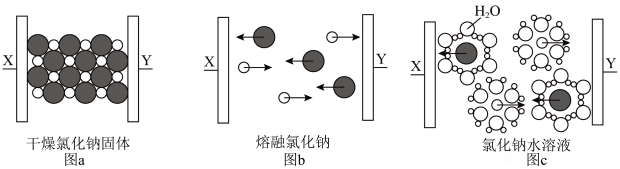

A.图示中“ ”代表的离子的电子式为 ”代表的离子的电子式为 |
| B.图a中放入的是氯化钠固体,该条件下氯化钠不导电 |
| C.图b和图c中发生的化学反应完全相同 |
| D.图b能证明氯化钠为离子化合物 |
您最近一年使用:0次
3 . 现有下列物质:①Cl2、②Na2O2、③NaOH、④HCl、⑤H2O2、⑥MgF2、⑦NH4Cl
(1)只由离子键构成的物质是___________ ;
(2)只由共价键构成的物质是___________ ;
(3)只由非金属元素组成的离子化合物是___________ ;
(4)由离子键和共价键构成的物质是___________ ;
(5)属于离子化合物的物质是___________ ;
(6)属于共价化合物的物质是___________ 。
(1)只由离子键构成的物质是
(2)只由共价键构成的物质是
(3)只由非金属元素组成的离子化合物是
(4)由离子键和共价键构成的物质是
(5)属于离子化合物的物质是
(6)属于共价化合物的物质是
您最近一年使用:0次
4 . 某元素原子最外层只有1个电子,它跟卤素相结合时,所形成的化学键
| A.一定是共价键 | B.一定是离子键 |
| C.可能是共价键,也可能是离子键 | D.以上说法均不正确 |
您最近一年使用:0次
5 . 下列表示正确的是
A.溴苯的分子式: |
B.用电子式表示氯化钠的形成过程: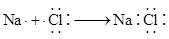 |
C.碳酸二甲酯的结构简式: |
D.丙烷分子的空间填充模型: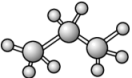 |
您最近一年使用:0次
6 . 下列说法错误的是
A.反应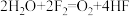 ,同时有极性键和非极性键的断裂和形成 ,同时有极性键和非极性键的断裂和形成 |
| B.Na2S和MgCl2中的化学键类型完全相同,都属于离子化合物 |
| C.CO2和HCl两种分子中,每个原子的最外层都满足8电子稳定结构 |
D.用电子式表示 的形成过程为 的形成过程为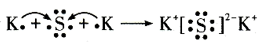 |
您最近一年使用:0次
解题方法
7 . 已知X、Y、Z、W、M、P为原子序数依次增大的六种短周期主族元素,X与M同主族,W与P同主族,W与P的原子序数之和等于X与M的原子序数之和的2倍,YX4是一种气体清洁能源,Z2、W2是组成空气的主要物质。六种元素组成的某脲醛树脂结构如图所示:

下列说法正确的是

下列说法正确的是
| A.W与X、Y、Z、M、P均可形成至少两种二元共价化合物 |
| B.脲醛树脂结构中所有元素原子最外层均满足8电子稳定结构 |
| C.简单氢化物的沸点:Z<W |
| D.由X、Z、W形成的化合物中只存在共价键 |
您最近一年使用:0次
8 . 设NA代表阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,2.24LCO2与足量的Na2O2反应,转移电子总数为0.2NA |
| B.1mol·L-1的AlCl3溶液中含有Cl-的个数为3NA |
| C.1LpH=13的Ba(OH)2溶液中Ba2+数目为0.1NA |
D.0.1mol环氧乙烷( )中含有共价键的总数约为0.7×6.02×1023 )中含有共价键的总数约为0.7×6.02×1023 |
您最近一年使用:0次
名校
解题方法
9 . 若不断地升高温度,实现"雪花→水→水蒸气→氧气和氢气"的变化。在变化的各阶段被破坏的粒子间主要的相互作用依次是
| A.氢键;分子间作用力;非极性键 | B.氢键;氢键;极性键 |
| C.氢键;极性键;分子间作用力 | D.分子间作用力;氢键;非极性键 |
您最近一年使用:0次
2022-09-15更新
|
840次组卷
|
25卷引用:湖南省益阳市箴言中学2021-2022学年高二下学期入学考试化学检测题
湖南省益阳市箴言中学2021-2022学年高二下学期入学考试化学检测题2015-2016学年河南省三门峡市灵宝一中高二下第一次月考化学试卷2020届高三化学二轮物质结构题型专攻——分子的性质【选择基础专练】(已下线)上海市建平中学2013届高三第一次模拟化学试题安徽省安庆市太湖县太湖中学2019-2020学年高二下学期3月线上考试化学试题甘肃省武威市第十八中学2019-2020学年高二下学期期末考试化学试题四川省乐山沫若中学2020-2021学年高二上学期第一次月考化学试题江苏省东台创新高级中学2019-2020学年高二下学期4月份月检测化学试题宁夏海原第一中学2021届高三上学期第二次月考化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第三节 分子结构与物质的性质 课时2 分子间的作用力(已下线)2.4 分子间作用力-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2) 湖北省黄冈市麻城市实验高级中学2020-2021学年高二3月月考化学试题山东省滕州市第一中学2020-2021学年高二下学期3月份阶段检测化学试题(已下线)考点34 分子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)重庆市万州第二高级中学2021-2022学年高二下学期期中考试化学试题河南省驻马店市环际大联考2021-2022学年高二下学期期中考试化学试题(已下线)考点47 分子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题14 分子结构与性质-2023年高考化学一轮复习小题多维练(全国通用)第二章分子结构与性质(基础卷)四川省南充市嘉陵第一中学2021-2022学年高二上学期第二次月考化学试题宁夏吴忠市吴忠中学2022-2023学年高三上学期阶段性测试 化学试题2.4分子间作用力(课前)-鲁科版选择性必修2新疆阿克苏市实验中学2022-2023学年高二下学期第二次月考化学试题四川省成都高新实验中学2023-2024学年高二下学期3月月考化学试卷四川省富顺一中2023-2024学年高二下学期第一次月考化学试题
名校
10 . I.下面是同学们熟悉的微粒,完成下列问题:
①N2H4②HBrO ③BaCl2④Ne ⑤NH4Cl ⑥Na2O2⑦N2
(1)这些物质中,只含有离子键的是____ ;(填序号,下同);属于共价化合物的是____ ;属于电解质的是____ 。
(2)①的结构式是____ ;用电子式表示NH3的形成____ 。
(3)在下列变化中,①液溴的挥发②烧碱熔化③H2S溶于水④Na2O2溶于水,破坏了化学键的是____ 。
II..表中的实线表示元素周期表的部分边界。____ 。
(5)某主族元素原子的核外电子排布为: ,该元素在元素周期表中的位置
,该元素在元素周期表中的位置____ 。
(6)元素I的非金属性____ (填“强于”或“弱于”)元素H,用原子结构的观点解释原因:同周期元素随着原子序数的递增,____ 。
(7)处于周期表中对角线位置(左上方和右下方)的元素,其性质具有相似性,称为“对角线规则”,元素D与F的单质及其化合物性质相似,如D、DO、D(OH)2与NaOH溶液都能反应生成Na2DO2等物质,写出D(OH)2与氢氧化钠溶液反应的化学方程式____ 。
(8)元素G的一种含氧酸化学式为:H3GO3,其结构式可表示为: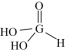 ,H3GO3分子中G原子
,H3GO3分子中G原子____ (填“是”或“不”)满足8电子稳定结构;H3GO3与过量氢氧化钠溶液反应生成的产物Na2HGO3为____ (填“酸式盐”或“正盐”)。
①N2H4②HBrO ③BaCl2④Ne ⑤NH4Cl ⑥Na2O2⑦N2
(1)这些物质中,只含有离子键的是
(2)①的结构式是
(3)在下列变化中,①液溴的挥发②烧碱熔化③H2S溶于水④Na2O2溶于水,破坏了化学键的是
II..表中的实线表示元素周期表的部分边界。
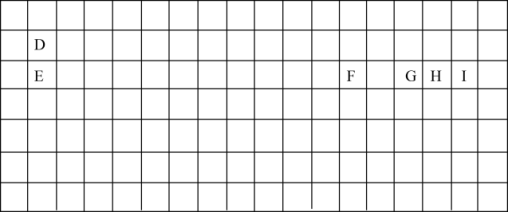
(5)某主族元素原子的核外电子排布为:
 ,该元素在元素周期表中的位置
,该元素在元素周期表中的位置(6)元素I的非金属性
(7)处于周期表中对角线位置(左上方和右下方)的元素,其性质具有相似性,称为“对角线规则”,元素D与F的单质及其化合物性质相似,如D、DO、D(OH)2与NaOH溶液都能反应生成Na2DO2等物质,写出D(OH)2与氢氧化钠溶液反应的化学方程式
(8)元素G的一种含氧酸化学式为:H3GO3,其结构式可表示为:
 ,H3GO3分子中G原子
,H3GO3分子中G原子
您最近一年使用:0次
2022-09-08更新
|
151次组卷
|
2卷引用:四川省内江市第六中学2022---2023学年高二上学期入学考试化学试题



