1 . 某有机配合物分子可对部分蛋白质进行纯化和分析,其结构如图所示,其组成元素X、Y、Z、W、Q的原子序数依次增大且分别处于3个周期,X原子无中子,Q的单质是紫红色固体。下列有关说法错误的是
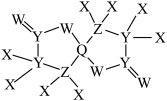
| A.该化合物可溶于水且具有还原性 | B.1mol该化合物中含有16mol的σ键 |
| C.基态原子的第一电离能:Q<Y<W<Z | D.基态原子的未成对电子数: |
您最近一年使用:0次
名校
解题方法
2 . 短周期主族元素A、B、C、D的原子序数依次增大,A、B、D分别位于不同周期,且B和D是同主族,B的最外层电子数是内层的3倍,C是同周期原子半径最大的,下列说法正确的是
| A.A与B、D均可形成18电子分子 |
| B.B、C两种元素形成的化合物中只含离子键 |
| C.B的非金属性强于D,故简单气态氢化物的沸点水高于硫化氢 |
D.离子半径大小关系: |
您最近一年使用:0次
名校
解题方法
3 . 短周期主族元素W、X、Y、Z在元素周期表中的相对位置如图所示。下列说法不正确 的是
| Y | W | |||
| X | Z |
A.简单离子半径: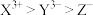 | B.简单氢化物的沸点: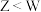 |
C.阴离子的还原性: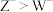 | D. 和 和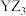 的化学键类型相同 的化学键类型相同 |
您最近一年使用:0次
4 . 下列说法正确的是
| A.在K能层中,有自旋相反的两条轨道 |
| B.最外层电子排布式为ns²的基态原子所对应元素一定位于第IIA族 |
| C.金属原子和非金属原子也能形成共价键 |
| D.焰色试验的原理是电子由基态跃迁到较高能量的激发态时,以光的形式释放能量 |
您最近一年使用:0次
名校
解题方法
5 . 学习了元素周期律可以把元素化合物知识系统地归纳起来,可以从物质的类别和元素的化合价两个方面在二维空间构造知识体系。例如:如图为S元素的价类二维图。回答下列问题:___________ ;图中所给出的物质属于含有共价键的离子化合物的是___________ (填化学式)。
(2)为验证 的相关性质,将
的相关性质,将 通入
通入 溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。
溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。
(3)Y与氢氧化钠溶液反应的离子方程式为___________ 。
(4) 中各元素原子半径由大到小的顺序为
中各元素原子半径由大到小的顺序为___________ 。
(5)木炭与浓硫酸反应的化学方程式为___________ ,验证该反应的气体产物所需溶液依次为___________ 。
A.品红溶液、酸性高锰酸钾、澄清石灰水
B.澄清石灰水、澄清石灰水、品红溶液
C.澄清石灰水、氢氧化钠溶液、品红溶液

(2)为验证
 的相关性质,将
的相关性质,将 通入
通入 溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。
溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。| 滴加的溶液 | 氯水 | 氨水 |  溶液 溶液 |
| 沉淀的化学式 |
(3)Y与氢氧化钠溶液反应的离子方程式为
(4)
 中各元素原子半径由大到小的顺序为
中各元素原子半径由大到小的顺序为(5)木炭与浓硫酸反应的化学方程式为
A.品红溶液、酸性高锰酸钾、澄清石灰水
B.澄清石灰水、澄清石灰水、品红溶液
C.澄清石灰水、氢氧化钠溶液、品红溶液
您最近一年使用:0次
解题方法
6 . 化学在日常防疫中发挥了重要作用,各类杀菌消毒剂逐渐被人们认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液;②3%H2O2溶液;③漂白粉;④ClO2;⑤O3;⑥碘酒;⑦75%酒精;⑧高铁酸钠(Na2FeO4)。按要求回答下列问题。
(1)上述杀菌消毒剂属于电解质的是___________ ,属于非电解质的是__________ 。(填序号)。
(2)“84”消毒液可由Cl2和NaOH溶液反应制得,若与“洁厕灵”(盐酸是成分之一)混合使用会产生黄绿色有毒气体,原因是_________ (用离子方程式表示)。
(3)H2O2是一种绿色环保型消毒剂,其结构式为__________ ,含有化学键的类型为__________ 。
(4)O3是一种强氧化剂,具有强大的杀菌能力。O3与O2的关系是互为__________ 。
(5)高铁酸钠(Na2FeO4)是一种多功能新型净水剂。工业上可在NaOH溶液中,用NaClO氧化Fe(OH)3的方法制备Na2FeO4,其离子方程式为__________ ,Na2FeO4在水中可以发生反应: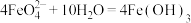 (胶体)
(胶体)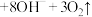 ,当反应转移的电子数为
,当反应转移的电子数为 时,生成标准状态下O2的体积约为
时,生成标准状态下O2的体积约为__________ 。
(1)上述杀菌消毒剂属于电解质的是
(2)“84”消毒液可由Cl2和NaOH溶液反应制得,若与“洁厕灵”(盐酸是成分之一)混合使用会产生黄绿色有毒气体,原因是
(3)H2O2是一种绿色环保型消毒剂,其结构式为
(4)O3是一种强氧化剂,具有强大的杀菌能力。O3与O2的关系是互为
(5)高铁酸钠(Na2FeO4)是一种多功能新型净水剂。工业上可在NaOH溶液中,用NaClO氧化Fe(OH)3的方法制备Na2FeO4,其离子方程式为
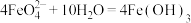 (胶体)
(胶体)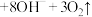 ,当反应转移的电子数为
,当反应转移的电子数为 时,生成标准状态下O2的体积约为
时,生成标准状态下O2的体积约为
您最近一年使用:0次
7 . 下列物质中含有非极性键的是
| A.Cl2 | B.KCl | C.CCl4 | D.NaOH |
您最近一年使用:0次
解题方法
8 . 下表是元素周期表的一部分。①~⑦分别对应七种元素,回答下列问题:___________ 。
(2)③和④两种元素的非金属性强弱关系:③___________ (填“>”或“<”)④。
(3)⑤和⑦两种元素组成的化合物中含有的化学键是___________ (填“共价”或“离子”)键。
(4)Cu与③的最高价氧化物对应的水化物的稀溶液反应的化学方程式为___________ 。

(2)③和④两种元素的非金属性强弱关系:③
(3)⑤和⑦两种元素组成的化合物中含有的化学键是
(4)Cu与③的最高价氧化物对应的水化物的稀溶液反应的化学方程式为
您最近一年使用:0次
名校
9 . 下列物质中含有非极性共价键的是
A. | B. | C.Ar | D. |
您最近一年使用:0次
名校
10 . 氮化钠(Na3N)是用科学方法制备的一种重要化合物,它与水作用产生NH3。请回答下列问题:
(1)Na3N的电子式是____________ ,该化合物由______ 键形成。
(2)Na3N与盐酸反应生成________ 种盐,其电子式分别为______________ 。
(1)Na3N的电子式是
(2)Na3N与盐酸反应生成
您最近一年使用:0次



