1 . 基态铬原子核外有___________ 种不同运动状态的电子,其价电子的轨道表示式为___________ 。
您最近一年使用:0次
2 . 聚氮化硫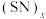 是重要的超导材料,目前已成为全球材料行业研究的热点。
是重要的超导材料,目前已成为全球材料行业研究的热点。
(1)基态S原子的原子核外能量最高的电子电子云轮廓图为___________ 形。
(2)下列电子排布图能表示氮原子的最低能量状态的是___________。
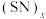 是重要的超导材料,目前已成为全球材料行业研究的热点。
是重要的超导材料,目前已成为全球材料行业研究的热点。(1)基态S原子的原子核外能量最高的电子电子云轮廓图为
(2)下列电子排布图能表示氮原子的最低能量状态的是___________。
A. | B.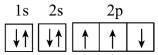 |
C.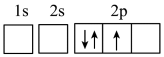 | D. |
您最近一年使用:0次
2024-04-23更新
|
80次组卷
|
2卷引用:上海市华东师范大学第三附属中学2023-2024学年高二下学期期中考试 化学试题(等级考)
3 . 硅原子核外电子运动状态为___________ 种;基态Si原子,若其电子排布式表示为 违背了
违背了___________ 。
 违背了
违背了
您最近一年使用:0次
2024-04-23更新
|
60次组卷
|
2卷引用:上海市华东师范大学第三附属中学2023-2024学年高二下学期期中考试 化学试题(等级考)
4 . 下列关于电子云或原子轨道的叙述中,正确的是
| A.电子云图中的小黑点越密,表示原子核外单位体积内的电子越多 |
| B.原子轨道是电子运动的轨迹 |
| C.原子轨道表示电子在空间各处出现的概率 |
| D.电子云用小黑点的疏密程度来表示电子在原子核外单位体积内出现概率的大小 |
您最近一年使用:0次
2024-04-22更新
|
91次组卷
|
3卷引用:上海交通大学附属中学2023-2024学年高二下学期期中考试化学试题
名校
解题方法
5 . 下列说法正确的是
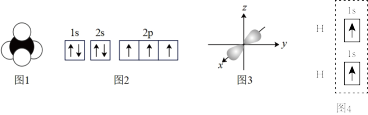

A.图1为 分子的球棍模型 分子的球棍模型 |
| B.图2为氮原子的电子轨道表示式 |
| C.图3为铍原子最外层的电子云图 |
| D.图4为用轨道表示式表示氢气分子中的共用电子对 |
您最近一年使用:0次
2022-05-07更新
|
260次组卷
|
3卷引用:上海交通大学附属中学2021-2022学年高三下学期期中考试化学试题
6 . 铅的合金可作轴承、电缆外皮之用,还可做体育器材铅球等。
(1)铅元素位于元素周期表第六周期IVA族,该族中原子序数最小的元素的原子有_______ 种 能量不同的电子,其次外层的电子云有_______ 种不同的伸展方向。
(2)与铅同主族的短周期元素中,其最高价氧化物对应水化物酸性最强的是_______ (填化学式),气态氢化物沸点最低的是_______ (填电子式)。
(3)配平下列化学方程式,把系数以及相关物质填写在空格上,并标出电子转移的方向和数目______ 。
_______PbO2+_______MnSO4+______HNO3→_______HMnO4+______Pb(NO3)2+_______PbSO4↓+_______
(4)把上述反应后的溶液稀释到1L,测出其中的Pb2+的浓度为0.6mol·L-1,则反应中转移的电子数为_______ 个,该反应中被氧化的元素是_______ 。 若将该反应设计成一原电池,则_______ 极 (填电极名称)附近溶液出现紫红色。
(5)根据上述反应,判断二氧化铅与浓盐酸反应的化学方程式正确的是_______。
(6)已知如下热化学方程式:
Ca(s)+Cl2(g)→CaCl2(s)+ 795kJ
Sr(s)+Cl2(g)→SrCl2(s) + 828kJ
Ba(s)+ Cl2(g) → BaCl2(s) + 860kJ
则①CaCl2、②SrCl2、③BaCl2三种氯化物的稳定性由大到小的排列为_______ (填序号)。从能量的角度解释理由是_______ 。
(1)铅元素位于元素周期表第六周期IVA族,该族中原子序数最小的元素的原子有
(2)与铅同主族的短周期元素中,其最高价氧化物对应水化物酸性最强的是
(3)配平下列化学方程式,把系数以及相关物质填写在空格上,并标出电子转移的方向和数目
_______PbO2+_______MnSO4+______HNO3→_______HMnO4+______Pb(NO3)2+_______PbSO4↓+_______
(4)把上述反应后的溶液稀释到1L,测出其中的Pb2+的浓度为0.6mol·L-1,则反应中转移的电子数为
(5)根据上述反应,判断二氧化铅与浓盐酸反应的化学方程式正确的是_______。
| A.PbO2+4HCl →PbCl4+2H2O | B.PbO2+4HCl →PbCl2+ Cl2↑+2H2O |
| C.PbO2+2HCl+2H+→PbCl2+2H2O | D.PbO2+4HCl→PbCl2+2OH- |
Ca(s)+Cl2(g)→CaCl2(s)+ 795kJ
Sr(s)+Cl2(g)→SrCl2(s) + 828kJ
Ba(s)+ Cl2(g) → BaCl2(s) + 860kJ
则①CaCl2、②SrCl2、③BaCl2三种氯化物的稳定性由大到小的排列为
您最近一年使用:0次
名校
解题方法
7 . 硼及其化合物在工业中有很多用处。一些硼的卤化物的沸点如图所示:
(1)硼原子的核外共有____ 种形状不同的电子云;溴原子的最外层电子排布式为____ 。
(2)表中三种卤化物分子的空间构型均为平面正三角形,由此推断F—B—F的键角为____ ,BF3属于____ 分子(填“极性”或“非极性”)。
(3)解释表中三种卤化硼沸点存在差异的原因____ 。
CS2是一种重要的化工原料。
(4)工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g) CS2(g)+2H2S(g),CS2的结构式为
CS2(g)+2H2S(g),CS2的结构式为____ ,利用燃煤废气(含N2、O2、SO2、CO2、H2O、NOx等)使尾气中的H2S转化为单质硫,可实现废物利用,保护环境,写出其中一个反应的化学方程式____ 。
| 卤化物 | BF3 | BCl3 | BBr3 |
| 沸点/℃ | -100.3 | 12.5 | 90 |
(2)表中三种卤化物分子的空间构型均为平面正三角形,由此推断F—B—F的键角为
(3)解释表中三种卤化硼沸点存在差异的原因
CS2是一种重要的化工原料。
(4)工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g)
 CS2(g)+2H2S(g),CS2的结构式为
CS2(g)+2H2S(g),CS2的结构式为
您最近一年使用:0次
8 . 有关氮原子核外p亚层中的电子的说法错误的是
| A.能量相同 | B.电子云形状相同 |
| C.电子云伸展方向相同 | D.自旋方向相同 |
您最近一年使用:0次
2021-12-27更新
|
368次组卷
|
4卷引用:上海外国语大学附属大境中学2019-2020学年高三上学期期中考化学试题
上海外国语大学附属大境中学2019-2020学年高三上学期期中考化学试题上海市嘉定区2022届高三一模化学试题(已下线)第37练 原子结构-2023年高考化学一轮复习小题多维练(全国通用)福建省漳平第二中学2021-2022学年高二下学期第一次月考化学试题
解题方法
9 . 下列电子层能量最低的是
| A.L | B.M | C.K | D.N |
您最近一年使用:0次
名校
解题方法
10 . 下列关于含氮微粒的表述正确的是( )
A.N2的电子式为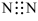 | B.N3-的最外层电子数为6 |
| C.N3-的质子数是20 | D.氮原子未成对电子的电子云形状相同 |
您最近一年使用:0次
2020-05-11更新
|
436次组卷
|
7卷引用:上海交通大学附属中学2021-2022学年高一下学期期中考试化学试题



