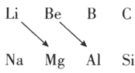
1 . (1)观察Li、Be、Mg、Al在元素周期表中的位置回答下列问题:______ (填“酸性”“碱性”或“两性”)化合物,证明这一结论的有关的离子方程式是______ 。
②根据Mg在空气中的燃烧情况可知,Li在空气中燃烧,生成的产物为______ (用化学式表示)。
(2)现有核电荷数小于20的元素A,其电离能数据如表:( 表示原子失去第n个电子的电离能,单位:
表示原子失去第n个电子的电离能,单位: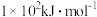 )
)
①外层电子离核越远,能量越高,电离能越______ (填“大”或“小”);阳离子所带电荷数越大,失去电子时,电离能越______ (填“大”或“小”)。
②表中11个电子分属______ 个电子层;失去了11个电子后,该元素原子还有______ 个电子。
③该元素最高价氧化物对应的水化物的化学式是______ 。
②根据Mg在空气中的燃烧情况可知,Li在空气中燃烧,生成的产物为
(2)现有核电荷数小于20的元素A,其电离能数据如表:(
 表示原子失去第n个电子的电离能,单位:
表示原子失去第n个电子的电离能,单位: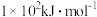 )
)| 序号 |  |  |  |  | 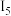 |  | 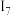 | 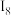 | 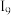 |  |  | … |
| 电离能 | 7.644 | 15.03 | 80.12 | 109.3 | 141.2 | 186.5 | 224.9 | 266.0 | 327.9 | 367.4 | 1761 | … |
②表中11个电子分属
③该元素最高价氧化物对应的水化物的化学式是
您最近一年使用:0次
名校
解题方法
2 . (1)短周期某主族元素,M的电离能情况如图A所示,则M在元素周期表的第_______ 族。

(2)如图B所示,每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ (写化学式)。a点所在折线元素氢化物的沸点变化规律如图B,呈现这种变化关系的原因是_______

(3)用氢键表示式写出氨水中NH3分子与水分子间可能存在的氢键_______ 。
(4)表中列出了含氧酸酸性强弱与非羟基氧原子数的关系。
亚磷酸 (H3PO3) 也是中强酸,它的结构式为_______ ;亚磷酸 (H3PO3)为_______ 元酸。

(2)如图B所示,每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(3)用氢键表示式写出氨水中NH3分子与水分子间可能存在的氢键
(4)表中列出了含氧酸酸性强弱与非羟基氧原子数的关系。
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 |  |  |  |  |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
您最近一年使用:0次
2021-04-07更新
|
157次组卷
|
2卷引用:山西省太原市第五中学2020-2021学年高二下学期4月阶段性检测化学试题
3 . VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
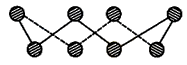
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是______ ;_______________ ;
(3)Se原子序数为_______ ,其核外M层电子的排布式为___________________ ;
(4)H2Se的酸性比H2S_________ (填“强”或“弱”)。气态SeO3分子的立体构型为______________ ,SO32-离子的立体构型为___________________ ;
(5)H2SeO3的K1和K2分别为2.7x l0-3和2.5x l0-8,H2SeO4第一步几乎完全电离,K2为1.2X10-2,请根据结构与性质的关系解释:
①H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:_____________________________________ ;
② H2SeO4比 H2SeO3酸性强的原因:______________________________________________________________
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是
(3)Se原子序数为
(4)H2Se的酸性比H2S
(5)H2SeO3的K1和K2分别为2.7x l0-3和2.5x l0-8,H2SeO4第一步几乎完全电离,K2为1.2X10-2,请根据结构与性质的关系解释:
①H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:
② H2SeO4比 H2SeO3酸性强的原因:
您最近一年使用:0次
2016-12-09更新
|
587次组卷
|
3卷引用:山西省晋中市新一双语学校2020-2021学年高二下学期3月月考化学试题



