1 . 天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种氧化镍NiO晶体中就存在如下图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但此化合物中Ni和O的比值却发生了变化。某氧化镍样品组成中个数比Ni∶O=97∶100
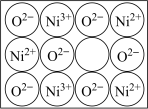
(1)写出该氧化镍样品的化学式_________________ 。
(2)试计算晶体中Ni2+与Ni3+的离子个数之比__________________ 。

(1)写出该氧化镍样品的化学式
(2)试计算晶体中Ni2+与Ni3+的离子个数之比
您最近一年使用:0次
名校
2 . 铁和钴是重要的过渡元素。
(1)钴位于元素周期表中第___ 族,基态钴原子中未成对电子的个数为_____ 。
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中中心离子Fe3+的核外价电子排布式为___ ;尿素分子中氮原子的杂化方式是___ ,尿素中所含非金属元素的电负性由大到小的顺序是___ 。
(3)Co(NH3)5BrSO4可形成两种结构的钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:
在第一种配合物溶液中加硝酸银溶液产生白色沉淀。
在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀,则第二种配合物的配体为_____ 。
(4)离子化合物CaC2的一种晶体结构如图1所示,从钙离子看,属于____ 堆积,其配位数是_____ ;一个晶胞中平均含有的π键的个数为_____ 。

图1
(5)科学研究结果表明。碳的氧化物CO2能够与H2O借助于太阳能制备HCOOH,其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中σ键和π键的个数比是____ 。
(6)奥氏体是碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为______ ,若晶体密度为ρg/cm3,则晶胞中最近的两个碳原子的距离为_____ pm(阿伏伽德罗常数的值用NA表示,写出计算式即可)。

图2
(1)钴位于元素周期表中第
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中中心离子Fe3+的核外价电子排布式为
(3)Co(NH3)5BrSO4可形成两种结构的钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:
在第一种配合物溶液中加硝酸银溶液产生白色沉淀。
在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀,则第二种配合物的配体为
(4)离子化合物CaC2的一种晶体结构如图1所示,从钙离子看,属于

图1
(5)科学研究结果表明。碳的氧化物CO2能够与H2O借助于太阳能制备HCOOH,其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中σ键和π键的个数比是
(6)奥氏体是碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为

图2
您最近一年使用:0次
2019-05-07更新
|
755次组卷
|
4卷引用:沪科版化学拓展性课程1《原子结构与元素周期律》测试题
12-13高二·全国·课时练习
名校
3 . 金晶体的最小重复单元(也称晶胞)是面心立方体,即在立方体的8个顶点各有一个金原子,各个面的中心有一个金原子,每个金原子被相邻的晶胞共用。金原子的直径为dcm,用NA表示阿伏伽德罗常数,M表示金的摩尔质量(单位:g·mol-1)。
(1)金晶体每个晶胞中含有________ 个金原子。
(2)欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定_________ 。
(3)一个晶胞的体积为________ cm3。
(4)金晶体的密度为________ g·cm-3。
(1)金晶体每个晶胞中含有
(2)欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定
(3)一个晶胞的体积为
(4)金晶体的密度为
您最近一年使用:0次
2019-02-19更新
|
219次组卷
|
10卷引用:高中化学人教版 选修三 第3章 晶体结构与性质 金属晶体的原子堆积模型
高中化学人教版 选修三 第3章 晶体结构与性质 金属晶体的原子堆积模型(已下线)2012年苏教版高中化学选修3 3.1金属键 金属晶体练习卷(已下线)2014年高二鲁科版选修3化学规范训练 3.1认识晶体练习卷(已下线)同步君 选修3 第三章 第三节 金属晶体的原子堆积模型河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:3.3 金属晶体云南省香格里拉县一中2018-2019学年高二上学期期中考试化学试题云南省普洱市景东县第一中学2018-2019学年高二上学期期末考试化学试题鲁科版高二化学物质结构与性质单元练习卷:第3章 物态的聚集状态与物质性质沪科版高中化学拓展课程第2章《化学键与晶体结构》检测题云南省红河县一中2020-2021学年高二下学期6月份考试化学试题
2016高二·全国·课时练习
名校
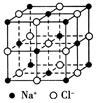
4 . 食盐晶体是由钠离子和氯离子组成的,且均为等距离的交错排列,如图所示。已知食盐的密度是2.2 g/cm3,阿伏伽德罗常数为6.02×1023/mol。在食盐晶体中两个距离最近的钠离子间的距离最接近于 厘米(保留整数)。

您最近一年使用:0次
2017-11-27更新
|
238次组卷
|
3卷引用:高中化学人教版 选修三 第3章 晶体结构与性质 晶胞



