名校
解题方法
1 . 下图是某同学设计的木炭和浓硫酸反应并检验所得产物的实验装置。
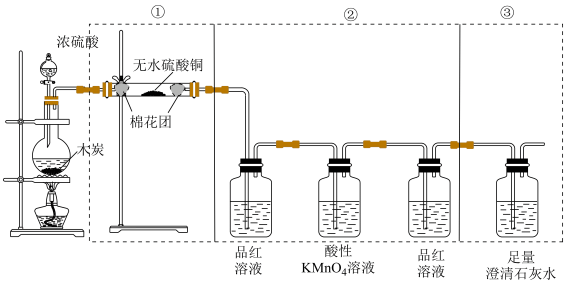
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:___________ 。
(2)②中酸性 溶液的作用是
溶液的作用是___________ ,第二瓶品红溶液的作用是___________ 。
(3)如果将装置中①、②、③三部分仪器的连接顺序变为②、①、③,则可以检出的物质是______ ;不能检出的物质是________ 。
(4)如果将仪器的连接顺序变为①、③、②,则可以检出的物质是___________ ;不能检出的物质是___________ 。
(5)有同学希望通过测量③中装置质量的增加来计算反应的木炭的质量,则在②③之间插入一个洗气瓶,其中装___________ (填写试剂名称)。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:
(2)②中酸性
 溶液的作用是
溶液的作用是(3)如果将装置中①、②、③三部分仪器的连接顺序变为②、①、③,则可以检出的物质是
(4)如果将仪器的连接顺序变为①、③、②,则可以检出的物质是
(5)有同学希望通过测量③中装置质量的增加来计算反应的木炭的质量,则在②③之间插入一个洗气瓶,其中装
您最近一年使用:0次
解题方法
2 . 一种活性氧食器消毒剂的主要成分是过碳酸钠(xNa2CO3·yH2O2)。过碳酸钠具有Na2CO3和H2O2的双重性质,50℃开始分解。某实验小组同学对过碳酸钠的制备、组成与性质进行了探究。
(一)过碳酸钠的制备
实验室用Na2CO3与稳定剂的混合溶液5%的H2O2化合制备过碳酸钠,实验装置如图:
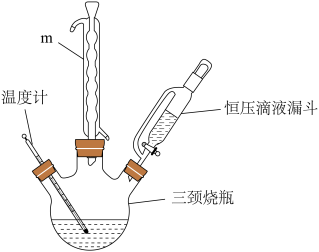
(1)仪器m的名称为___ 。
(2)恒压滴液漏斗盛装的药品是___ 。
(3)下列可用作稳定剂的是__ 。(填选项字母)。
A.FeCl3 B.CH3COOH C.Na3PO4 D.MnO2
(4)为更好的控制反应温度,采用的合适加热方式是___ 。
(二)过碳酸钠(xNa2CO3·yH2O2)组成的测定
(5)采用加热法可测定过碳酸钠(xNa2CO3·yH2O2)的组成。称取ag过碳酸钠固体样品,加热至恒重后,冷却,称量固体质量为bg。通过上述数据计算:y=__ 用含a、b、x的代数式表示)。
(三)过碳酸钠的性质
活性氧食器消毒剂可用于清洗杯温,使用说明如图所示:

(6)使用时,需要使用80°C以上热水的原因为___ 。
(7)使用时会迅速产生大量气泡,实验室检验该气体的方法为___ 。
(一)过碳酸钠的制备
实验室用Na2CO3与稳定剂的混合溶液5%的H2O2化合制备过碳酸钠,实验装置如图:

(1)仪器m的名称为
(2)恒压滴液漏斗盛装的药品是
(3)下列可用作稳定剂的是
A.FeCl3 B.CH3COOH C.Na3PO4 D.MnO2
(4)为更好的控制反应温度,采用的合适加热方式是
(二)过碳酸钠(xNa2CO3·yH2O2)组成的测定
(5)采用加热法可测定过碳酸钠(xNa2CO3·yH2O2)的组成。称取ag过碳酸钠固体样品,加热至恒重后,冷却,称量固体质量为bg。通过上述数据计算:y=
(三)过碳酸钠的性质
活性氧食器消毒剂可用于清洗杯温,使用说明如图所示:

(6)使用时,需要使用80°C以上热水的原因为
(7)使用时会迅速产生大量气泡,实验室检验该气体的方法为
您最近一年使用:0次
解题方法
3 . 无水AlCl 3 易升华,可用作有机合成的催化剂等,工业上由铝土矿(主要成分是Al 2 O 3 和Fe 2 O 3 ,还含有少量的SiO 2 )和石油焦(主要成分是C)为原料制备无水AlCl 3 :2Al 2 O 3 +6Cl 2 ===4AlCl 3 +3O 2
回答以下问题:
(1)Cl-的电子式为________ 。Al在元素周期表最中的位置是________ 。
(2)生产中加入石油焦,其目的是_____________________________________ 。
(3)加入焦炭后的化学反应可表示为Al2O3 +C+Cl2 AlCl3 +X↑,设计实验确定气体X的成分:
AlCl3 +X↑,设计实验确定气体X的成分: ____________________________________ 。
(4)在提纯AlCl3 粗产品时,需加入少量铝粉,可使熔点较低的FeCl3 转化为熔点较高的FeCl2 ,从而避免在AlCl3 中混入铁的氯化物。该反应的化学方程式为___________________________________ 。
(5)为测定制得的无水AlCl3 产品(含FeCl3 杂质)的纯度,称取16.25 g无水AlCl3 样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
①过程涉及的离子方程式__________________________ 、___________ 。
②AlCl3 产品的纯度为__________________________________ 。
(6)以铝土矿为原料可以通过以下途径提纯氧化铝

①写出滤液甲中溶质的化学式______________________________ 。
②写出滤液乙中加入过量氨水得到Al(OH)3 的离子方程式__________________ 。
回答以下问题:
(1)Cl-的电子式为
(2)生产中加入石油焦,其目的是
(3)加入焦炭后的化学反应可表示为Al2O3 +C+Cl2
 AlCl3 +X↑,设计实验确定气体X的成分:
AlCl3 +X↑,设计实验确定气体X的成分: (4)在提纯AlCl3 粗产品时,需加入少量铝粉,可使熔点较低的FeCl3 转化为熔点较高的FeCl2 ,从而避免在AlCl3 中混入铁的氯化物。该反应的化学方程式为
(5)为测定制得的无水AlCl3 产品(含FeCl3 杂质)的纯度,称取16.25 g无水AlCl3 样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
①过程涉及的离子方程式
②AlCl3 产品的纯度为
(6)以铝土矿为原料可以通过以下途径提纯氧化铝

①写出滤液甲中溶质的化学式
②写出滤液乙中加入过量氨水得到Al(OH)3 的离子方程式
您最近一年使用:0次



