名校
解题方法
1 . 过氧化钠(Na2O2)常用作漂白剂、杀菌剂、供氧剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验。
(1)探究 Na2O2样品是否已经变质:Na2O2在空气中久置易变质生成_______ ,现取少量样品加水溶解,加入_______ 溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该实验小组为了粗略测定这包Na2O2样品的质量分数,称取了m g样品,并设计如图所示装置来测定过氧化钠的质量分数。
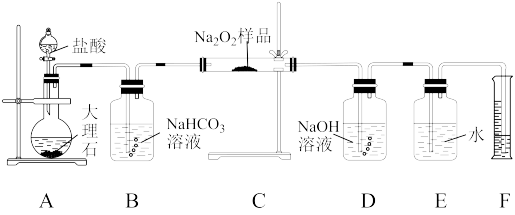
已知:饱和NaHCO3溶液的作用是除去CO2中的HCl气体,E和F是排水集气装置。
①写出装置C中发生的主要反应的化学方程式:_______ 。
②装置D的作用是_______ 。
③反应结束,待冷却后读出量筒内水的体积,将其折算成O2的质量为n g,则样品中过氧化钠的质量分数为_______ ×100%(用含m、n的最简式表示)。
(1)探究 Na2O2样品是否已经变质:Na2O2在空气中久置易变质生成
(2)该实验小组为了粗略测定这包Na2O2样品的质量分数,称取了m g样品,并设计如图所示装置来测定过氧化钠的质量分数。

已知:饱和NaHCO3溶液的作用是除去CO2中的HCl气体,E和F是排水集气装置。
①写出装置C中发生的主要反应的化学方程式:
②装置D的作用是
③反应结束,待冷却后读出量筒内水的体积,将其折算成O2的质量为n g,则样品中过氧化钠的质量分数为
您最近半年使用:0次
2 . 绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
I.测定绿矾中结晶水含量
为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按如图连接好装置进行实验。
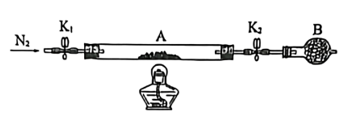
(1)将下列实验操作步骤正确排序________→________→________→________→c→e(填字母)______ ;重复上述操作步骤,直至A恒重,记为m3g。
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量A
f.冷却到室温
(2)根据实验记录,计算绿矾化学式中结晶水数目x=______ (列式表示)。
II.探究绿矾的热分解产物
该小组用如图所示装置进行实验(夹持仪器略)。
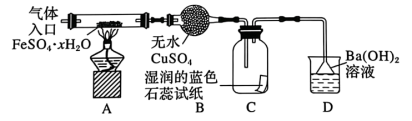
(3)在实验过程中,观察到A中固体变红棕色,B中的现象:______ ;C中试纸的颜色变化是_____ 。
(4)D中有白色沉淀生成,该沉淀的化学式为______ 。有同学认为还应该增加一个实验,取D中沉淀,加入一定量的盐酸以确定其组成,从而确定FeSO4·xH2O的分解产物,你认为是否必要?______ (填“是”或者“否”)请说明你的理由:______ 。
III.测定绿矾热分解时的温度与剩余固体质量关系
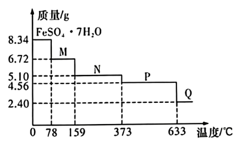
(5)将8.34gFeSO4∙7H2O样品隔绝空气加热脱水,其热重曲线(样品质量随温度变化的曲线)如图所示。已知M(FeSO4∙7H2O)=278g∙mol-1,在100℃时,M的化学式为______ 。
I.测定绿矾中结晶水含量
为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按如图连接好装置进行实验。

(1)将下列实验操作步骤正确排序________→________→________→________→c→e(填字母)
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量A
f.冷却到室温
(2)根据实验记录,计算绿矾化学式中结晶水数目x=
II.探究绿矾的热分解产物
该小组用如图所示装置进行实验(夹持仪器略)。

(3)在实验过程中,观察到A中固体变红棕色,B中的现象:
(4)D中有白色沉淀生成,该沉淀的化学式为
III.测定绿矾热分解时的温度与剩余固体质量关系
(5)将8.34gFeSO4∙7H2O样品隔绝空气加热脱水,其热重曲线(样品质量随温度变化的曲线)如图所示。已知M(FeSO4∙7H2O)=278g∙mol-1,在100℃时,M的化学式为

您最近半年使用:0次
3 . 钾是人体必需的元素之一,若血液中钾元素含量偏低,易引发低钾血症,严重时会引发心率失常,甚至猝死。医学专家提醒:应重视日常补钾。可以服用的某种钾的化合物,其水溶液可以和硝酸银溶液反应,生成不溶于稀硝酸的白色沉淀。此化合物是
| A.KCl | B.K2CO3 | C.KNO3 | D.KOH |
您最近半年使用:0次
18-19高三·浙江·阶段练习
4 . 阿司匹林铜具有很强的抗炎作用。它是一种亮蓝色结晶粉末,不溶于水、醇、醚及氯仿等溶剂中。易受热分解成浅绿色混合物。在强酸条件下能解离出铜离子。合成阿司匹林铜,其实验流程如下:
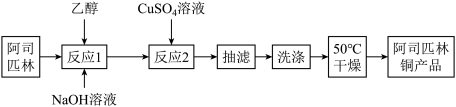
已知反应方程式如下:
 +NaOH→
+NaOH→ +H2O
+H2O
 +CuSO4→
+CuSO4→ +Na2SO4
+Na2SO4
(1)下列有关说法正确的是_____ 。
A.反应1中加乙醇作溶剂,目的是增大接触面积,加快反应速率
B.用倾析法将反应2中的液体和沉淀同时转移到布氏漏斗中进行抽滤
C.洗涤操作中,可先用水洗2-3次,再用酒精洗涤2-3次
D.干燥后发现固体呈浅绿色,可能是烘干温度过高造成的结果
(2)反应1中的反应温度要求控制在室温的理由是______ 。
(3)阿司匹林铜中铜含量的测定,可用碘量法测定:
步骤一:准确称取0.800g样品,置于250mL锥形瓶中,加4mL3.00mol/L,再加20mL水,加热煮沸,样品完全分解后,摇匀,冷却到室温。
步骤二:往溶液中加入1.200gKI摇匀,用0.100mol/LNa2S2O3标准溶液滴定至溶液变浅黄色时,加入10mL 10% KSCN试剂,并加几滴淀粉溶液,继续用0.100mol/LNa2S2O3标准溶液滴定至终点,共消耗溶液体积为23.00mL。
已知:CuI难溶于水,能吸附碘;I2+2S2O32-=S4O62-+2I-。
CuI(s)+SCN-(aq) CuSCN(s)+I-(aq)
CuSCN(s)+I-(aq)
①实验中加入10mL 10%KSCN试剂的目的是______ 。
②上述测定实验中,继续滴加Na2S2O3标准溶液至终点的具体实验操作______ 。
③该样品中的铜含量为______ 。

已知反应方程式如下:
 +NaOH→
+NaOH→ +H2O
+H2O +CuSO4→
+CuSO4→ +Na2SO4
+Na2SO4(1)下列有关说法正确的是
A.反应1中加乙醇作溶剂,目的是增大接触面积,加快反应速率
B.用倾析法将反应2中的液体和沉淀同时转移到布氏漏斗中进行抽滤
C.洗涤操作中,可先用水洗2-3次,再用酒精洗涤2-3次
D.干燥后发现固体呈浅绿色,可能是烘干温度过高造成的结果
(2)反应1中的反应温度要求控制在室温的理由是
(3)阿司匹林铜中铜含量的测定,可用碘量法测定:
步骤一:准确称取0.800g样品,置于250mL锥形瓶中,加4mL3.00mol/L,再加20mL水,加热煮沸,样品完全分解后,摇匀,冷却到室温。
步骤二:往溶液中加入1.200gKI摇匀,用0.100mol/LNa2S2O3标准溶液滴定至溶液变浅黄色时,加入10mL 10% KSCN试剂,并加几滴淀粉溶液,继续用0.100mol/LNa2S2O3标准溶液滴定至终点,共消耗溶液体积为23.00mL。
已知:CuI难溶于水,能吸附碘;I2+2S2O32-=S4O62-+2I-。
CuI(s)+SCN-(aq)
 CuSCN(s)+I-(aq)
CuSCN(s)+I-(aq) ①实验中加入10mL 10%KSCN试剂的目的是
②上述测定实验中,继续滴加Na2S2O3标准溶液至终点的具体实验操作
③该样品中的铜含量为
您最近半年使用:0次
名校
5 . 明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量的氧化铁杂质,其体实验流程如下:
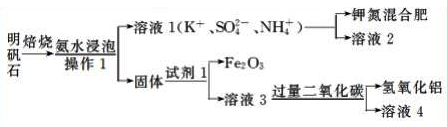
请回答下列问题:
(1)明矾石焙烧后用稀氨水浸出。需用到480mL稀氨水(每升含有39g氨), 则需取浓氨水(每升含有210g氨)_____ mL来配制(数值取整数),用规格为____ 量筒量取。操作l所用到的玻璃仪器的名称是______ 。
(2)写出上图“固体”中所有物质的化学式_____ 。
(3)由溶液3制取氢氧化铝的离子方程式为_______ 。
(4)请你写出验证溶液l中有K+的实验操作:________ 。
(5)为测定混合肥料K2S04、(NH4)2SO4中钾的含量,完成下列步骤:
①称取钾氮肥试样并溶于水,加入足量____ 溶液,产生白色沉淀。
②过滤、洗涤、干燥。其中,洗涤沉淀的操作方法为________ 。
③冷却、称重。
(6)若试样为mg,沉淀的物质的量为nmol, 则试样中K2S04的物质的量为:_____ mol(用含m 、n 的代数式表示)。
(7)实验室用Fe203与CO反应来制取单质Fe。
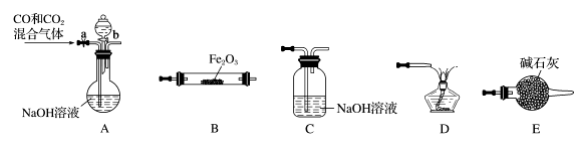
①请按气流由左到右的方向连接下列各装置,顺序为A→____ →____ →____ →_____ 。
②检查装置A气密性的方法是_____ 。
③在点燃B处的酒精灯前,应进行的操作是______ 。
④装置C的作用是_____________ 。

请回答下列问题:
(1)明矾石焙烧后用稀氨水浸出。需用到480mL稀氨水(每升含有39g氨), 则需取浓氨水(每升含有210g氨)
(2)写出上图“固体”中所有物质的化学式
(3)由溶液3制取氢氧化铝的离子方程式为
(4)请你写出验证溶液l中有K+的实验操作:
(5)为测定混合肥料K2S04、(NH4)2SO4中钾的含量,完成下列步骤:
①称取钾氮肥试样并溶于水,加入足量
②过滤、洗涤、干燥。其中,洗涤沉淀的操作方法为
③冷却、称重。
(6)若试样为mg,沉淀的物质的量为nmol, 则试样中K2S04的物质的量为:
(7)实验室用Fe203与CO反应来制取单质Fe。

①请按气流由左到右的方向连接下列各装置,顺序为A→
②检查装置A气密性的方法是
③在点燃B处的酒精灯前,应进行的操作是
④装置C的作用是
您最近半年使用:0次



