1 . 化学兴趣小组的同学在实验室发现一瓶未盖瓶盖的 固体,于是对其是否变质及
固体,于是对其是否变质及 的含量进行探究。
的含量进行探究。
【提出问题】
该 固体是否变质?若变质,则
固体是否变质?若变质,则 的质量分数是多少?
的质量分数是多少?
【查阅资料】
室温时, 易溶于水,
易溶于水, 微溶于水。
微溶于水。
【设计与实验】
实验一:定性探究。分别取等质量的未盖瓶盖试剂瓶中的 固体(下称“待测样品”)和盖好瓶盖试剂瓶中的
固体(下称“待测样品”)和盖好瓶盖试剂瓶中的 固体(下称“对比样品”)与等体积、等浓度的稀盐酸在图所示的三颈烧瓶中反应,采集数据,绘制出图2所示的图像。
固体(下称“对比样品”)与等体积、等浓度的稀盐酸在图所示的三颈烧瓶中反应,采集数据,绘制出图2所示的图像。
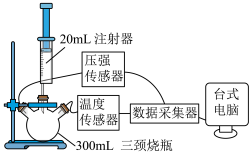
(1)据下图分析,开始时 -a段压强快速增大的原因是
-a段压强快速增大的原因是_______________ 。
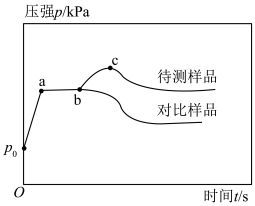
(2)据上图分析,待测样品部分变质,其中a-b段发生反应的化学方程式为___________ 。
实验二:定量探究。兴趣小组的同学设计了如下图所示装置进行定量测定。
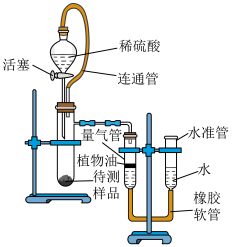
(3)检查图中装置气密性的方法是______________________ 。
(4)图装置中,量气管内水面上的一层植物油的作用是___________ 。
(5)若图装置中没有连通管,则测出待测样品中 的质量分数会
的质量分数会___________ (填“偏大”或“偏小”或“无影响”)。
实验三:实验改进。为提高定量实验的准确性,该小组设计了下图所示装置进行测定。

(6)向图装置的三颈烧瓶中加入足量稀硫酸,一段时间后反应停止。再加入 溶液,发现又产生气泡。推测加入
溶液,发现又产生气泡。推测加入 溶液的作用是
溶液的作用是___________ 。
【数据处理】
(7)实验三中,待测样品质量为m g,加入稀硫酸的体积为 mL,加入
mL,加入 溶液的体积为
溶液的体积为 mL,右侧注射器最后读数为V mL。已知实验条件下
mL,右侧注射器最后读数为V mL。已知实验条件下 气体的密度为
气体的密度为 g/mL,则待测样品中
g/mL,则待测样品中 的质量分数的表达式为
的质量分数的表达式为___________ 。
(8)与实验二相比,实验三的优点是___________ 。
 固体,于是对其是否变质及
固体,于是对其是否变质及 的含量进行探究。
的含量进行探究。【提出问题】
该
 固体是否变质?若变质,则
固体是否变质?若变质,则 的质量分数是多少?
的质量分数是多少?【查阅资料】
室温时,
 易溶于水,
易溶于水, 微溶于水。
微溶于水。【设计与实验】
实验一:定性探究。分别取等质量的未盖瓶盖试剂瓶中的
 固体(下称“待测样品”)和盖好瓶盖试剂瓶中的
固体(下称“待测样品”)和盖好瓶盖试剂瓶中的 固体(下称“对比样品”)与等体积、等浓度的稀盐酸在图所示的三颈烧瓶中反应,采集数据,绘制出图2所示的图像。
固体(下称“对比样品”)与等体积、等浓度的稀盐酸在图所示的三颈烧瓶中反应,采集数据,绘制出图2所示的图像。
(1)据下图分析,开始时
 -a段压强快速增大的原因是
-a段压强快速增大的原因是
(2)据上图分析,待测样品部分变质,其中a-b段发生反应的化学方程式为
实验二:定量探究。兴趣小组的同学设计了如下图所示装置进行定量测定。

(3)检查图中装置气密性的方法是
(4)图装置中,量气管内水面上的一层植物油的作用是
(5)若图装置中没有连通管,则测出待测样品中
 的质量分数会
的质量分数会实验三:实验改进。为提高定量实验的准确性,该小组设计了下图所示装置进行测定。

(6)向图装置的三颈烧瓶中加入足量稀硫酸,一段时间后反应停止。再加入
 溶液,发现又产生气泡。推测加入
溶液,发现又产生气泡。推测加入 溶液的作用是
溶液的作用是【数据处理】
(7)实验三中,待测样品质量为m g,加入稀硫酸的体积为
 mL,加入
mL,加入 溶液的体积为
溶液的体积为 mL,右侧注射器最后读数为V mL。已知实验条件下
mL,右侧注射器最后读数为V mL。已知实验条件下 气体的密度为
气体的密度为 g/mL,则待测样品中
g/mL,则待测样品中 的质量分数的表达式为
的质量分数的表达式为(8)与实验二相比,实验三的优点是
您最近一年使用:0次
名校
2 . 某化学实验小组为了探究氨气的性质设计了如图实验装置:
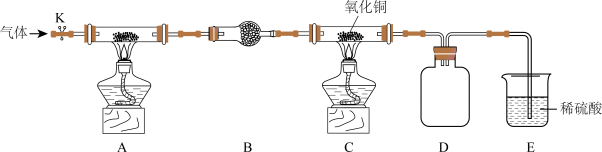
已知:CuO在高温时不稳定,会分解得到Cu2O,Cu2O粉末呈红色。
(1)实验前需先通入一段时间某气体,该气体可以是____ (填字母)。
a.空气b.氩气c.氢气
装置A用于制备氨气,选择的试剂通常是____ (填化学式)。
(2)装置D、E的作用分别是____ 、____ 。
(3)经实验测定NH3和CuO反应的产物有N2和Cu,则NH3和CuO反应的化学方程式为____ 。
(4)实验结束后装置c中黑色粉末变成红色,该红色粉末的成分能否确定?____ (填“能”或“否”)。请通过检验其他产物证明NH3和CuO发生了反应,简述实验方案:____ 。
(5)加热条件下,氨气可以与铝发生置换反应生成AlN;AlN性质稳定,加热时溶于浓碱溶液且可产生氨气。
①写出氨气与铝反应的化学方程式:____ 。
②称取AlN样品23.2g(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为14.56L(标准状况),则样品中AlN的质量分数为____ %(保留一位小数)。

已知:CuO在高温时不稳定,会分解得到Cu2O,Cu2O粉末呈红色。
(1)实验前需先通入一段时间某气体,该气体可以是
a.空气b.氩气c.氢气
装置A用于制备氨气,选择的试剂通常是
(2)装置D、E的作用分别是
(3)经实验测定NH3和CuO反应的产物有N2和Cu,则NH3和CuO反应的化学方程式为
(4)实验结束后装置c中黑色粉末变成红色,该红色粉末的成分能否确定?
(5)加热条件下,氨气可以与铝发生置换反应生成AlN;AlN性质稳定,加热时溶于浓碱溶液且可产生氨气。
①写出氨气与铝反应的化学方程式:
②称取AlN样品23.2g(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为14.56L(标准状况),则样品中AlN的质量分数为
您最近一年使用:0次
2022-07-12更新
|
404次组卷
|
3卷引用:四川省泸县第五中学2022-2023学年高一下学期6月期末考试化学试题
3 . 某化学学习小组探究浓度对硝酸氧化能力的影响。
Ⅰ.资料显示:浓硝酸能将NO氧化成 ,而稀硝酸不能氧化NO;氢氧化钠能吸收
,而稀硝酸不能氧化NO;氢氧化钠能吸收 ,但不能吸收NO。该学习小组按如图装置进行验证实验(夹持仪器已略去)。
,但不能吸收NO。该学习小组按如图装置进行验证实验(夹持仪器已略去)。
(1)装置a的名称___________ 。
(2)写出装置①中反应的离子反应方程式___________ 。
(3)写出装置②中反应的化学反应方程式___________ 。
(4)①~⑥装置中,没有发生氧化还原反应的是___________ 。(填装置序号)
(5)下列说法正确的是___________。
Ⅱ.测得铁与不同浓度硝酸反应时各还原产物的物质的量相对含量与硝酸溶液浓度的关系如图所示:___________ 。
A.硝酸的浓度越大,其还原产物中高价态的N元素成分越多
B.硝酸与铁反应往往同时生成多种还原产物
C.铁能与大于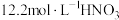 溶液反应说明不存在“钝化”现象
溶液反应说明不存在“钝化”现象
(7)已知:在上述反应条件下,反应后铁以 形式存在于溶液中。当硝酸浓度为
形式存在于溶液中。当硝酸浓度为 时,计算氧化剂与还原剂的物质的量之比为:
时,计算氧化剂与还原剂的物质的量之比为:___________ 。
Ⅰ.资料显示:浓硝酸能将NO氧化成
 ,而稀硝酸不能氧化NO;氢氧化钠能吸收
,而稀硝酸不能氧化NO;氢氧化钠能吸收 ,但不能吸收NO。该学习小组按如图装置进行验证实验(夹持仪器已略去)。
,但不能吸收NO。该学习小组按如图装置进行验证实验(夹持仪器已略去)。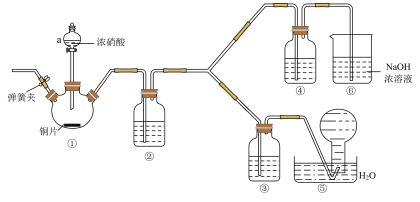
(1)装置a的名称
(2)写出装置①中反应的离子反应方程式
(3)写出装置②中反应的化学反应方程式
(4)①~⑥装置中,没有发生氧化还原反应的是
(5)下列说法正确的是___________。
| A.能证明氧化性的相对强弱的实验现象为③中溶液上方出现红棕色气体 |
| B.②中的试剂为水 |
| C.滴加浓硝酸前要先打开弹簧夹通一段时间氮气 |
| D.⑥的作用是吸收尾气NO |
Ⅱ.测得铁与不同浓度硝酸反应时各还原产物的物质的量相对含量与硝酸溶液浓度的关系如图所示:

A.硝酸的浓度越大,其还原产物中高价态的N元素成分越多
B.硝酸与铁反应往往同时生成多种还原产物
C.铁能与大于
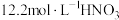 溶液反应说明不存在“钝化”现象
溶液反应说明不存在“钝化”现象(7)已知:在上述反应条件下,反应后铁以
 形式存在于溶液中。当硝酸浓度为
形式存在于溶液中。当硝酸浓度为 时,计算氧化剂与还原剂的物质的量之比为:
时,计算氧化剂与还原剂的物质的量之比为:
您最近一年使用:0次
2023-07-13更新
|
348次组卷
|
6卷引用:四川省宜宾市叙州区第二中学校2023-2024学年高二上学期开学化学试题
四川省宜宾市叙州区第二中学校2023-2024学年高二上学期开学化学试题辽宁省五校(大连二十四中、东北育才等)2022-2023学年高一下学期期末考试化学试题辽宁省沈阳市2022-2023学年高一下学期期末考试化学试题河北师范大学附属中学2023-2024学年高二上学期开学考试化学试题广东省佛山市顺德区桂洲中学2023-2024学年高一下学期第二次联考化学模拟试题2(已下线)综合突破02 期末压轴80题之非选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
解题方法
4 . 高氯酸铵(NH4ClO4)是复合火箭推进剂的重要成分,也可以做氧化剂、分析试剂等。实验室可由NaClO3等原料制取高氯酸铵(部分物质溶解度如图),其实验流程如图:
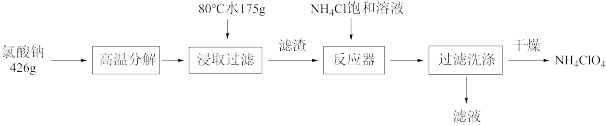
已知:氯酸钠受热分解生成高氯酸钠和氯化钠。
(1)根据如下溶解度与温度的关系图象推测,80℃时浸取液冷却至0℃过滤,滤渣的主要成分为___ (写化学式)。反应器中加入氯化铵饱和溶液,然后加热并搅拌使其充分反应,反应的化学方程式为___ 。若氯化铵用氨气和浓盐酸代替上述反应,则无需加热反应就能进行,其原因是___ 。
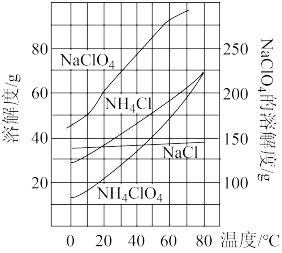
(2)反应得到的混合液中NH4ClO4和NaCl的质量分数分别为0.40和0.20。根据溶解度与温度的关系图象,从混合溶液中获得较多NH4ClO4晶体的实验操作依次为___ 、___ (均填实验操作名称)、过滤、冷水洗涤、干燥,冷水洗涤的作用是__ 。
(3)已知NH4ClO4在400℃时开始分解,某课题组设计实验探究NH4ClO4的分解产物(假设装置内的药品均足量)。甲同学设计如图实验(部分夹持装置已省略):
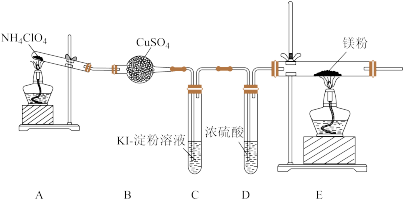
①若高氯酸铵分解有氯气生成,则可能观察到C中的现象是___ ,写出产生该现象的离子方程式___ 。
②通过查阅资料:NH4ClO4在加热分解时还产生了一种使带火星木条复燃的气体。写出高氯酸铵分解的化学方程式__ 。实验完毕后,取出E处硬质玻璃管中固体于试管中,滴加蒸馏水,产生的气体R能使湿润的红色石蕊试纸变蓝,R的电子式为___ 。

已知:氯酸钠受热分解生成高氯酸钠和氯化钠。
(1)根据如下溶解度与温度的关系图象推测,80℃时浸取液冷却至0℃过滤,滤渣的主要成分为

(2)反应得到的混合液中NH4ClO4和NaCl的质量分数分别为0.40和0.20。根据溶解度与温度的关系图象,从混合溶液中获得较多NH4ClO4晶体的实验操作依次为
(3)已知NH4ClO4在400℃时开始分解,某课题组设计实验探究NH4ClO4的分解产物(假设装置内的药品均足量)。甲同学设计如图实验(部分夹持装置已省略):

①若高氯酸铵分解有氯气生成,则可能观察到C中的现象是
②通过查阅资料:NH4ClO4在加热分解时还产生了一种使带火星木条复燃的气体。写出高氯酸铵分解的化学方程式
您最近一年使用:0次
名校
解题方法
5 . 草酸铵,化学式为(NH4)2C2O4,溶于水,水溶液显酸性,不稳定,受热可分解,溶液中的钙、镁等离子可以与草酸铵生成沉淀而除去。___ 。
(2)D装置的作用是___ 。
(3)尾气处理的方法是___ 。
(4)草酸铵分解的化学方程式为___ 。
Ⅱ.用草酸铵样品测定硬水中Ca2+和Mg2+的浓度
(5)某化学小组用0.0100mol/L的草酸铵滴定某硬水样品以测定Ca2+和Mg2+的含量。取三份25.00mL的硬水样品分别滴定,平均消耗10.60mL草酸铵溶液,则硬水中Ca2+和Mg2+的总浓度约为____ 。(保留三位有效数字)
(6)草酸铵标准液应放在_____ 滴定管中,若滴定前仰视读数,滴定后平视读数,则所测定的Ca2+和Mg2+浓度将__ (填“偏高”“偏低”或“无影响”)。
Ⅰ.某同学利用如图所示实验装置检验草酸铵的分解产物,现象为B、F中澄清石灰水变浑浊,E中固体变红。
(2)D装置的作用是
(3)尾气处理的方法是
(4)草酸铵分解的化学方程式为
Ⅱ.用草酸铵样品测定硬水中Ca2+和Mg2+的浓度
(5)某化学小组用0.0100mol/L的草酸铵滴定某硬水样品以测定Ca2+和Mg2+的含量。取三份25.00mL的硬水样品分别滴定,平均消耗10.60mL草酸铵溶液,则硬水中Ca2+和Mg2+的总浓度约为
(6)草酸铵标准液应放在
您最近一年使用:0次
2021-09-06更新
|
226次组卷
|
5卷引用:四川省遂宁市射洪中学校2021-2022学年高二下学期期中考试化学试题



