解题方法
1 . 84消毒液是一种常见的含氯消毒剂。如图为某品牌84消毒液的说明书中的部分内容。
(1)常温,将氯气通入NaOH溶液中可制得84消毒液的主要成分。写出离子方程式:_______ 。
(2)某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。
;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。
I.向2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
II.向2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
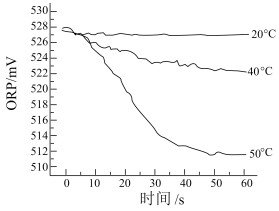
III.测得84消毒液在不同温度时ORP随时间的变化曲线如下。
①已知白醋显酸性,不具有漂白性。实验I、II现象不同的原因是_______ 。
②由实验III可得出的结论是_______ 。ORP值不同的原因可能是_______ 。
(3)针对不同物品的消毒,84消毒液需要稀释到不同的浓度来使用。取含次氯酸钠14.9g/L的84消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为_______  。
。
(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是 将
将 氧化产生的
氧化产生的 促进藻类快速生长。写出该反应的化学方程式:
促进藻类快速生长。写出该反应的化学方程式:_______ 。
| 产品特点 本品是以次氯酸钠为主要成分的液体消毒剂。可杀灭肠道致病菌、化脓性球菌、致病性酵母菌,并能灭活病毒。 注意事项 1.本品易使有色衣脱色,禁止用于丝、毛、麻织物的消毒。 2.不得将本品与酸性产品(如洁厕类清洁产品)同时使用。 3.置于避光、阴凉处保存。 4.需稀释后使用,勿口服。 |
(1)常温,将氯气通入NaOH溶液中可制得84消毒液的主要成分。写出离子方程式:
(2)某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有
 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。
;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。I.向2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
II.向2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
III.测得84消毒液在不同温度时ORP随时间的变化曲线如下。

①已知白醋显酸性,不具有漂白性。实验I、II现象不同的原因是
②由实验III可得出的结论是
(3)针对不同物品的消毒,84消毒液需要稀释到不同的浓度来使用。取含次氯酸钠14.9g/L的84消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为
 。
。(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是
 将
将 氧化产生的
氧化产生的 促进藻类快速生长。写出该反应的化学方程式:
促进藻类快速生长。写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
2 . 某学习小组探究 的性质:
的性质:
(1)【观察】描述其颜色、状态:___________ 。
(2)【预测性质】从元素化合价来看, 中氧元素显
中氧元素显___________ 价,它具有的性质是___________ (填“氧化性”“还原性”或“氧化性和还原性”)。
(3)【设计实验】探究 和
和 反应情况
反应情况
取少量 粉末于试管,加入适量蒸馏水,产生气泡,用一根带火星的木条放在试管口,观察到木条复燃。振荡试管,使固体全部溶解,不再产生气泡时,将溶液分装甲、乙两支试管。向甲试管中撒少量
粉末于试管,加入适量蒸馏水,产生气泡,用一根带火星的木条放在试管口,观察到木条复燃。振荡试管,使固体全部溶解,不再产生气泡时,将溶液分装甲、乙两支试管。向甲试管中撒少量 粉末,又产生气泡;向乙试管中滴几滴酚酞溶液,溶液变红色,立即褪色。
粉末,又产生气泡;向乙试管中滴几滴酚酞溶液,溶液变红色,立即褪色。
①一般认为, 和
和 反应过程分两步:
反应过程分两步:
第一步, ;第二步,
;第二步,___________ (补充化学方程式)。
②为了进一步证明上述反应过程真实性,取少量粉末于试管,加入蒸馏水,使固体全部溶解,不再产生气泡时滴加几滴稀硫酸酸化的淀粉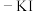 溶液,若
溶液,若___________ (填实验现象),则证明结论成立。(已知:淀粉溶液遇 变蓝色。)
变蓝色。)
(4)【归纳总结】根据 和
和 反应生成
反应生成 和
和 ,
,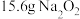 完全反应,参与反应的氧化剂质量为
完全反应,参与反应的氧化剂质量为___________ 。
(5)【问题与讨论】通过上述探究,你认为实验室保存 注意什么问题?答:
注意什么问题?答:______ 。
 的性质:
的性质:(1)【观察】描述其颜色、状态:
(2)【预测性质】从元素化合价来看,
 中氧元素显
中氧元素显(3)【设计实验】探究
 和
和 反应情况
反应情况取少量
 粉末于试管,加入适量蒸馏水,产生气泡,用一根带火星的木条放在试管口,观察到木条复燃。振荡试管,使固体全部溶解,不再产生气泡时,将溶液分装甲、乙两支试管。向甲试管中撒少量
粉末于试管,加入适量蒸馏水,产生气泡,用一根带火星的木条放在试管口,观察到木条复燃。振荡试管,使固体全部溶解,不再产生气泡时,将溶液分装甲、乙两支试管。向甲试管中撒少量 粉末,又产生气泡;向乙试管中滴几滴酚酞溶液,溶液变红色,立即褪色。
粉末,又产生气泡;向乙试管中滴几滴酚酞溶液,溶液变红色,立即褪色。①一般认为,
 和
和 反应过程分两步:
反应过程分两步:第一步,
 ;第二步,
;第二步,②为了进一步证明上述反应过程真实性,取少量粉末于试管,加入蒸馏水,使固体全部溶解,不再产生气泡时滴加几滴稀硫酸酸化的淀粉
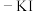 溶液,若
溶液,若 变蓝色。)
变蓝色。)(4)【归纳总结】根据
 和
和 反应生成
反应生成 和
和 ,
,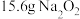 完全反应,参与反应的氧化剂质量为
完全反应,参与反应的氧化剂质量为(5)【问题与讨论】通过上述探究,你认为实验室保存
 注意什么问题?答:
注意什么问题?答:
您最近一年使用:0次
名校
3 . 实验室可用图中装置(略去部分夹持仪器)制取 并验证其性质。
并验证其性质。
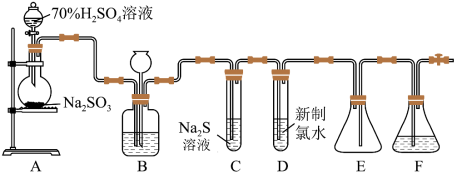
(1)装置A中发生反应的化学方程式为___________ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择___________ (填序号)。
a.蒸馏水 b.饱和 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和
溶液 d.饱和 溶液
溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为___________ 。E装置的作用为___________ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案I:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅲ:向第三份溶液中加入 溶液,有产生白色沉淀。
溶液,有产生白色沉淀。
上述方案中合理的是方案___________ (填“I”“Ⅱ”或“Ⅲ”)。
(5)工业上常用SO2做海水提溴过程中的吸收剂,海水提溴工艺流程示意图如下。
浓缩海水 含溴海水
含溴海水 HBr溶液
HBr溶液 高浓度溴水
高浓度溴水 Br2
Br2
其中SO2和H2O吸收热空气吹出的溴(g)时发生的主要化学方程式为___________ 。
 并验证其性质。
并验证其性质。
(1)装置A中发生反应的化学方程式为
(2)装置B的作用之一是通过观察产生气泡的多少判断
 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择a.蒸馏水 b.饱和
 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和
溶液 d.饱和 溶液
溶液(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案I:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案Ⅱ:向第二份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案Ⅲ:向第三份溶液中加入
 溶液,有产生白色沉淀。
溶液,有产生白色沉淀。上述方案中合理的是方案
(5)工业上常用SO2做海水提溴过程中的吸收剂,海水提溴工艺流程示意图如下。
浓缩海水
 含溴海水
含溴海水 HBr溶液
HBr溶液 高浓度溴水
高浓度溴水 Br2
Br2其中SO2和H2O吸收热空气吹出的溴(g)时发生的主要化学方程式为
您最近一年使用:0次
4 . 关于SO2的叙述中,不正确的是
| A.SO2既有氧化性,又有还原性 |
| B.SO2释放到空气中,会造成环境污染 |
| C.SO2中有HCl气体,可以通过饱和Na2SO3溶液除去 |
| D.过量SO2气体通入石蕊溶液中,溶液最终为红色 |
您最近一年使用:0次
名校
解题方法
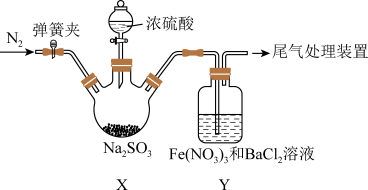
5 . 实验室探究 和
和 溶液反应的原理,装置如图,实验中Y装置产生白色沉淀。下列说法错误的是
溶液反应的原理,装置如图,实验中Y装置产生白色沉淀。下列说法错误的是
 和
和 溶液反应的原理,装置如图,实验中Y装置产生白色沉淀。下列说法错误的是
溶液反应的原理,装置如图,实验中Y装置产生白色沉淀。下列说法错误的是
A.滴加浓硫酸之前应进行的操作是打开弹簧夹,通入 一段时间 一段时间 |
B.Y中产生的白色沉淀是 |
| C.在X装置中浓硫酸体现氧化性和酸性 |
D.若将 换成氨水,Y中能产生白色沉淀 换成氨水,Y中能产生白色沉淀 |
您最近一年使用:0次
2023-03-17更新
|
397次组卷
|
4卷引用:江西省五校2022-2023学年高一下学期直升班联考化学试题
6 . 某实验兴趣小组用氯酸钾(KClO3)和浓盐酸制取氯气,为了制取并验证氯气的某些性质和证明在制备Cl2的过程中会有水蒸气和HCl挥发出来。某甲同学查阅资料知Cl2易溶于CCl4,HCl不溶于CCl4,于是设计如图装置(部分夹持仪器省略)进行实验。
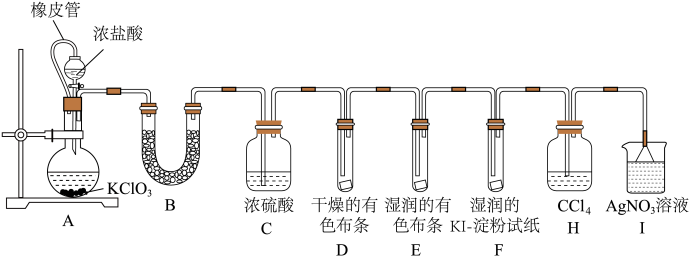
请按要求回答下列问题:
(1)装置A中发生反应的化学方程式为______ ,橡皮管的作用是______ 。
(2)证明混有水蒸气,装置B中的U形接管中所盛试剂为______ 。
(3)装置D、E的实验目的是______ 。
(4)装置F中湿润的KI-淀粉试纸变蓝色,反应的离子方程式为______ 。
(5)证明混有HCl的离子方程式:______ 。
(6)乙同学认为甲同学的实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在H和I两个装置之间再加一个装置瓶检验。你认为该装置瓶中可以放入______ 。

请按要求回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)证明混有水蒸气,装置B中的U形接管中所盛试剂为
(3)装置D、E的实验目的是
(4)装置F中湿润的KI-淀粉试纸变蓝色,反应的离子方程式为
(5)证明混有HCl的离子方程式:
(6)乙同学认为甲同学的实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在H和I两个装置之间再加一个装置瓶检验。你认为该装置瓶中可以放入
您最近一年使用:0次
2023-03-01更新
|
231次组卷
|
3卷引用:江西省九江市修水县第一中学等六校2022-2023学年高一下学期2月第一次联考化学试卷
名校
解题方法
7 . 酸和碱能发生中和反应,它在日常生活和工农业生产中有着广泛的应用。下图表示硫酸和氢氧化钠溶液发生反应时烧杯中溶液的pH随加入液体体积的变化曲线及相关的实验操作。请从中获取信息,回答下列问题:
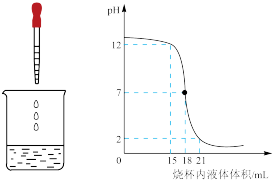
(1)烧杯中盛放的是_______ 溶液。
(2)小明向氢氧化钠溶液中加入稀硫酸,该中和反应的实质是(离子方程式表示)_______ ,然后,对反应过程中溶液的溶质进行了如下探究:
(提出问题)氢氧化钠溶液和稀硫酸混合后,溶质是什么?
(查阅资料)猜想I:硫酸钠和氢氧化钠;
猜想II:硫酸钠和硫酸;
猜想III:_______ 。
(设计实验)
(反思与评价)小芳认为实验操作b.得出的结论不成立,理由是_________ 。可以改为向溶液中加入少量________ ,溶液变为红色,证明猜想II成立

(1)烧杯中盛放的是
(2)小明向氢氧化钠溶液中加入稀硫酸,该中和反应的实质是(离子方程式表示)
(提出问题)氢氧化钠溶液和稀硫酸混合后,溶质是什么?
(查阅资料)猜想I:硫酸钠和氢氧化钠;
猜想II:硫酸钠和硫酸;
猜想III:
(设计实验)
| 实验操作 | 实验现象 | 实验结论 |
| a.取少量溶液于试管中,滴入几滴酚酞溶液 | 溶液无明显变化 | 猜想 |
| b.另取少量溶液于试管中,滴入几滴氯化钡溶液 | 猜想Ⅱ成立 |
您最近一年使用:0次
8 . 若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析不正确的是


| A.Cu与浓硫酸反应,H2SO4体现酸性和还原性 |
| B.a处变红,说明SO2是酸性氧化物 |
| C.b和c处分别褪色,体现SO2的漂白性和还原性 |
| D.试管底部出现白色固体,不能说明反应中否有H2O生成 |
您最近一年使用:0次
2023-12-05更新
|
160次组卷
|
2卷引用:江西省上饶市清源学校2023-2024学年高三上学期12月考试化学试题
9 . 下列说法正确的是
| A.工业上常用MnS作沉淀剂除去废水中的Cu2+,证明Ksp(MnS)>Ksp(CuS) |
| B.将FeCl2溶液滴加到酸性KMnO4溶液中,紫色褪去,证明Fe2+具有还原性 |
| C.红热的炭插入浓硝酸中产生红棕色气体,证明炭与浓硝酸反应生成NO2气体 |
| D.苯、液溴与铁粉混合,生成气体通入AgNO3溶液中,若得到淡黄色沉淀则证明苯与液溴发生取代反应 |
您最近一年使用:0次
2023-02-21更新
|
267次组卷
|
2卷引用:江西省宜春市宜丰中学2022-2023学年高三下学期3月月考化学试题
名校
解题方法
10 . 为了探究氯气的性质进行以下四个实验。下列说法错误的是


| A.四个实验中氯气均表现氧化性 |
| B.四个实验中均有烟产生 |
| C.金属铁和铜在实验中均燃烧得到高价态的金属氯化物 |
| D.氢气需要先验纯,再点燃后送入装有氯气的集气瓶中 |
您最近一年使用:0次
2023-11-12更新
|
191次组卷
|
3卷引用:江西省抚州市黎川县第二中学2023-2024学年高一上学期11月期中化学试题



