名校
解题方法
1 . 某实验小组用如下实验装置模拟工业上制取硝酸:
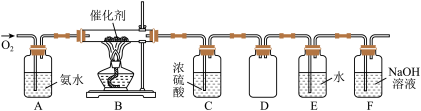
(1)控制氧气的流速是制硝酸的关键,该实验可通过观察氨水中_________ 控制氧气的流速。
(2)写出装置B中发生反应的化学方程式:__________________ 。
(3)由于水的比热容较大,A中挥发的水蒸气会影响B中的反应温度,所以在AB之间插入装有_________ 的干燥装置。
A.浓 B.碱石灰 C.
B.碱石灰 C.
(4)实验后装置 中
中 和
和 物质的量浓度较大的是
物质的量浓度较大的是_________ (填化学名称)。(装置 中发生的主要反应为:
中发生的主要反应为: ;
; )
)
(5)工业上要获得浓度较大的硝酸,往往在稀硝酸中加入吸水剂硝酸镁,然后在较低温度下进行蒸馏,但不能采用较高温度的原因是___________________ 。
(6)请从环境保护角度设计制备硝酸铜的方案,实验室可提供新制硝酸、Cu粉,写出方案中涉及到的化学方程式___________________ ;___________________ 。

(1)控制氧气的流速是制硝酸的关键,该实验可通过观察氨水中
(2)写出装置B中发生反应的化学方程式:
(3)由于水的比热容较大,A中挥发的水蒸气会影响B中的反应温度,所以在AB之间插入装有
A.浓
 B.碱石灰 C.
B.碱石灰 C.
(4)实验后装置
 中
中 和
和 物质的量浓度较大的是
物质的量浓度较大的是 中发生的主要反应为:
中发生的主要反应为: ;
; )
)(5)工业上要获得浓度较大的硝酸,往往在稀硝酸中加入吸水剂硝酸镁,然后在较低温度下进行蒸馏,但不能采用较高温度的原因是
(6)请从环境保护角度设计制备硝酸铜的方案,实验室可提供新制硝酸、Cu粉,写出方案中涉及到的化学方程式
您最近一年使用:0次
2024-01-27更新
|
544次组卷
|
2卷引用:湖南省岳阳市岳阳楼区2022-2023学年高一下学期期末考试化学试题
2 . 已知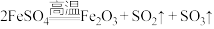 ,某同学设计利用如图装置分别检验产物中的气体。下列有关表述错误的是
,某同学设计利用如图装置分别检验产物中的气体。下列有关表述错误的是
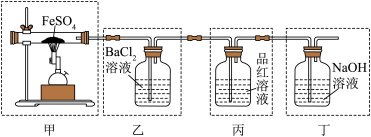
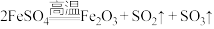 ,某同学设计利用如图装置分别检验产物中的气体。下列有关表述错误的是
,某同学设计利用如图装置分别检验产物中的气体。下列有关表述错误的是
A.用装置甲高温分解 ,点燃酒精喷灯前应先向装置内通一段时间 ,点燃酒精喷灯前应先向装置内通一段时间 |
B.用装置乙可检验分解产生的 ,现象是产生白色沉淀 ,现象是产生白色沉淀 |
C.装置丙中品红溶液不会褪色,无法检验 |
| D.用装置丁可吸收尾气,避免污染环境 |
您最近一年使用:0次
3 . 化学是一门以实验为基础的学科,某同学为探究FeCl3溶液的性质进行如下实验,操作如图所示,根据实验现象,下列分析不正确的是
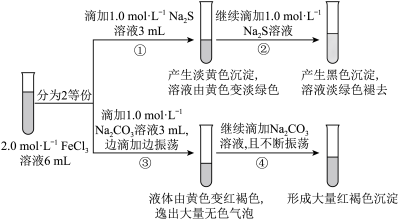

| A.①~④的变化中,有2处涉及氧化还原反应 |
| B.向②后试管加入足量稀盐酸,沉淀部分溶解 |
| C.若将FeCl3溶液滴加到Na2S溶液中,产生的现象与图中①、②现象不相同 |
| D.④中的现象与胶体的聚沉有关 |
您最近一年使用:0次
2023-07-26更新
|
424次组卷
|
3卷引用:湖南省株洲市2023届高三教学质量统一检测(一模)化学试题
解题方法
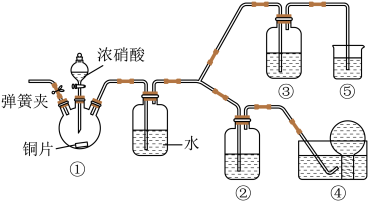
4 . 某学习小组为验证浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO,设计如图装置进行实验(夹持仪器已略去)。
NO与NaOH溶液不反应;NO2与NaOH溶液能反应(2NO2+2NaOH=NaNO3+NaNO2+H2O)。
备选药品:浓硝酸、2.4 mol·L 稀硝酸、蒸馏水、浓硫酸、NaOH溶液及CO2气体。
稀硝酸、蒸馏水、浓硫酸、NaOH溶液及CO2气体。
回答下列问题:
(1)连接好装置,紧接着的操作步骤是___________ ,再加入药品,打开装置①中的弹簧夹后通入CO2气体一段时间,关闭弹簧夹,将装置④中导管末端伸入倒置的烧瓶内,然后再通过①中___________ (填仪器名称)滴入浓硝酸,进行实验。
(2)装置①中发生反应的化学方程式为___________ 。
(3)若用质量分数为63.0%的浓硝酸(密度为1.25 g·cm )配制250 mL 2.4 mol·L
)配制250 mL 2.4 mol·L 的稀硝酸,除量筒、烧杯、胶头滴管、玻璃棒外,还要用到的玻璃仪器有
的稀硝酸,除量筒、烧杯、胶头滴管、玻璃棒外,还要用到的玻璃仪器有___________ ,则需量取63.0%的浓硝酸体积为___________ mL。
(4)装置中盛有水的洗气瓶的主要作用是(用化学方程式回答)___________ 。
(5)根据实验设计,装置③中盛放的试剂是___________ 。
(6)实验证明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO,则②和③装置中的实验现象是___________ 。
NO与NaOH溶液不反应;NO2与NaOH溶液能反应(2NO2+2NaOH=NaNO3+NaNO2+H2O)。
备选药品:浓硝酸、2.4 mol·L
 稀硝酸、蒸馏水、浓硫酸、NaOH溶液及CO2气体。
稀硝酸、蒸馏水、浓硫酸、NaOH溶液及CO2气体。回答下列问题:
(1)连接好装置,紧接着的操作步骤是
(2)装置①中发生反应的化学方程式为
(3)若用质量分数为63.0%的浓硝酸(密度为1.25 g·cm
 )配制250 mL 2.4 mol·L
)配制250 mL 2.4 mol·L 的稀硝酸,除量筒、烧杯、胶头滴管、玻璃棒外,还要用到的玻璃仪器有
的稀硝酸,除量筒、烧杯、胶头滴管、玻璃棒外,还要用到的玻璃仪器有(4)装置中盛有水的洗气瓶的主要作用是(用化学方程式回答)
(5)根据实验设计,装置③中盛放的试剂是
(6)实验证明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO,则②和③装置中的实验现象是
您最近一年使用:0次
5 . 过多 的排放,往往会产生污染。某研究性小组验证
的排放,往往会产生污染。某研究性小组验证 与炽热的铜粉会发生反应
与炽热的铜粉会发生反应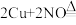
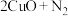 ,方案设计如下:
,方案设计如下: 能被酸性高锰酸钾溶液氧化成
能被酸性高锰酸钾溶液氧化成 ,此体系中产生的
,此体系中产生的 浓度较稀。
浓度较稀。
(1)装置C的名称___________ 。
(2)装置B中Cu单质的作用___________ 。
(3)有关该实验,下列说法不正确的是___________。
(4)实验过程中,装置E中溶液颜色变浅,则装置E发生的离子方程式为___________ 。
(5)有同学发现装置A溶液呈绿色,而不显蓝色;甲认为是该溶液中硝酸铜质量分数较高所致,而乙认为是该溶液溶解了生成的气体所致。设计方案来判断甲或乙哪种合理,下列方案中不可行的是___________。
 的排放,往往会产生污染。某研究性小组验证
的排放,往往会产生污染。某研究性小组验证 与炽热的铜粉会发生反应
与炽热的铜粉会发生反应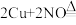
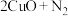 ,方案设计如下:
,方案设计如下:
 能被酸性高锰酸钾溶液氧化成
能被酸性高锰酸钾溶液氧化成 ,此体系中产生的
,此体系中产生的 浓度较稀。
浓度较稀。(1)装置C的名称
(2)装置B中Cu单质的作用
(3)有关该实验,下列说法不正确的是___________。
A.实验开始前要通 ,实验结束后也要通 ,实验结束后也要通 |
| B.B装置中若加入稀硫酸,可以提高氮原子的利用率 |
C.C装置中的 可用无水 可用无水 替代 替代 |
D.F装置中的试剂是 ,吸收尾气,防止污染环境 ,吸收尾气,防止污染环境 |
(5)有同学发现装置A溶液呈绿色,而不显蓝色;甲认为是该溶液中硝酸铜质量分数较高所致,而乙认为是该溶液溶解了生成的气体所致。设计方案来判断甲或乙哪种合理,下列方案中不可行的是___________。
| A.适当加热该绿色溶液,观察颜色变化 |
| B.加水稀释绿色溶液,观察颜色变化 |
| C.向该绿色溶液中通入氮气,观察颜色变化 |
| D.向硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化 |
您最近一年使用:0次
名校
解题方法
6 . 某实验小组利用下图装置探究浓硫酸与葡萄糖反应生成的气体成分。下列说法不正确的是

| A.使浓硫酸与葡萄糖反应发生的操作是将a中的Y形管向左倾斜 |
B.装置b中若出现白色沉淀,不可能是 或 或 |
C.装置d中出现浑浊,证明产生的气体中含有 |
D.装置e中可以盛放 溶液,f的作用为防倒吸 溶液,f的作用为防倒吸 |
您最近一年使用:0次
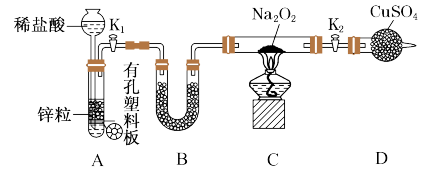
7 . 某同学结合所学知识探究 与
与 能否反应,设计装置如下,下列说法正确的是
能否反应,设计装置如下,下列说法正确的是
 与
与 能否反应,设计装置如下,下列说法正确的是
能否反应,设计装置如下,下列说法正确的是
A.装置A也可直接用于 与浓盐酸反应制取 与浓盐酸反应制取 |
B.装置A气密性检查方法:先关闭活塞 ,再向长颈漏斗中加水,当漏斗中液面高于试管液面且高度不变说明气密性良好 ,再向长颈漏斗中加水,当漏斗中液面高于试管液面且高度不变说明气密性良好 |
| C.装置B中盛放的试剂只是用来除去A中挥发出来的少量水蒸气 |
| D.若装置气密性良好,连接好装置,装好试剂,再直接点燃酒精灯,观察现象 |
您最近一年使用:0次
解题方法
8 . 某研究性学习小组对二氧化硫的制备、性质以及含量测定进行探究。
Ⅰ.制备二氧化硫
用70%的浓硫酸与 固体反应制备
固体反应制备 气体。
气体。
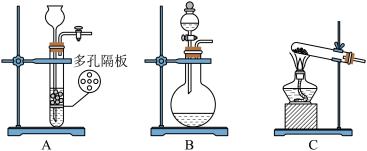
(1)制备 气体最合适的发生装置是
气体最合适的发生装置是___________ (填写字母),反应的化学方程式为___________ 。
Ⅱ.探究 的性质
的性质
在下图装置中先后三次加入相同浓度、相同体积、不同条件下的钡盐溶液,控制食用油油层厚度一致、打开开关K,通入 流速一致。三次实验现象如下表:
流速一致。三次实验现象如下表:

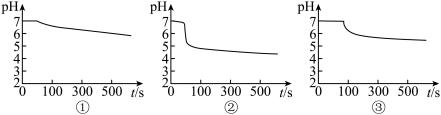
三次实验分别得到如下 图:
图:
(2)A装置中覆盖食用油的目的是___________ 。
(3) 图中,曲线①呈缓慢下降趋势,这是因为
图中,曲线①呈缓慢下降趋势,这是因为___________ ;曲线②出现骤降,这是因为 与
与 溶液中溶解的
溶液中溶解的___________ 发生了氧化还原反应生成了 ;写出实验③中反应的离子方程式为
;写出实验③中反应的离子方程式为___________ 。
Ⅲ.测定空气中二氧化硫含量。
(4)将空气样品经过管道通入密闭容器中的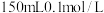 的酸性
的酸性 溶液,若管道中空气流量为
溶液,若管道中空气流量为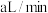 ,经过
,经过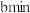 溶液恰好褪色,假设样品中的
溶液恰好褪色,假设样品中的 可被溶液充分吸收。则该空气样品中
可被溶液充分吸收。则该空气样品中 的含量为
的含量为___________  。
。
Ⅰ.制备二氧化硫
用70%的浓硫酸与
 固体反应制备
固体反应制备 气体。
气体。(1)制备
 气体最合适的发生装置是
气体最合适的发生装置是
Ⅱ.探究
 的性质
的性质在下图装置中先后三次加入相同浓度、相同体积、不同条件下的钡盐溶液,控制食用油油层厚度一致、打开开关K,通入
 流速一致。三次实验现象如下表:
流速一致。三次实验现象如下表:| ① | ② | ③ |
已煮沸的 溶液 溶液 | 未煮沸的 溶液 溶液 | 己煮沸的 溶液 溶液 |
| 无白色沉淀生成 | 有白色沉淀生成 | 有白色沉淀生成 |

三次实验分别得到如下
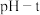 图:
图:
(2)A装置中覆盖食用油的目的是
(3)
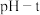 图中,曲线①呈缓慢下降趋势,这是因为
图中,曲线①呈缓慢下降趋势,这是因为 与
与 溶液中溶解的
溶液中溶解的 ;写出实验③中反应的离子方程式为
;写出实验③中反应的离子方程式为Ⅲ.测定空气中二氧化硫含量。
(4)将空气样品经过管道通入密闭容器中的
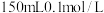 的酸性
的酸性 溶液,若管道中空气流量为
溶液,若管道中空气流量为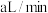 ,经过
,经过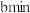 溶液恰好褪色,假设样品中的
溶液恰好褪色,假设样品中的 可被溶液充分吸收。则该空气样品中
可被溶液充分吸收。则该空气样品中 的含量为
的含量为 。
。
您最近一年使用:0次
9 . 将1.95gNa2O2加入水中,反应后配成50mL溶液A,进行如下实验。下列说法错误的是
| 编号 | ① | ② | ③ | ④ |
| 操作 | 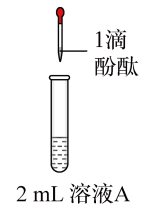 | 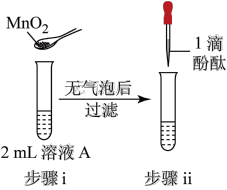 | 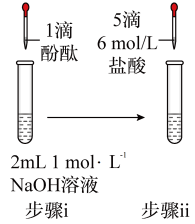 | 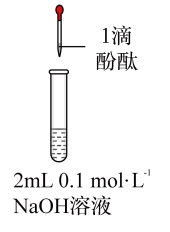 |
| 现象 | 溶液变红色,20秒后褪色 | ⅰ.产生大量使带火星的木条复燃的气体 ⅱ.溶液变红色,10分钟后褪色 | ⅰ.溶液变红色,10分钟后溶液褪色 ⅱ.溶液变红色 | 溶液变红色,2小时后无明显变化 |
| A.由实验可知,Na2O2与水反应有H2O2生成 |
B.②、③溶液褪色与 浓度较大有关 浓度较大有关 |
C.若向①褪色后的溶液中滴加5滴 盐酸,溶液将变红 盐酸,溶液将变红 |
D.若向④中继续滴加 盐酸或 盐酸或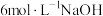 溶液,溶液均可能褪色 溶液,溶液均可能褪色 |
您最近一年使用:0次
2023-07-07更新
|
1099次组卷
|
6卷引用:湖南省邵阳市第二中学2023-2024学年高一上学期基础知识竞赛化学试题
10 . Ⅰ.氨的制备
氨在化工生产领域有广泛应用,历史上曾有三位科学家在合成氨领域获得诺贝尔化学奖。

(1)实验室常用铵盐与强碱反应制取氨气,可选择装置___________ (填“A”或“B”),反应的化学方程式为___________ 。
(2)制备干燥的 时,发生、净化、收集和尾气处理装置的接口顺序为
时,发生、净化、收集和尾气处理装置的接口顺序为___________ (按气流方向填写小写字母)
(3)检验某溶液中存在 的操作及现象为
的操作及现象为___________ 。
(4)工业上在一定温度和催化剂条件下,可用 消除
消除 污染,生成两种对环境无害的物质,请写出
污染,生成两种对环境无害的物质,请写出 与
与 反应的化学方程式
反应的化学方程式___________ 。
Ⅱ.某实验小组研究 与溶液的反应,实验如下:
与溶液的反应,实验如下:
实验中所取镁粉质量均为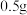 ,分别加入到选取的实验试剂中。
,分别加入到选取的实验试剂中。
资料:a. 溶液呈中性;b.Cl-对该反应几乎无影响。
溶液呈中性;b.Cl-对该反应几乎无影响。
(5)甲同学认为实验2比实验1反应剧烈的原因是 溶液中
溶液中 大,与Mg反应快。乙同学通过实验3证明甲同学的说法不合理。
大,与Mg反应快。乙同学通过实验3证明甲同学的说法不合理。
试剂X是___________ 。
(6)为进一步探究实验2反应剧烈的原因,进行实验4:
依据上述实验,可以得出Mg能与 反应生成
反应生成 ,乙同学认为该方案不严谨,需要补充的实验方案是
,乙同学认为该方案不严谨,需要补充的实验方案是___________ 。
实验总结:通过上述实验,该小组同学得出Mg能与 反应生成
反应生成 的结论。
的结论。
氨在化工生产领域有广泛应用,历史上曾有三位科学家在合成氨领域获得诺贝尔化学奖。

(1)实验室常用铵盐与强碱反应制取氨气,可选择装置
(2)制备干燥的
 时,发生、净化、收集和尾气处理装置的接口顺序为
时,发生、净化、收集和尾气处理装置的接口顺序为(3)检验某溶液中存在
 的操作及现象为
的操作及现象为(4)工业上在一定温度和催化剂条件下,可用
 消除
消除 污染,生成两种对环境无害的物质,请写出
污染,生成两种对环境无害的物质,请写出 与
与 反应的化学方程式
反应的化学方程式Ⅱ.某实验小组研究
 与溶液的反应,实验如下:
与溶液的反应,实验如下:实验中所取镁粉质量均为
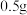 ,分别加入到选取的实验试剂中。
,分别加入到选取的实验试剂中。资料:a.
 溶液呈中性;b.Cl-对该反应几乎无影响。
溶液呈中性;b.Cl-对该反应几乎无影响。| 实验 | 实验试剂 | 实验现象 |
| 1 |  蒸馏水 蒸馏水 | 反应缓慢,有少量气泡产生(经检验为H2) |
| 2 | 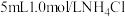 溶液 溶液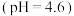 | 剧烈反应,产生刺激性气味气体和灰白色难溶固体 |
 溶液中
溶液中 大,与Mg反应快。乙同学通过实验3证明甲同学的说法不合理。
大,与Mg反应快。乙同学通过实验3证明甲同学的说法不合理。| 实验 | 实验装置 | 现象 |
| 3 | 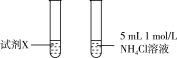 | 两试管反应剧烈程度相当 |
(6)为进一步探究实验2反应剧烈的原因,进行实验4:
| 实验 | 实验试剂 | 实验现象 |
| 4 | 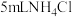 乙醇溶液 乙醇溶液 | 有无色无味气体产生(经检验为 ) ) |
 反应生成
反应生成 ,乙同学认为该方案不严谨,需要补充的实验方案是
,乙同学认为该方案不严谨,需要补充的实验方案是实验总结:通过上述实验,该小组同学得出Mg能与
 反应生成
反应生成 的结论。
的结论。
您最近一年使用:0次



