1 . 中国“奋斗号”载人潜水器在马里亚纳海沟成功坐底深度10909米,挑战了全球海洋最深处。国产新型钛合金、能源供给锂电池等功不可没。磷酸亚铁锂 可作为锂电池的正极材料,请回答下列问题:
可作为锂电池的正极材料,请回答下列问题:
(1)潜水器外壳使用的钛合金不可能具有的性质是______(单选).
(2)锂电池工作时,将化学能转化为______ 。
(3)锂位于元素周期表中第______ 周期______ 族;磷酸亚铁锂 中
中 的化合价为
的化合价为______ .
(4)铁的原子结构示意图为 .由此可知,铁的原子序数为
.由此可知,铁的原子序数为______ ;x为______ ;铁元素是______ (双选).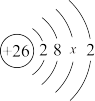 A.主族元素 B.副族元素 C.短周期元素 D.长周期元素
A.主族元素 B.副族元素 C.短周期元素 D.长周期元素
(5)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是______(单选).
(6)能与 反应,且可证明
反应,且可证明 具有氧化性的是______(双选).
具有氧化性的是______(双选).
(7)除去氯化亚铁溶液中的氯化铁,需加入______ ,发生的离子反应为______ ,要检验废液中是否还存在 ,实验方案是
,实验方案是____________ 。
(8) 可作载人潜水器供氧剂,下列关于
可作载人潜水器供氧剂,下列关于 说法正确的是______(单选)。
说法正确的是______(单选)。
钛因为具有神奇的性能越来越引起人们的关注.常温下钛不与非金属、强酸反应。目前大规模生产钛的方法是,第一步将金红石(含 )、炭粉混合,在高温条件下通入
)、炭粉混合,在高温条件下通入 制得
制得 :
: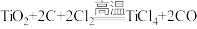 ①;第二步在氩气的气氛中,用过量的镁在加热条件下与
①;第二步在氩气的气氛中,用过量的镁在加热条件下与 反应制得金属钛:
反应制得金属钛: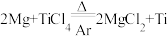 ②。
②。
(9)反应①的还原剂为______ ,反应消耗了标准状况下 氯气,则反应①转移的电子数为
氯气,则反应①转移的电子数为___ 。
(10)简述从反应②所得产物中获取金属钛的步骤:______________ 。
 可作为锂电池的正极材料,请回答下列问题:
可作为锂电池的正极材料,请回答下列问题:(1)潜水器外壳使用的钛合金不可能具有的性质是______(单选).
| A.耐高压 | B.耐腐蚀 | C.硬度小 | D.密度小 |
(3)锂位于元素周期表中第
 中
中 的化合价为
的化合价为(4)铁的原子结构示意图为
 .由此可知,铁的原子序数为
.由此可知,铁的原子序数为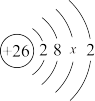 A.主族元素 B.副族元素 C.短周期元素 D.长周期元素
A.主族元素 B.副族元素 C.短周期元素 D.长周期元素(5)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是______(单选).
A. | B. | C. | D. |
 反应,且可证明
反应,且可证明 具有氧化性的是______(双选).
具有氧化性的是______(双选).A. | B. | C. | D. |
 ,实验方案是
,实验方案是(8)
 可作载人潜水器供氧剂,下列关于
可作载人潜水器供氧剂,下列关于 说法正确的是______(单选)。
说法正确的是______(单选)。| A.只有离子键 | B.可在常温下由 与 与 反应制得 反应制得 |
C.与 发生化合反应 发生化合反应 | D.与 反应有 反应有 生成 生成 |
钛因为具有神奇的性能越来越引起人们的关注.常温下钛不与非金属、强酸反应。目前大规模生产钛的方法是,第一步将金红石(含
 )、炭粉混合,在高温条件下通入
)、炭粉混合,在高温条件下通入 制得
制得 :
: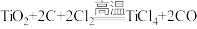 ①;第二步在氩气的气氛中,用过量的镁在加热条件下与
①;第二步在氩气的气氛中,用过量的镁在加热条件下与 反应制得金属钛:
反应制得金属钛: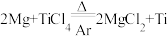 ②。
②。(9)反应①的还原剂为
 氯气,则反应①转移的电子数为
氯气,则反应①转移的电子数为(10)简述从反应②所得产物中获取金属钛的步骤:
您最近一年使用:0次
名校
解题方法
2 . 按要求回答下列问题
Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:_______ 。
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾)。取补铁剂少许溶于水配成溶液,_______ (填写实验操作、现象和结论)
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(3)镁铝合金的硬度比金属铝的硬度_______ (选填:大、小)。使用该合金前用NaOH溶液处理Al2O3,其离子方程式为_______ 。取一定量的镁铝合金均分为两份,分别与足量的盐酸、NaOH溶液充分反应,产生气体的物质的量之比为5:3,合金中镁铝的物质的量之比为_______ 。
Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾)。取补铁剂少许溶于水配成溶液,
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(3)镁铝合金的硬度比金属铝的硬度
您最近一年使用:0次
名校
解题方法
3 . 按要求回答下列问题
Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:___________ 。
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾、过氧化氢),取补铁剂少许溶于水配成溶液,___________ (填写实验操作、现象和结论)
(3)氢氧化亚铁在空气中极不稳定,易被空气中氧气氧化。这一过程中观察到的现象是___________ ,反应的化学方程式是___________ 。
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(4)镁铝合金的硬度比金属铝的硬度___________ (选填:大、小)。使用该合金前用NaOH溶液处理Al2O3,其离子方程式为___________ 。取一定量的镁铝合金均分为两份,分别与足量的盐酸、NaOH溶液充分反应,产生气体的物质的量之比为5:3,合金中镁铝的物质的量之比为___________ 。
Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾、过氧化氢),取补铁剂少许溶于水配成溶液,
(3)氢氧化亚铁在空气中极不稳定,易被空气中氧气氧化。这一过程中观察到的现象是
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(4)镁铝合金的硬度比金属铝的硬度
您最近一年使用:0次
2024-01-08更新
|
54次组卷
|
2卷引用:吉林省长春外国语学校2023-2024学年高一上学期12月月考化学试题
解题方法
4 . Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫胶亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:________________________ 。
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾、过氧化氢),__________ (填写实验操作、现象和结论)
(3)氢氧化亚铁在空气中极不稳定,易被空气中氧气氧化。这一过程中观察到的现象是__________ ,反应的化学方程式是______________ 。
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(4)镁铝合金的硬度比金属铝的硬度______ (选填:大、小)。使用该合金前用NaOH溶液处理Al2O3,其离子方程式为_________ 。取一定量的镁铝合金均分为两份,分别与足量的盐酸、NaOH溶液充分反应,产生气体的物质的量之比为5:3。合金与NaOH溶液反应的化学方程式为__________ 。合金中镁铝的物质的量之比为_____________ 。
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾、过氧化氢),
(3)氢氧化亚铁在空气中极不稳定,易被空气中氧气氧化。这一过程中观察到的现象是
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(4)镁铝合金的硬度比金属铝的硬度
您最近一年使用:0次
解题方法
5 . 鄂东地区富含铜矿。下列有关铜的说法正确的是
| A.铜元素位于周期表d区 | B.铜的焰色试验为红色 |
C. 含配位键 含配位键 | D.青铜的硬度小于纯铜 |
您最近一年使用:0次
6 . 2022年11月29日,神舟十五号载人飞船成功发射。下列说法不 正确的是
| A.光束通过空间站使用的纳米气凝胶时,可观察到丁达尔效应 |
| B.新一代运载火箭使用的液氢和液氧均为非金属单质 |
| C.飞船外壳材料使用的是钛合金,其熔点高于纯钛 |
| D.空间站使用石墨烯存储器,石墨烯与金刚石互为同素异形体 |
您最近一年使用:0次
7 . 近年来,我国航天成就显著。下列有关说法正确的是
| A.某运载火箭利用液氧和煤油为燃料,煤油的主要成分为酯类物质 |
| B.飞船返回舱表层材料中的玻璃纤维属于有机高分子材料 |
| C.火箭箭体采用铝合金主要是为了美观耐用 |
| D.北斗卫星导航系统所用芯片的主要成分为硅 |
您最近一年使用:0次
8 . 西安是首批国家历史文化名城,历史上有13个朝代在此建都,是世界四大古都之一,不仅拥有厚重的历史,同时也展现着现代大都市的活力和浪漫。下列说法错误的是
| A.半坡出土的“人面鱼纹彩陶盆”是新石器时代仰韶文化的遗物,该陶盆的材料属于传统无机非金属材料 |
| B.西安城墙又称西安明城墙,是中国现存规模最大、保存最完整的古代城垣,城垣上青灰色砖瓦的颜色主要是因为其中含有氧化铁 |
| C.大唐芙蓉园的灯光秀吸引着中外游客,激光灯柱透过空气呈现着优美的图案,同时也体现着胶体的性质——丁达尔效应 |
| D.“长安塔”位于西安世界园艺博览会园区制高点小终南山上,采用了大量钢材结构、玻璃和不锈钢,其中不锈钢、钢材均属于金属材料 |
您最近一年使用:0次
9 . 下列关于材料说法不正确的是
A | 在纯金属中加入其他元素形成合金 | 改变了金属原子有规则的层状排列,硬度变大 |
B | 石墨通过化学剥离法制得石墨烯 | 石墨烯的导电性、导热性更好 |
C | 在涤纶纤维中混纺天然纤维 | 增强了透气性和吸湿性 |
D | 顺丁橡胶硫化 | 硫化程度越高,强度越大,弹性越好 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 我国科学家通过机械化学方法,在氢化镧(LaH1.95~3)晶格中制造大量的缺陷和纳米微晶,研发出首个室温环境下超快氢负离子(H−)导体。下列说法不正确 的是
| A.电负性:La > H | B.氢属于s区元素 |
| C.H−具有还原性 | D.超快氢负离子导体有望用于新型电池研发 |
您最近一年使用:0次
2024-04-15更新
|
258次组卷
|
2卷引用:北京市丰台区2023-2024学年高三下学期综合练习(一)化学试题



