1 . H2O2是重要的化学试剂,在实验室和生产实际中应用广泛。
(1)写出H2O2的结构式:________ ,H2O2在MnO2催化下分解的化学方程式:__________ 。
(2) ①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:_______________ 。
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是____________ 。
(3)H2O2还有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:___________________ 。
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在________ (填“酸式”或“碱式”)滴定管中,判断到达滴定终点的现象是__________________ ;
(4)H2O2是一种二元弱酸,其与过量的Ba(OH)2反应的化学方程式为_____________ 。
(1)写出H2O2的结构式:
(2) ①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是
(3)H2O2还有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在
(4)H2O2是一种二元弱酸,其与过量的Ba(OH)2反应的化学方程式为
您最近一年使用:0次
2 . 碘是人类必需的生命元素,在人体的生长发育过程中起着重要作用,实验小组进行碘单质的制备。
【查阅资料】碱性条件下,I2会发生歧化反应生成I-和IO3-,酸性条件下, I-和IO3-又会发生归中反应生成I2;碘在水中的溶解度为0.029g。
【碘的制取】以海带为原料,按照以下步骤进行实验。
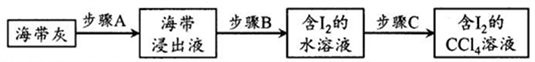
(1)步骤B发生的反应是“氧化”,这一操作中可供选用的试剂: ①Cl2;②Br2;③稀硫酸和H2O2,从无污染角度考虑,你认为合适试剂是______ (填编号),反应中I-转化为I2 的离子反应方程式为________ 。
(2)步骤C中使用的起到分离作用的仪器是_______ ,使用该仪器时,第一步操作是_______________ 。
(3)有同学查资料后发现CCl4有毒,提议用乙醇代替,请判断该提议是否可行,原因是_______________ 。
(4)【碘的分离】得到含I2的CCl4溶液后,利用下图装置进行碘的提取并回收溶剂。

图中有两处明显错误,分别是①_________ ;②_________ 。
【查阅资料】碱性条件下,I2会发生歧化反应生成I-和IO3-,酸性条件下, I-和IO3-又会发生归中反应生成I2;碘在水中的溶解度为0.029g。
【碘的制取】以海带为原料,按照以下步骤进行实验。

(1)步骤B发生的反应是“氧化”,这一操作中可供选用的试剂: ①Cl2;②Br2;③稀硫酸和H2O2,从无污染角度考虑,你认为合适试剂是
(2)步骤C中使用的起到分离作用的仪器是
(3)有同学查资料后发现CCl4有毒,提议用乙醇代替,请判断该提议是否可行,原因是
(4)【碘的分离】得到含I2的CCl4溶液后,利用下图装置进行碘的提取并回收溶剂。

图中有两处明显错误,分别是①
您最近一年使用:0次



