福建省长泰县第一中学2017-2018学年高一上学期期中考试化学试题
福建
高一
期中
2017-12-11
244次
整体难度:
适中
考查范围:
认识化学科学、化学实验基础、常见无机物及其应用
一、单选题 添加题型下试题
| A.12g碳所含的原子数就是阿伏伽德罗常数 |
| B.阿伏伽德罗常数没有单位 |
| C.“物质的量”指物质的质量 |
| D.摩尔是表示物质的量的单位,每摩尔物质含有阿伏伽德罗常数个微粒 |
| A.0.8 mol二氧化碳 |
| B.标准状况下2.24L氨气 |
| C.3.6g水(水的摩尔质量为18g·mol-1) |
| D.含NA个氢分子的氢气 |
【知识点】 化学计量
A.2Al+Fe2O3 2Fe+Al2O3 2Fe+Al2O3 | B.2Mg+CO2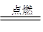 2MgO+C 2MgO+C |
C.N2+3H2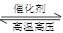 2NH3 2NH3 | D.SiO2+CaO CaSiO3 CaSiO3 |
| A.铜 | B.蔗糖 | C.三氧化硫 | D.醋酸 |
【知识点】 电解质
| A.X2与Y2 | B.XY 与X2 | C.X2与YX | D.YX 与Y2 |
【知识点】 阿伏加德罗定律
| A.含氧原子的个数比为2∶3 |
| B.含硫元素的质量比是5∶4 |
| C.含氧元素的质量比为5∶4 |
| D.含硫原子的个数比为1∶1 |
| A.纯碱从物质的分类看不属于碱 | B.由一种元素组成的物质一定是单质 |
| C.单质只能用置换反应制取 | D.含氧元素的化合物称为氧化物 |
【知识点】 无机物质的分类
二、未知 添加题型下试题
三、单选题 添加题型下试题
| A.某溶液与NaOH 溶液共热,产生使湿润的红色石蕊试纸变蓝色的气体,说明原溶液中存在NH4+ |
| B.某溶液中加入AgNO3 溶液时,产生白色沉淀,说明原溶液中一定存在Cl- |
| C.某溶液中滴加BaCl2 溶液时,产生白色沉淀,说明原溶液中一定存在SO42- |
| D.焰色反应中火焰显黄色,说明样品中存在钠元素,不存在钾元素 |
【知识点】 化学实验基础
| A.氯化钠溶液在电流作用下电离成Na+与Cl‑ |
| B.溶于水后能电离出H+的化合物都是酸 |
| C.氯化氢水溶液能导电,所以氯化氢是电解质 |
| D.O2的水溶液能不导电,所以O2是非电解质 |
【知识点】 电解质与非电解质
A.H2CO3 CO2↑+H2O(分解反应) CO2↑+H2O(分解反应) |
B.3CO+Fe2O3 2Fe+3CO2(置换反应) 2Fe+3CO2(置换反应) |
C.2KClO3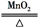 2KCl+3O2↑(氧化还原反应) 2KCl+3O2↑(氧化还原反应) |
| D.2FeCl2+Cl2====2FeCl3(化合反应) |
| A.Zn→H2 | B.Cu→Cu(OH)2 |
| C.CO2→CaCO3 | D.KMnO4→MnO2 |
【知识点】 无机综合推断
| A.0.1mol Zn,0.1mol Fe | B.1mol Fe,1mol Zn |
| C.1g Zn,1g Fe | D.10g Zn,10g Fe |
【知识点】 化学计量
| A.除去CO2中的少量HCl:通入NaOH溶液 |
| B.除去NaCl溶液中的少量MgCl2:加入适量KOH溶液,过滤 |
| C.除去KCl溶液中的少量K2CO3:加入适量的盐酸 |
| D.除去N2中的少量O2:通过灼热的CuO粉末 |
【知识点】 物质分离、提纯的常见化学方法解读
| A.密度比为16∶11 |
| B.分子个数比为16∶11 |
| C.体积比为1∶1 |
| D.氧原子个数比为1∶1 |
【知识点】 阿伏加德罗定律 阿伏加德罗定律及其推论解读
| A.10 mL 1 mol·L-1 NaNO3溶液 |
| B.10 mL 1 mol·L-1 Al(NO3)3溶液 |
| C.15 mL 2 mol·L-1 AgNO3溶液 |
| D.10 mL 1.5 mol·L-1 Cu(NO3)2溶液 |
【知识点】 化学计量
四、填空题 添加题型下试题
(1)写出Al2(SO4)3在水溶液中的电离方程式:
(2)该溶液中Al2(SO4)3的物质的量浓度为
(3)从该溶液中取出10mL,其中SO42— 的物质的量浓度为
(4)从该溶液中取出10mL,稀释到100mL,稀释后溶液中溶质Al2(SO4)3的物质的量浓度为
【知识点】 物质的量浓度的计算
(1)88gCO2在标准状况下所占体积为
(2)3.01×1024个OH—与
(3)19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的相对分子质量是
(4)质量比为16:7:6的三种气体 SO2、CO 、NO,分子个数之比为
(5)等物质的量浓度、等体积的盐酸与硫酸,其H+的个数比为
【知识点】 物质的量有关计算
A.萃取分液 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤
(1)分离饱和食盐水与沙子的混合物
(2)从硝酸钾和氯化钠的混合液中获得硝酸钾
(3)分离水和汽油的混合物
(4)分离酒精(沸点为78.1℃)和甲苯(沸点为110.6℃)两种互溶液体
(5)从碘水中提取碘单质
【知识点】 物质分离、提纯的常见物理方法
五、解答题 添加题型下试题
(1)各取适量固体试剂分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到5种固体全部溶解,1支试管中得到蓝色溶液,被检出物质的化学式是
(2)分别取四种未检出的溶液,往其中加入上述已检出的溶液,观察到1支试管中有白色沉淀生成,则被检出物质的化学式是
另1支试管中有蓝色沉淀生成,则被检出物质的化学式是
(3)取(2)中产生蓝色沉淀的原无色溶液,分别加入尚未检出的最后两溶液中,并加热,有刺激性气味气体产生的原未知液是
【知识点】 物质的检验 无机物的检验 物质检验和鉴别的实验方案设计解读
六、计算题 添加题型下试题
【知识点】 化学方程式计算中物质的量的运用解读
试卷分析
试卷题型(共 25题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 物理变化与化学变化 | |
| 2 | 0.65 | 阿伏加德罗常数 物质的量的含义 摩尔 阿伏加德罗常数的含义 | |
| 3 | 0.64 | 化学计量 | |
| 4 | 0.94 | 氧化还原反应基本概念 氧化还原反应的定义及实质 氧化还原反应定义、本质及特征 | |
| 5 | 0.65 | 胶体的性质和应用 | |
| 6 | 0.85 | 电解质 | |
| 7 | 0.64 | 阿伏加德罗定律 | |
| 8 | 0.65 | 根据n=m/M进行相关计算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 9 | 0.65 | 无机物质的分类 | |
| 10 | 0.65 | 无机物质的分类 | |
| 12 | 0.64 | 化学实验基础 | |
| 13 | 0.65 | 化学实验基础操作 | |
| 14 | 0.65 | 电解质与非电解质 | |
| 15 | 0.65 | 四种基本反应类型 | |
| 16 | 0.65 | 无机综合推断 | |
| 17 | 0.64 | 化学计量 | |
| 18 | 0.65 | 物质分离、提纯的常见化学方法 | |
| 19 | 0.85 | 阿伏加德罗定律 阿伏加德罗定律及其推论 | |
| 20 | 0.64 | 化学计量 | |
| 二、未知 | |||
| 11 | 0.94 | 胶体的定义及分类 | 未知 |
| 三、填空题 | |||
| 21 | 0.65 | 物质的量浓度的计算 | |
| 22 | 0.4 | 物质的量有关计算 | |
| 23 | 0.65 | 物质分离、提纯的常见物理方法 | |
| 四、解答题 | |||
| 24 | 0.65 | 物质的检验 无机物的检验 物质检验和鉴别的实验方案设计 | 实验探究题 |
| 五、计算题 | |||
| 25 | 0.65 | 化学方程式计算中物质的量的运用 | |







