26. 2018年1月11日,广西某地高速公路大桥上用于融冰作业的2包共100公斤含有亚硝酸钠的工业盐遗失,当地迅速组织警力开展搜寻遗失的工业盐,确保不流入市场和家庭。
【资料卡1】亚硝酸钠与食盐氯化钠相似,为白色有咸味的固体,但误食会使人中毒。腌制食品、泡菜等制作过程中会产生亚硝酸钠。
根据以上资料,回答下列问题:
(1)用盐融冰的原理是
____ ,该过程主要发生的是
___ (填“物理变化”或“化学变化”)。
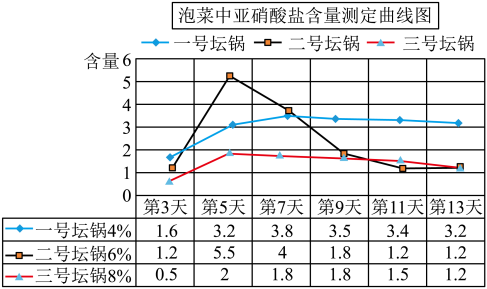
(2)下图是用不同浓度盐水腌制泡菜过程中亚硝酸盐含量测定曲线图。据此回答:当盐水浓度为6%时,第
____ 天亚硝酸盐含量达到最大值。为了安全,泡菜腌制时盐水浓度最好是
____ 并在腌制
____ 天后再食用。
(3)兴趣小组欲测定某工业盐中亚硝酸钠的质量分数
【资料卡2】实验室常用亚硝酸钠与氯化铵溶液反应制取纯净的氮气,其化学方程式为:NaNO
2 + NH
4Cl

NaCl + N
2↑+ 2H
2O(此反应是放热反应)
【资料卡3】在酸性环境中高锰酸钾能与亚硝酸钠发生如下反应:2KMnO
4 + 5NaNO
2 + 3H
2SO
4 = K
2SO
4 + 2MnSO
4 + 5NaNO
3 + 3H
2O
【方案一】取1g该工业盐样品与足量氯化铵溶液于如图装置中充分反应(该工业盐中其他成分不与氯化铵溶液反应),实验时加热片刻后,即可移去酒精灯,其原因
___ 。最终量筒中收集到300mL水,已知该条件下氮气的密度为1.25g/L,则该工业盐样品中亚硝酸钠的质量分数为
____ (写出计算过程,结果保留一位小数,)。

实验结束后发现测量结果偏大,可能原因是
____ 。
【方案二】为更准确地测定该工业盐中亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用含量为15.8g/L的酸性KMnO
4溶液进行反应,实验所得数据如下表所示:
| 实验次序 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积(mL) | 20.60 | 20.02 | 20.00 | 19.98 |
上述第
____ 次实验所得数据明显异常,剔除异常数据后,计算出该工业盐中亚硝酸钠的质量分数为
___ 。