16. 空气中的氧气含量测定再认识。
实验过程如下:
A 在实际容积为230mL的集气瓶里,先装进30mL的水,用止水夹夹紧橡皮管;
B 点燃燃烧匙内的红磷,观察到红磷燃烧,立即伸入瓶中并塞紧瓶塞;
C 等装置冷却至室温后,打开止水夹。
(1)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内
_______减小,烧杯中水倒吸到集气瓶,进入水的体积即为氧气的体积。红磷燃烧的文字表达式为
_______。
(2)红磷燃烧的主要现象是
_______。若实验非常成功,红磷熄灭后,待装置冷却至室温,打开止水夹,观察到烧杯中的水倒吸入集气瓶,最终集气瓶中水的总体积约为
_______mL。实际观察水面的变化情况发现,集气瓶内上升的水面小于瓶内原有气体体积的五分之一,可能的原因是:
_______(写一种即可)
(3)上面的实验同时证明了氮气
_______(填“易”或“难”)溶于水和化学性质
_______(填“活泼”或“不活泼”)的结论。
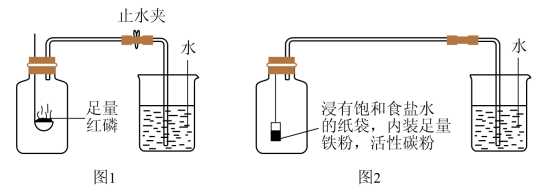
【查阅资料】
燃烧过程中当氧气体积分数低于8.8%时,红磷就无法继续燃烧,因此通过上述实验测定空气中氧气的含量,测定结果与理论值误差较大。
【实验改进】
(一)根据铁在空气中生锈的原理设计如图2实验装置,再次测定空气中氧气含量。铁生锈是缓慢氧化,对氧气浓度要求小。(提示:铁生锈会消耗空气中的氧气和水蒸气,装置中饱和食盐水、活性炭会加速铁生锈。)
(二)测得实验数据如下:
| 实验前 | 实验后 |
| 烧杯中的水的体积 | 烧杯中剩余水的体积 |
| 80.0mL | 54.5mL |
已知:集气瓶(扣除内容物)和导管的总体积=126.0mL。
(4)根据测得实验数据计算:进入集气瓶中水的体积是
_______mL,改进实验后测得的空气中氧气的体积分数是
_______(计算结果精确到0.1%)。
(5)对比两个实验,你觉得改进后实验的优点有
_______(写一点)。
(6)丁同学设想用图1装置,换用铁粉和活性炭(主要成分碳)代替红磷将其燃烧,进行氧气含量的测定,你认为是否可行
_______(填“可行”或“不行”)。理由:
_______。