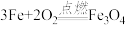江苏省扬州市2021年中考化学试题
江苏
九年级
中考真题
2021-06-20
1511次
整体难度:
适中
考查范围:
化学与社会发展、物质的化学变化、物质构成的奥秘、身边的化学物质、化学实验
一、选择题 添加题型下试题
| A.铁 | B.碳 | C.氢 | D.氧 |
【知识点】 人体内的常量元素解读 人体内的微量元素——碘、铁元素解读
| A.高炉炼铁 | B.冰雪融化 | C.食物变质 | D.木材燃烧 |
【知识点】 化学变化与物理变化判断解读
| A.氢氧化钾 | B.铝 | C.金刚石 | D.水 |
【知识点】 物质化学性质的决定因素解读
| A.导电性 | B.延展性 | C.导热性 | D.抗腐蚀性 |
【知识点】 金属的物理通性与用途解读
A. | B. | C. | D. |
【知识点】 与爆炸和燃烧有关图标的辨认解读
 。X的化学式是
。X的化学式是| A.Fe | B.FeCl2 | C.Fe(OH)2 | D.Fe(OH)3 |
【知识点】 根据方程式推测化学式解读
| A.干冰:CO2 | B.小苏打:NaHCO3 | C.纯碱:Na2CO3 | D.熟石灰:CaO |
【知识点】 常见酸、碱的俗称及化学式解读 常见盐的俗名、用途解读
| A.肥皂水:pH=10.2 | B.唾液:pH=6.8 | C.柠檬汁:pH=2.5 | D.洗涤剂:pH=12.2 |
【知识点】 溶液酸碱性及pH相关关系解读
| A.H、O原子个数比为2:1 | B.相对分子质量为(12+1+16) |
| C.蔗糖中含45种元素 | D.氧元素的质量分数最小 |
【知识点】 化学式、分子式及涵义解读 根据化学式计算元素质量分数解读
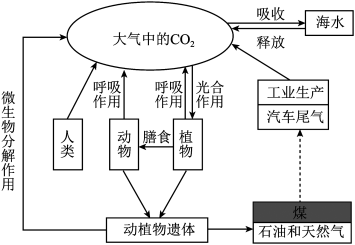
| A.向空气中排放CO2会形成酸雨 | B.无机物和有机物不可相互转化 |
| C.植树造林有利于吸收CO2 | D.煤、石油和天然气是可再生能源 |
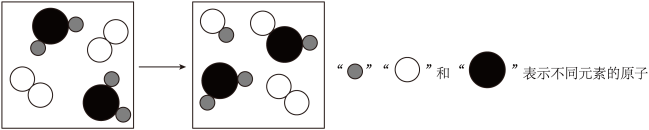
| A.反应有单质生成 | B.反应前后原子种类、数目不变 |
| C.反应物和生成物共有8种物质 | D.该反应为置换反应 |
【知识点】 微粒图像的分析及应用解读
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 稀盐酸的用量/g | 5.0 | 5.0 | 5.0 | 5.0 |
| 剩余固体的质量/g | 1.5 | 1.0 | 0.5 | 0.3 |
| A.第三次实验后碳酸钙无剩余 | B.第四次实验后盐酸无剩余 |
| C.盐酸中HCl的质量分数是3.65% | D.样品中碳酸钙的质量分数是85% |
【知识点】 含杂质的化学方程式计算解读 化学方程式与实验的计算解读
| A.生石灰具有吸水性,可用作干燥剂 | B.氮气性质稳定,可用作保护气 |
| C.金属铁具有导电性,可用于制炊具 | D.盐酸易挥发,可用于除铁锈 |
A.量取浓硫酸 | B.测稀硫酸pH 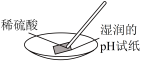 |
C.制取氢气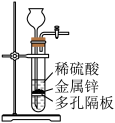 | D.收集氢气 |
二、多选题 添加题型下试题
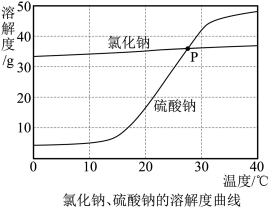
| A.加水能使NaCl溶液从不饱和变为饱和 |
| B.20℃时,NaCl的溶解度比Na2SO4大 |
| C.P点时,NaCl与Na2SO4的饱和溶液质量分数相等 |
| D.将Na2SO4饱和溶液从30℃冷却至10℃,有晶体析出,溶液变为不饱和 |
【知识点】 饱和溶液和不饱和溶液的转换解读 固体溶解度曲线的应用解读
三、选择题 添加题型下试题
| 选项 | 实验操作和现象 | 结论 |
| A | 将某气体通过灼热的黑色氧化铜固体,固体变红 | 该气体是氢气 |
| B | 将铜片和银片投入稀硫酸中,均无气泡放出 | 铜、银的金属活动性相同 |
| C | 向NaOH溶液中滴加稀盐酸,无明显现象 | 该过程中未发生化学反应 |
| D | 向某溶液中滴加酚酞试液,有红色出现 | 该溶液显碱性 |
| A.A | B.B | C.C | D.D |
四、多选题 添加题型下试题

| A.反应过程中,S、O和Fe的化合价发生了变化 |
| B.理论上每生成16gS,需补充200g Fe2(SO4)3 |
| C.理论上每生成32gS,同时有16gO2参与反应 |
| D.理论上反应Ⅱ中每生成18gH2O,同时消耗152 g FeSO4 |
【知识点】 不含杂质的化学方程式计算解读 化合价代数和的计算与应用解读
五、填空与简答 添加题型下试题
(1)故人西辞黄鹤楼,烟花三月下扬州。一唐·李白


①孟浩然“下扬州”的交通工具是木船。现代游船常用玻璃钢制造船体,玻璃钢属于
②现代人远行可乘坐飞机。铝锂合金材料大量运用于国产C919大飞机的制造,下列不属于铝锂合金性质的是
A.密度大 B.硬度大 C.抗腐蚀
③汽车是重要的陆路交通工具。燃油车辆须加装尾气催化净化装置,该装置将尾气中的CO和NO转化成CO2和一种无污染的气体,发生反应的化学方程式是
(2)天下三分明月夜,二分无赖是扬州。一唐·徐凝
①空气质量影响人们观赏明月。空气属于
②下列做法不利于改善空气质量的是
A.风力发电 B.徒步出行 C.垃圾露天焚烧
③煤的气化和液化可实现能源清洁化,改善空气质量。水煤气中CO和H2在高温、高压和催化剂条件下合成甲醇(CH4O),该反应的化学方程式是
(3)前日扬州去,酒熟美蟹蜊。一宋·梅尧臣

①蟹肉鲜美,富含蛋白质。蛋白质水溶液在加热时会生成沉淀,此沉淀
②各种酒中都含有乙醇(C2H6O)。在酿酒过程中,粮食中的
③下列食品中富含维生素C的是
A.盐水鹅 B.西红柿 C.大虾
(1)实验室用NaCl固体配制50g15%NaCl溶液。
①使用托盘天平称取
②溶解过程中需要用到的玻璃仪器有烧杯、量筒、胶头滴管和
(2)大多数天然淡水需要经过处理方可直接饮用。
①工厂锅炉长期使用会形成水垢,可用盐酸去除。写出水垢中Mg2(OH)2CO3溶于盐酸时发生反应的化学方程式
②某家用净水机工作原理如下图所示:
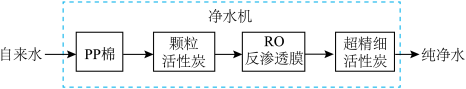
净水机中,PP棉净水原理是
(3)扬州积极推进水环境整治,建设“秀美瘦西湖,文明新扬州”。
①环保部门对水质进行长期监测,将水质从“优”到 “劣”分为Ⅰ~V类。由如图可知,近年来扬州市Ⅱ~Ⅲ类优良水质百分比明显呈

②产生这种变化趋势的原因可能是
A.夜间排放工业污水
B.清理污染河道的淤泥
C.关停或整改存在污染隐患的企业
(4)污水未经处理直接排入河流,会使水面上藻类物质大量繁殖,水质恶化。某藻类含化学式为 C106H263O106N16P的物质,则污水中导致藻类生长过快的营养元素是
【知识点】 化学方程式的书写解读 活性炭的吸附性 固体配制一定质量分数溶液解读
六、实验题 添加题型下试题
(1)实验室用如图所示的装置制取少量氧气。
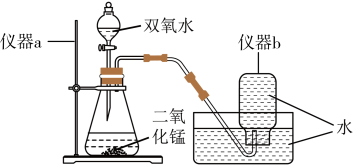
①仪器a、仪器b的名称分别是
②锥形瓶内发生反应的化学方程式是
(2)工业上有多种制取氧气的方法,如:
方法一:在低温、加压条件下,将空气液化。然后将温度升高至-196℃~-183℃之间,使液态氮气先蒸发,剩余液态氧气储存于钢瓶里。
方法二:利用电解水的方法制取氧气,将得到的氧气干燥。在低温、加压条件下,使之转化为液态,储存于钢瓶里。
①从构成物质的微粒视角分析,在方法一空气液化过程中,主要改变的是
②某工厂用方法二制取氧气,发现氧气的产量略小于理论值,且所得氧气中有淡淡的鱼腥气味。从元素守恒角度分析,该鱼腥气味的气体是
(3)氢气和氧气在Pd基催化剂表面可反应生成H2O2,其微观示意图如下:

“解离”时,结构被破坏的分子是
(4)为探究双氧水的分解,进行以下两个实验:
①氯化物对双氧水分解的影响。
反应条件:6.0mL30%双氧水,0.1g氯化物,室温;实验时间:1.5h。
实验数据如下表所示:
| 氯化物 | NaCl | MgCl2 | CuCl2 |
| 放出氧气的体积/mL | 2.0 | 4.0 | 420.0 |
| 双氧水的分解率/% | 0.30 | 0.60 | 63.18 |
②pH对双氧水分解的影响。
反应条件:6.0mL30%双氧水,60℃;用NaOH溶液调pH;实验时间:1.5h。实验结果如图所示:

由如图可知,pH为
(5)用双氧水可制得“鱼浮灵”、“钙多宝”。
①“鱼浮灵”主要成分是2Na2CO3·3H2O2,可迅速增加水体含氧量,其原因是
②“钙多宝”主要成分是CaO2,常温下能与水反应生成氢氧化钙和氧气。长时间存放的过氧化钙中含有主要杂质是
七、综合应用题 添加题型下试题
(1)“西气东输”工程利于国家能源和产业结构调整,极大改善了沿线居民生活质量。
①为防止传输天然气的钢管被腐蚀,可采取的措施有
②CH4完全燃烧的化学方程式是
③天然气的使用可有效减少酸雨形成。下列现象与酸雨有关的是
A.石刻文物被腐蚀 B.全球海平面上升
(2)工业上以CH4为原料生产H2,制取原理如下图所示:
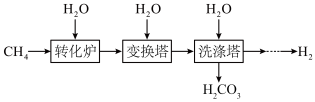
已知变换塔、洗涤塔发生的主要反应依次是:
 ,
,
①“转化炉”中有H2产生,参加反应的CH4与H2O的质量比

②“洗涤塔”中气体从塔底通入,水从塔顶喷淋。这样操作的优点是
③若有32gCH4参与反应(假设各步反应都完全转化),理论上可制得
(3)我国是世界上首个成功试采海域可燃冰的国家。可燃冰是CH4被H2O分子形成的笼包裹,在海底低温和高压作用下形成的结晶物质。

①可燃冰样品常存放于液氮储存罐中,其原因是
②可燃冰有多种结构,某H型可燃冰的化学式为CH4·9H2O,分析其结构发现:平均34个H2O分子构成6个笼,每个笼只容纳一个CH4或H2O分子,这6个笼内容纳的CH4与H2O分子个数比是
八、填空与简答 添加题型下试题
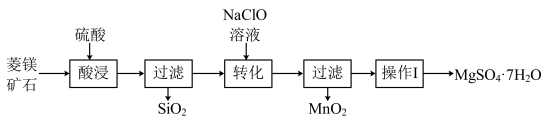
(2)“转化”时主要反应是
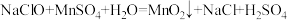 ,氯元素反应前后化合价变化情况是
,氯元素反应前后化合价变化情况是(3)硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
| 温度/℃ | -3.9-1.8 | 1.8-48.1 | 48.1-67.5 | 67.5-200 |
| 析出晶体 | MgSO4·12H2O | MgSO4·7H2O | MgSO4·6H2O | MgSO4·H2O等 |
②“操作1”所得滤液中能分离出一种可循环使用的物质,该物质是
(4)已知:MgSO4·7H2O中镁元素质量分数为9.76%,采用热分析法测定所得MgSO4·7H2O样品中镁元素质量分数:
①未加热前,测得样品中镁元素质量分数略大于9.76%,可能的原因是
②高于900℃后,测得剩余固体中镁元素质量分数大于20%,可能的原因是
(5)若用100t菱镁矿石可制得246 t MgSO4·7H2O产品,忽略反应过程中镁元素损失,求该菱镁矿石中MgCO3的质量分数。(写出计算过程)
试卷分析
试卷题型(共 25题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 人体内的常量元素 人体内的微量元素——碘、铁元素 | 单选题 |
| 2 | 0.85 | 化学变化与物理变化判断 | 单选题 |
| 3 | 0.65 | 物质化学性质的决定因素 | 单选题 |
| 4 | 0.65 | 酸的定义 碱的定义 盐的定义 氧化物的定义 | 单选题 |
| 5 | 0.94 | 金属的物理通性与用途 | 单选题 |
| 6 | 0.65 | 与爆炸和燃烧有关图标的辨认 | 单选题 |
| 7 | 0.65 | 根据方程式推测化学式 | 单选题 |
| 8 | 0.65 | 常见酸、碱的俗称及化学式 常见盐的俗名、用途 | 单选题 |
| 9 | 0.94 | 溶液酸碱性及pH相关关系 | 单选题 |
| 10 | 0.85 | 化合反应 | 单选题 |
| 11 | 0.94 | 化学式、分子式及涵义 根据化学式计算元素质量分数 | 单选题 |
| 12 | 0.85 | 二氧化碳对生活环境的影响 自然界碳循环 化石燃料的形成及现状 | 单选题 |
| 13 | 0.65 | 氯化钠 | 单选题 |
| 14 | 0.94 | 微粒图像的分析及应用 | 单选题 |
| 15 | 0.4 | 含杂质的化学方程式计算 化学方程式与实验的计算 | 单选题 |
| 16 | 0.65 | 空气中各成分的用途 金属的物理通性与用途 常见几种酸的用途 生石灰的性质及用途 | 单选题 |
| 17 | 0.85 | 溶液的酸碱性的判断与pH的测定 制备氢气实验的探究 量筒的正确使用方法和注意事项 | 单选题 |
| 19 | 0.65 | 一氧化碳的还原性 金属活动顺序理解和判断 常见的酸碱指示剂及其变色情况 无明显现象的中和反应的判断 | 单选题 |
| 二、多选题 | |||
| 18 | 0.65 | 饱和溶液和不饱和溶液的转换 固体溶解度曲线的应用 | |
| 20 | 0.4 | 不含杂质的化学方程式计算 化合价代数和的计算与应用 | |
| 三、填空与简答 | |||
| 21 | 0.65 | 用质量守恒定律确定物质组成 维生素的来源 常见物品质材的辨别 空气污染及其保护 | 填空题 |
| 22 | 0.4 | 化学方程式的书写 活性炭的吸附性 固体配制一定质量分数溶液 | 填空题 |
| 25 | 0.4 | 有关质量守恒定律的计算 化学方程式的书写 结晶分离混合物 盐类参与的反应 | 流程题 |
| 四、实验题 | |||
| 23 | 0.4 | 过氧化氢制取氧气实验 溶液酸碱性及pH相关关系 碳酸氢钠、碳酸钠、碳酸钙 气体制备实验的反应条件的控制 | |
| 五、综合应用题 | |||
| 24 | 0.4 | 资源综合利用和新能源开发的重要意义 常见几种燃料使用对环境的影响 甲烷的燃烧 | |