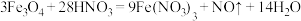根据信息和要求书写相关反应的方程式
(1)用84消毒液对新冠病毒进行消杀。将 通入NaOH溶液制备84消毒液,写出反应的离子方程式
通入NaOH溶液制备84消毒液,写出反应的离子方程式___________ 。
(2) 与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:_____ 。

(3)以 为原料可在加热熔融条件下制取
为原料可在加热熔融条件下制取 。该反应中包含的所有物质有
。该反应中包含的所有物质有 、
、 、KCl、KOH、
、KCl、KOH、 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
(4)向 溶液中逐滴加入
溶液中逐滴加入 溶液至沉淀完全,写出发生反应的离子方程式:
溶液至沉淀完全,写出发生反应的离子方程式:___________ 。
(1)用84消毒液对新冠病毒进行消杀。将
 通入NaOH溶液制备84消毒液,写出反应的离子方程式
通入NaOH溶液制备84消毒液,写出反应的离子方程式(2)
 与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
(3)以
 为原料可在加热熔融条件下制取
为原料可在加热熔融条件下制取 。该反应中包含的所有物质有
。该反应中包含的所有物质有 、
、 、KCl、KOH、
、KCl、KOH、 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式(4)向
 溶液中逐滴加入
溶液中逐滴加入 溶液至沉淀完全,写出发生反应的离子方程式:
溶液至沉淀完全,写出发生反应的离子方程式:
更新时间:2024-01-01 17:14:51
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】将下列化学方程式改写成离子方程式。
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑___________________________________ ;
(2)2Al+2NaOH+2H2O=2NaAlO2+3H2↑___________________________________ ;
(3)Fe+2HCl=FeCl2+H2↑___________________________________ ;
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑
(2)2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(3)Fe+2HCl=FeCl2+H2↑
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求书写化学方程式或离子方程式。
(1)氢氧化铜与盐酸反应的离子方程式:___________
(2)硝酸钙与碳酸钠反应的离子方程式:___________
(3)2H++CO =CO2↑+H2O对应的化学方程式:
=CO2↑+H2O对应的化学方程式:___________
(4)H++OH-=H2O对应的化学方程式:___________
(5)Ba2++SO =BaSO4↓对应的化学方程式:
=BaSO4↓对应的化学方程式:___________
(1)氢氧化铜与盐酸反应的离子方程式:
(2)硝酸钙与碳酸钠反应的离子方程式:
(3)2H++CO
 =CO2↑+H2O对应的化学方程式:
=CO2↑+H2O对应的化学方程式:(4)H++OH-=H2O对应的化学方程式:
(5)Ba2++SO
 =BaSO4↓对应的化学方程式:
=BaSO4↓对应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图为氯及其化合物的“价—类”二维图。

(1)某同学利用以下试剂研究HCl性质,进行了如下预测:从物质类别上看,HCl属于酸,可能与_______ 发生反应(填序号);从化合价角度看,Cl-具有还原性,可能与_______ 发生反应(填序号)。
a.NaClOb.Fec.NaOHd.KMnO4e.AgNO3
(2)某工厂用NaCl溶液制备氯气,其化学原理为如下反应:
 H2O+
H2O+ NaCl
NaCl Cl2+
Cl2+ NaOH+
NaOH+
请将上述方程式补充完整,并用单线桥表示电子转移_______ 。

(1)某同学利用以下试剂研究HCl性质,进行了如下预测:从物质类别上看,HCl属于酸,可能与
a.NaClOb.Fec.NaOHd.KMnO4e.AgNO3
(2)某工厂用NaCl溶液制备氯气,其化学原理为如下反应:
 H2O+
H2O+ NaCl
NaCl Cl2+
Cl2+ NaOH+
NaOH+
请将上述方程式补充完整,并用单线桥表示电子转移
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)某反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O、H2S是反应物之一,试回答下列问题。
①在上述反应中,表现出氧化性的物质是__ ,__ 是氧化产物。
②写出该反应的化学方程式:__ 。
(2)根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题。
①氧化剂与还原剂的质量之比为__ 。
②当生成56 g N2时,电子转移的物质的量为__ 。
(1)某反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O、H2S是反应物之一,试回答下列问题。
①在上述反应中,表现出氧化性的物质是
②写出该反应的化学方程式:
(2)根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题。
①氧化剂与还原剂的质量之比为
②当生成56 g N2时,电子转移的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】H2O2是重要的化学试剂,在实验室和实际生产中应用广泛。
(1)H2O2有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:______________ 。
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在___________ (填“酸式”或“碱式”)滴定管中,判断到达滴定终点的现象是___________ 。
(2)①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:___________ 。
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是___________ 。
③利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥Cr(Ⅲ)的处理工艺流程如图:
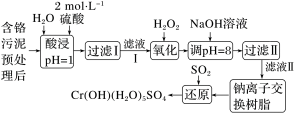
已知:硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。H2O2的作用是将滤液Ⅰ中的Cr3+转化为 ,写出此反应的离子方程式:
,写出此反应的离子方程式: ___________ 。
(3)H2O2是一种二元弱酸,写出其第一步电离的方程式:___________ ,它与过量的Ba(OH)2反应的化学方程式为________________ 。
(1)H2O2有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在
(2)①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是
③利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥Cr(Ⅲ)的处理工艺流程如图:

已知:硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。H2O2的作用是将滤液Ⅰ中的Cr3+转化为
 ,写出此反应的离子方程式:
,写出此反应的离子方程式: (3)H2O2是一种二元弱酸,写出其第一步电离的方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】将一定量的 通入体积为40mL的氢氧化钾溶液中,两者恰好完全反应,测得反应后溶液中有三种含氯元素的离子,其中
通入体积为40mL的氢氧化钾溶液中,两者恰好完全反应,测得反应后溶液中有三种含氯元素的离子,其中 的物质的量为0.06mol,
的物质的量为0.06mol, 的物质的量为0.03mol,请按要求回答下列问题。
的物质的量为0.03mol,请按要求回答下列问题。
(1)该反应的化学方程式为________________________________________________ 。
(2)该反应中,氧化剂与还原剂的物质的量之比为____________ 。
(3)上述反应中,通入 的物质的量为
的物质的量为____________ mol,氢氧化钾溶液的物质的量浓度为__________
mol/L。
 通入体积为40mL的氢氧化钾溶液中,两者恰好完全反应,测得反应后溶液中有三种含氯元素的离子,其中
通入体积为40mL的氢氧化钾溶液中,两者恰好完全反应,测得反应后溶液中有三种含氯元素的离子,其中 的物质的量为0.06mol,
的物质的量为0.06mol, 的物质的量为0.03mol,请按要求回答下列问题。
的物质的量为0.03mol,请按要求回答下列问题。(1)该反应的化学方程式为
(2)该反应中,氧化剂与还原剂的物质的量之比为
(3)上述反应中,通入
 的物质的量为
的物质的量为mol/L。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)工业上将氯气溶于一定浓度的氢氧化钠溶液可制得“84消毒液”,用电子式表示“84消毒液”的有效成分是__________ 。
(2)二氧化氯(ClO2)是一种黄绿色易溶于水的气体,也可用于自来水的杀菌消毒。工业上常用NaClO3和Na2SO3溶液混合并加入稀H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为______________ 。
(1)工业上将氯气溶于一定浓度的氢氧化钠溶液可制得“84消毒液”,用电子式表示“84消毒液”的有效成分是
(2)二氧化氯(ClO2)是一种黄绿色易溶于水的气体,也可用于自来水的杀菌消毒。工业上常用NaClO3和Na2SO3溶液混合并加入稀H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】疫情期间,环境消毒是极其关键的,常常喷洒“84”消毒液,其有效成分为NaClO。已知某“84”消毒液瓶体部分标签如图所示。请回答下列问题:

(1)Cl2是制取“84”消毒液的主要原料之一,请写出实验室用MnO2制Cl2的化学方程式:__ ,工业上将Cl2通入NaOH溶液中可制得“84”消毒液,请写出该反应的化学方程式:__ 。
(2)该同学参阅该“84”消毒液的配方,欲用NaClO固体配制480mL此消毒液。

①配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、__ 。
②关于配制过程的说法正确的是__ (填字母)。
A.容量瓶用蒸馏水洗净后,必须烘干后才能用于溶液配制
B..配制过程中,未用蒸馏水洗涤烧杯和玻璃棒会导致结果偏低
C.需要称量NaClO固体的质量为148.8g
D.将称量NaClO固体完全溶于水后,直接将溶液转移至如图仪器中
E.按如图所示转移烧杯中的溶液,对所配溶液浓度无影响
F.定容时,俯视观察刻度线可能导致结果偏高
G.称量时,所使用的砝码有残缺可能导致结果偏高
(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是盐酸)与“84”消毒液而发生氯气中毒事件。请用离子方程式解释原因:__ 。
(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。在此过程中H2O2表现了__ (填“氧化性”或“还原性”),当有0.1molO2生成时,转移电子__ mol。

(1)Cl2是制取“84”消毒液的主要原料之一,请写出实验室用MnO2制Cl2的化学方程式:
(2)该同学参阅该“84”消毒液的配方,欲用NaClO固体配制480mL此消毒液。

①配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、
②关于配制过程的说法正确的是
A.容量瓶用蒸馏水洗净后,必须烘干后才能用于溶液配制
B..配制过程中,未用蒸馏水洗涤烧杯和玻璃棒会导致结果偏低
C.需要称量NaClO固体的质量为148.8g
D.将称量NaClO固体完全溶于水后,直接将溶液转移至如图仪器中
E.按如图所示转移烧杯中的溶液,对所配溶液浓度无影响
F.定容时,俯视观察刻度线可能导致结果偏高
G.称量时,所使用的砝码有残缺可能导致结果偏高
(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是盐酸)与“84”消毒液而发生氯气中毒事件。请用离子方程式解释原因:
(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。在此过程中H2O2表现了
您最近一年使用:0次

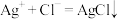 所对应的化学方程式:
所对应的化学方程式: