目前从海水提溴(Br2)大致有以下步骤。
(1)向浓缩的海水中通入某种气体,将海水中的Br﹣氧化为Br2,该气体是___ 。
(2)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3、1molBr2需消耗Na2CO3___ mol。
(3)再将所得混合溶液用稀硫酸酸化,得到浓度较高的溴水,配平该反应的离子方程式。
__ Br﹣+__ BrO3﹣+__ H+→___ Br2+___ H2O。
(1)向浓缩的海水中通入某种气体,将海水中的Br﹣氧化为Br2,该气体是
(2)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3、1molBr2需消耗Na2CO3
(3)再将所得混合溶液用稀硫酸酸化,得到浓度较高的溴水,配平该反应的离子方程式。
更新时间:2019-11-19 11:56:50
|
相似题推荐
填空题
|
容易
(0.94)
解题方法
【推荐1】 与热的
与热的 溶液反应生成
溶液反应生成 的离子方程式为
的离子方程式为_______ 。
 与热的
与热的 溶液反应生成
溶液反应生成 的离子方程式为
的离子方程式为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】H2O2是一种重要的化学品,其合成方法不断发展。
早期制备方法:Ba(NO3)2 BaO
BaO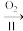 BaO2
BaO2
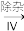 滤液
滤液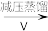 H2O2
H2O2
I为分解反应,产物除BaO、O2外,还有一种红棕色气体。该反应的化学方程式是____ 。
早期制备方法:Ba(NO3)2
 BaO
BaO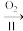 BaO2
BaO2
 滤液
滤液 H2O2
H2O2I为分解反应,产物除BaO、O2外,还有一种红棕色气体。该反应的化学方程式是
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】工业用盐中含亚硝酸钠(NaNO2),该物质有毒,不能用作食盐用于烹调。
(1)食盐主要成分的化学式为____ 。
(2)亚硝酸钠和食盐中都含有的离子的化学符号是____ 。
(3)亚硝酸钠与氯化铵共热能发生反应,其化学方程式为:NaNO2+NH4Cl NaCl+X↑+2H2O,则X的化学式为
NaCl+X↑+2H2O,则X的化学式为____ 。该化学方程式里的含氮物质中,氮元素未表现出的化合价为____ 价(填序号)。
A.+3 B.-3 C.0 D.+5
(1)食盐主要成分的化学式为
(2)亚硝酸钠和食盐中都含有的离子的化学符号是
(3)亚硝酸钠与氯化铵共热能发生反应,其化学方程式为:NaNO2+NH4Cl
 NaCl+X↑+2H2O,则X的化学式为
NaCl+X↑+2H2O,则X的化学式为A.+3 B.-3 C.0 D.+5
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】氧化还原反应在生产生活中普遍存在。
(1)工业上制取 Cl2的原理为:2NaCl + 2H2O 2NaOH + H2↑+ Cl2↑。当收集到标准状况下224 mL H2时,生成的 NaOH 为
2NaOH + H2↑+ Cl2↑。当收集到标准状况下224 mL H2时,生成的 NaOH 为_______ g,转移的电子为_______ mol。
(2)工业上制取ClO2的某一原理为: 。该反应中,氧化剂与还原剂的物质的量之比为
。该反应中,氧化剂与还原剂的物质的量之比为_______ 。ClO2作饮用水消毒剂是利用其_______ (填“氧化”或“还原”)性。
(1)工业上制取 Cl2的原理为:2NaCl + 2H2O
 2NaOH + H2↑+ Cl2↑。当收集到标准状况下224 mL H2时,生成的 NaOH 为
2NaOH + H2↑+ Cl2↑。当收集到标准状况下224 mL H2时,生成的 NaOH 为(2)工业上制取ClO2的某一原理为:
 。该反应中,氧化剂与还原剂的物质的量之比为
。该反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
已知:①海水中溴元素(以Br-表示)的浓度0.068g/L;
②Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。

(1)请写出一种海水淡化的方法:_____________ 。
(2)海水中溴离子的物质的量浓度为__________________ 。
(3)步骤Ⅰ中已获得低溶度的含Br2溶液,步骤Ⅱ中又将Br2还原为Br-,步骤Ⅲ又得到Br2,其目的为________________ 。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_________________________________________________ 。
(5)工业溴提纯可用蒸馏法,蒸馏时加热方法最好采用_______________ ,蒸馏装置中仪器连接均不能用橡胶塞和橡胶管,其原因是_________________________________ 。
已知:①海水中溴元素(以Br-表示)的浓度0.068g/L;
②Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。

(1)请写出一种海水淡化的方法:
(2)海水中溴离子的物质的量浓度为
(3)步骤Ⅰ中已获得低溶度的含Br2溶液,步骤Ⅱ中又将Br2还原为Br-,步骤Ⅲ又得到Br2,其目的为
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为
(5)工业溴提纯可用蒸馏法,蒸馏时加热方法最好采用
您最近一年使用:0次
【推荐2】世界上绝大部分卤素都存在于海洋。海水呈微碱性,海水晒盐可以得到粗盐和卤水,对粗盐和卤水进一步加工可以得到氯气、溴以及其他一些重要的化工产品。
二氧化氯(ClO2)可以除去工业污水中的氰化物,反应的离子方程式为:2CIO2+2CN-→2CO2↑+N2↑+2Cl-
(1)氯的另一种氧化物Cl2O每个原子都达到8电子稳定结构,它的电子式为___________ 。
(2)另一种处理含氰化物污水的方法是电解法,分析判断CN-是在________ 极上(选填编号:①阴;②阳)被反应成CO2和N2。
(3)工业上从卤水获取溴,涉及到“氧化”、“提取”等步骤。“氧化”时先在卤水中加入硫酸酸化,然后再通入氯气,硫酸酸化可以提高氯气的利用率,原因是_________ 。用上述方法制得的液溴常溶有少量氯气,除去氯气的方法是__________ 。
二氧化氯(ClO2)可以除去工业污水中的氰化物,反应的离子方程式为:2CIO2+2CN-→2CO2↑+N2↑+2Cl-
(1)氯的另一种氧化物Cl2O每个原子都达到8电子稳定结构,它的电子式为
(2)另一种处理含氰化物污水的方法是电解法,分析判断CN-是在
(3)工业上从卤水获取溴,涉及到“氧化”、“提取”等步骤。“氧化”时先在卤水中加入硫酸酸化,然后再通入氯气,硫酸酸化可以提高氯气的利用率,原因是
您最近一年使用:0次

 所需要用的试剂
所需要用的试剂



