1 . 下列图示与对应的叙述相符或能达到相应目的的是
| |
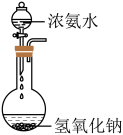
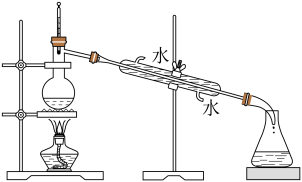
| A.实验室快速制氨气 | B.提纯苯甲酸 |
|
|
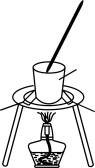
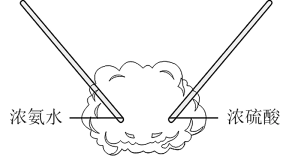
C.绿矾晶体制备 | D.浓氨水与浓硫酸反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 回答下列问题:
(1)某化学社团为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计了如下实验。
已知:溶液的导电性由溶液中离子的浓度及离子电荷数决定,可通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。实验装置如图所示:
(2)写出下列情况发生反应的离子方程式:向NaHSO4液中逐滴加入Ba(OH)2溶液至溶液显中性___________ 。
(3)某化工厂排出的废水呈酸性,且其中含大量的Na+、Cu2+、Cl-、 ,为除去废水样品中的Cu2+和
,为除去废水样品中的Cu2+和 ,最终得到中性溶液,设计的方案流程如下图:
,最终得到中性溶液,设计的方案流程如下图:___________ (用离子符号表示)。
②上述流程中,试剂c为___________ (写化学式)。
(1)某化学社团为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计了如下实验。
已知:溶液的导电性由溶液中离子的浓度及离子电荷数决定,可通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。实验装置如图所示:
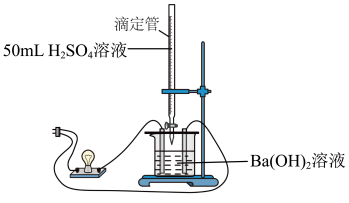
| 实验步骤 | 实验现象 | 实验结论 |
| 连接好装置,向烧杯中加入一定浓度的Ba(OH)2溶液,逐滴滴加H2SO4溶液直至过量,边滴边振荡 | Ba(OH)2溶液和H2SO4溶液的反应是离子反应 |
(2)写出下列情况发生反应的离子方程式:向NaHSO4液中逐滴加入Ba(OH)2溶液至溶液显中性
(3)某化工厂排出的废水呈酸性,且其中含大量的Na+、Cu2+、Cl-、
 ,为除去废水样品中的Cu2+和
,为除去废水样品中的Cu2+和 ,最终得到中性溶液,设计的方案流程如下图:
,最终得到中性溶液,设计的方案流程如下图: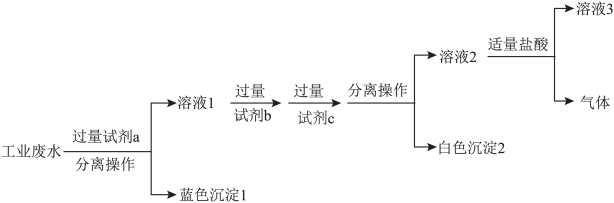
②上述流程中,试剂c为
您最近半年使用:0次
3 . 下列实验设计能够成功的是
A.除去粗盐中含有的硫酸钙杂质:粗盐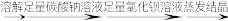 精盐 精盐 |
B.检验亚硫酸钠试样是否变质:试样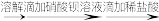 白色沉淀不溶解→试样已变质 白色沉淀不溶解→试样已变质 |
C.证明酸性条件H2O2的氧化性比I2强:NaI溶液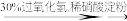 溶液变蓝色→氧化性:H2O2>I2 溶液变蓝色→氧化性:H2O2>I2 |
D.检验某溶液中是否含有Fe2+:试样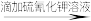 溶液颜色无变化 溶液颜色无变化 溶液变红色→溶液中含有Fe2+ 溶液变红色→溶液中含有Fe2+ |
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
4 . 下列能达到实验目的并且对装置或仪器的使用或操作规范的是
|
|
| A.用裂化汽油提纯溴水中的Br2 | B.用标准KMnO4溶液滴定未知浓度的FeSO4溶液 |
|
|
| C.蒸干溶液获得Cu(NO3)2固体 | D.灼烧海带灰 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
5 . 碲被誉为金属性最强的非金属,某科研小组从碲渣(主要含有Cu2Te )中提取粗碲的工艺流程如图所示。下列有关说法错误的是
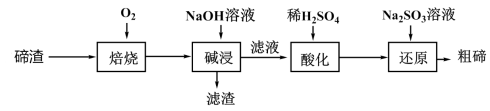
| A.“焙烧”后铜以Cu2O形式存在 |
| B.“碱浸”后过滤用到的主要仪器有:烧杯、漏斗、玻璃棒 |
| C.“酸化”后生成Te(SO4)2 |
| D.“还原”后,溶液的酸性减弱 |
您最近半年使用:0次
解题方法
6 . 除去下列物质中的杂质(括号中的物质为杂质),所选除杂试剂和分离方法均正确的是
| 选项 | 被提纯的物质(杂质) | 除杂试剂 | 分离方法 |
| A |  溶液( 溶液( ) ) | 四氯化碳 | 萃取、分液 |
| B |  (小苏打) (小苏打) | 蒸馏水 | 重结晶 |
| C |  溶液( 溶液( ) ) | 过量铜粉 | 过滤 |
| D | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
7 . 某粗苯甲酸样品中含有少量 和泥沙,某实验小组提纯苯甲酸的实验流程如图(已知:常温下,苯甲酸微溶于水,易溶于乙醇;
和泥沙,某实验小组提纯苯甲酸的实验流程如图(已知:常温下,苯甲酸微溶于水,易溶于乙醇; 和
和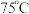 时苯甲酸在水中的溶解度分别为
时苯甲酸在水中的溶解度分别为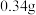 和
和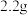 )。下列说法不正确的是
)。下列说法不正确的是
 和泥沙,某实验小组提纯苯甲酸的实验流程如图(已知:常温下,苯甲酸微溶于水,易溶于乙醇;
和泥沙,某实验小组提纯苯甲酸的实验流程如图(已知:常温下,苯甲酸微溶于水,易溶于乙醇; 和
和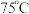 时苯甲酸在水中的溶解度分别为
时苯甲酸在水中的溶解度分别为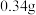 和
和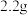 )。下列说法不正确的是
)。下列说法不正确的是
| A.“过滤1”需趁热,以减少苯甲酸的析出 | B.为除去 ,“结晶”时应采用蒸发结晶 ,“结晶”时应采用蒸发结晶 |
| C.“洗涤”时,不宜用乙醇作洗涤剂 | D.可通过酸碱中和滴定测定所得苯甲酸晶体的纯度 |
您最近半年使用:0次
8 . 下列说法正确的是
| A.除去乙烷中的少量乙烯,在催化剂条件下向混合气体中通入氢气 |
| B.用酸性高锰酸钾溶液可鉴别苯和环己烷 |
| C.分液时,下层液体从下口放出,继续放出上层溶液于另一烧杯 |
| D.在苯甲酸重结晶实验中,趁热过滤的目的是除去泥沙、减少苯甲酸的析出 |
您最近半年使用:0次
9 . 下列实验处理可行的有几项
①将CH3CH(OH)CHO与NaOH的醇溶液共热制备CH3CH=CH2
②向丙烯醛(CH2=CHCHO)中加入溴水,观察橙色褪去,能证明结构中存在碳碳双键
③实验时手指不小心沾上苯酚,立即用乙醇冲洗,再用水冲洗
④用溴水除去混在苯中的己烯,分液得到纯净的苯
⑤利用重结晶法可以提纯含有少量NaCl的苯甲酸
⑥在分别盛有少量苯和四氯化碳的试管中加碘水后振荡,可根据现象区分苯和四氯化碳
⑦向含有苯酚的苯中加入碳酸钠溶液,反应后分液,可除去苯中的少量苯酚
⑧用碳酸钠溶液可区分乙醇、甲苯、乙酸、溴乙烷和苯
⑨煤油的主要成分为烃类物质,可用来保存金属钠
①将CH3CH(OH)CHO与NaOH的醇溶液共热制备CH3CH=CH2
②向丙烯醛(CH2=CHCHO)中加入溴水,观察橙色褪去,能证明结构中存在碳碳双键
③实验时手指不小心沾上苯酚,立即用乙醇冲洗,再用水冲洗
④用溴水除去混在苯中的己烯,分液得到纯净的苯
⑤利用重结晶法可以提纯含有少量NaCl的苯甲酸
⑥在分别盛有少量苯和四氯化碳的试管中加碘水后振荡,可根据现象区分苯和四氯化碳
⑦向含有苯酚的苯中加入碳酸钠溶液,反应后分液,可除去苯中的少量苯酚
⑧用碳酸钠溶液可区分乙醇、甲苯、乙酸、溴乙烷和苯
⑨煤油的主要成分为烃类物质,可用来保存金属钠
| A.3 | B.4 | C.5 | D.6 |
您最近半年使用:0次
10 . 为了除去粗盐中含有的CaCl2、MgCl2、Na2SO4及泥沙等杂质,将粗盐溶于水,进行下列操作:①加入适量盐酸;②加入BaCl2溶液;③过滤;④加入NaOH溶液;⑤加入Na2CO3溶液.下列说法错误的是
| A.为了保证杂质除尽,每次加入的试剂应该稍稍过量 |
| B.操作顺序可以是②④⑤③①或④②⑤③①或⑤②④①③ |
| C.实验过程中各步骤产生的沉淀不需要多次过滤 |
| D.加入适量盐酸的目的是除去滤液中的NaOH和Na2CO3 |
您最近半年使用:0次