解题方法
1 . 某学习小组用MnO2与浓盐酸混合共热制备氯气。
(1)写出该反应的离子方程式:_______ ,基态锰原子的价电子排布式为_______ 。
(2)为净化与收集Cl2,选用如图所示的部分装置进行实验,装置的接口连接顺序为_______ 。
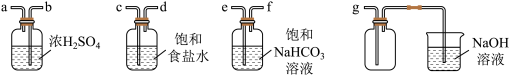
(3)当Cl2不再生成时,反应容器中仍存在MnO2和盐酸,该小组对不再产生Cl2的原因进行以下实验探究。
【查阅资料】物质氧化性和还原性变化的一般规律是:还原反应中,增天反应物浓度或降低生成物浓度,氧化剂的氧化性增强;氧化反应中,增大发应物浓度或降低生成物浓度,还原剂的还原性增强。
【提出猜想】
猜想a:在此反应中,随H+浓度降低,①_______ (填氧化剂化学式)氧化性减弱
猜想b:在此反应中,随②_______ 浓度降低,还原剂还原性减弱。
猜想c:在此反应中,随Mn2+浓度升高,氧化剂氧化性减弱。
【设计实验、验证猜想】向反应后的固液混合物中加入试剂,观条并记录有无氯气生成(Na+对各物质的氧化性与还原性均无影响)。
【数据分析、得出结论】猜想a、猜想b和猜想c均正确。
【迁移应用】25℃时,Ksp(AgI)=8.51×10-17。一般情况下,在金属活动性顺序里,位于氢前面的金属能置换出酸中的氢,资料显示Ag也可以与HI发生置换反应生成H,可能的原因是④_______ 。
(1)写出该反应的离子方程式:
(2)为净化与收集Cl2,选用如图所示的部分装置进行实验,装置的接口连接顺序为

(3)当Cl2不再生成时,反应容器中仍存在MnO2和盐酸,该小组对不再产生Cl2的原因进行以下实验探究。
【查阅资料】物质氧化性和还原性变化的一般规律是:还原反应中,增天反应物浓度或降低生成物浓度,氧化剂的氧化性增强;氧化反应中,增大发应物浓度或降低生成物浓度,还原剂的还原性增强。
【提出猜想】
猜想a:在此反应中,随H+浓度降低,①
猜想b:在此反应中,随②
猜想c:在此反应中,随Mn2+浓度升高,氧化剂氧化性减弱。
【设计实验、验证猜想】向反应后的固液混合物中加入试剂,观条并记录有无氯气生成(Na+对各物质的氧化性与还原性均无影响)。
| 实验序号 | 操作 | 有无氯气生成 |
| 1 | 加入较浓硫酸,使c(H+)=amol·L-1,c( )=bmol・L-1 )=bmol・L-1 | 有氯气 |
| 2 | 加入NaCl固体,使c(Cl-)=cmol·L-1 | 有氯气 |
| 3 | ③ | 无氯气 |
【迁移应用】25℃时,Ksp(AgI)=8.51×10-17。一般情况下,在金属活动性顺序里,位于氢前面的金属能置换出酸中的氢,资料显示Ag也可以与HI发生置换反应生成H,可能的原因是④
您最近一年使用:0次
2 . 海淀黄庄某中学化学小组为探究 的性质,进行了下列实验。
的性质,进行了下列实验。
[实验一]探究 的还原性,波波做了下列实验:
的还原性,波波做了下列实验:
(1)对比实验ⅰ与ⅱ,关于盐酸的作用,珊珊提出两个假设:
假设一:c(H+)增大,提高了 的氧化性或
的氧化性或 的还原性;
的还原性;
假设二: c(Cl-)增大,降低了还原产物的浓度,提高了 的氧化性。
的氧化性。
小雨设计实验方案,确认假设一不正确,实验方案是_______ 。
睿睿查阅资料: (白色沉淀)
(白色沉淀)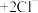 。
。
设计实验方案,确认了假设二正确,实验方案是_______ 。
(2)写出ⅱ中反应的离子方程式_______ 。
(3)对比实验ⅱ与ⅲ,针对反应速率的差异,进行了以下探究:
瑛瑛进行理论预测:依据_______ 反应(写离子方程式),氧化性: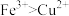 ,ⅲ的反应速率快于ⅱ的。
,ⅲ的反应速率快于ⅱ的。
萌萌查阅资料: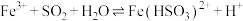 。
。
结合资料,解释实验ⅱ与ⅲ的速率差异_______ 。
[实验二]探究 的氧化性,邹邹做了下列实验:
的氧化性,邹邹做了下列实验:
(4)博博借助仪器检验黑色沉淀是 ,溶液中没有
,溶液中没有 。写出ⅴ中反应的离子方程式
。写出ⅴ中反应的离子方程式_______ 。
(5)反应ⅴ能发生,可能是因为Cu2S的生成提高了Cu的还原性或 的氧化性,
的氧化性, 的生成提高了Cu的还原性。对比实验ⅳ、ⅴ与ⅵ,昊昊得出结论:起主要作用的是
的生成提高了Cu的还原性。对比实验ⅳ、ⅴ与ⅵ,昊昊得出结论:起主要作用的是_______ 。
通过以上实验, 既有氧化性又有还原性,条件改变会影响其性质。
既有氧化性又有还原性,条件改变会影响其性质。
 的性质,进行了下列实验。
的性质,进行了下列实验。[实验一]探究
 的还原性,波波做了下列实验:
的还原性,波波做了下列实验:| 实验 | ⅰ | ⅱ | ⅲ |
| 实验操作 | 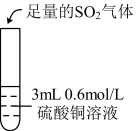 |  | 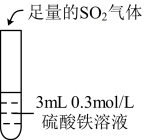 |
| 实验现象 | 无明显现象 | 通入 后溶液迅速变为棕色 后溶液迅速变为棕色 | 溶液迅速变成红棕色。两天后,溶液变浅绿色 |
假设一:c(H+)增大,提高了
 的氧化性或
的氧化性或 的还原性;
的还原性;假设二: c(Cl-)增大,降低了还原产物的浓度,提高了
 的氧化性。
的氧化性。小雨设计实验方案,确认假设一不正确,实验方案是
睿睿查阅资料:
 (白色沉淀)
(白色沉淀)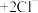 。
。设计实验方案,确认了假设二正确,实验方案是
(2)写出ⅱ中反应的离子方程式
(3)对比实验ⅱ与ⅲ,针对反应速率的差异,进行了以下探究:
瑛瑛进行理论预测:依据
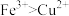 ,ⅲ的反应速率快于ⅱ的。
,ⅲ的反应速率快于ⅱ的。萌萌查阅资料:
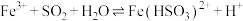 。
。结合资料,解释实验ⅱ与ⅲ的速率差异
[实验二]探究
 的氧化性,邹邹做了下列实验:
的氧化性,邹邹做了下列实验:| 实验 | ⅳ | ⅴ | ⅵ |
| 实验操作 | 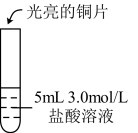 | 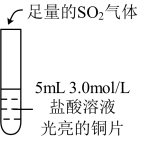 | 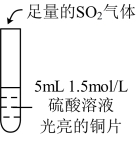 |
| 实验现象 | 无明显现象 | 光亮的紫红色铜片很快变暗,并有黑色沉淀生成,溶液变为棕色 | 无明显现象 |
 ,溶液中没有
,溶液中没有 。写出ⅴ中反应的离子方程式
。写出ⅴ中反应的离子方程式(5)反应ⅴ能发生,可能是因为Cu2S的生成提高了Cu的还原性或
 的氧化性,
的氧化性, 的生成提高了Cu的还原性。对比实验ⅳ、ⅴ与ⅵ,昊昊得出结论:起主要作用的是
的生成提高了Cu的还原性。对比实验ⅳ、ⅴ与ⅵ,昊昊得出结论:起主要作用的是通过以上实验,
 既有氧化性又有还原性,条件改变会影响其性质。
既有氧化性又有还原性,条件改变会影响其性质。
您最近一年使用:0次
2022-05-28更新
|
667次组卷
|
5卷引用:北京市中国人民大学附属中学2022届高三下学期第三次适应性练习化学试题
北京市中国人民大学附属中学2022届高三下学期第三次适应性练习化学试题(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)突破超重点 高效突破综合实验 实验4 创新探究实验热点1物质性质探究类实验(已下线)考点10 硫及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
解题方法
3 . 亚硝酸钠(NaNO2)有毒、有咸味,外形与食盐相似,人若误食会引起中毒。某兴趣小组欲研究亚硝酸钠,查阅资料得到如表信息。试根据信息回答下列问题:
(1)已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O,则该反应中氧化剂是 _______ ;若有0.75mol电子发生转移,则被氧化的还原剂的粒子数为 _______ (用NA表示阿伏加德罗常数的值)。
(2)人若误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列说法错误的是 _______(填序号)。
(3)下列方法中,可用来区分NaNO2和NaCl的是 _______ (填序号)。
A.焰色反应
B.滴加酸化的FeSO4溶液和KSCN溶液
C.在酸性条件下加入淀粉KI溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式_______ 。
| 药品 | NaNO2(亚硝酸钠) |
| 性质 | 在酸性溶液中有较强氧化性,能将Fe2+氧化成Fe3+。 |
(2)人若误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列说法错误的是 _______(填序号)。
| A.NaNO2被还原 |
| B.维生素C具有还原性 |
| C.还原性:维生素C>Fe2+ |
| D.NaNO2是还原剂 |
A.焰色反应
B.滴加酸化的FeSO4溶液和KSCN溶液
C.在酸性条件下加入淀粉KI溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式
您最近一年使用:0次
解题方法
4 . 氯气是一种重要的化工原料,大量用于制造盐酸、漂白剂、农药、染料和药品等。
Ⅰ.为探究氯气与 溶液的反应,某课外小组用下图装置进行实验(夹持仪器已略去)
溶液的反应,某课外小组用下图装置进行实验(夹持仪器已略去)
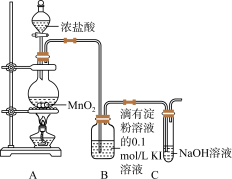
(1)装置A中生成氯气的化学反应方程式为___________ 。
(2)装置C中 的作用是
的作用是___________ 。
(3)能证明氯气的氧化性强于碘的实验现象是___________ 。
(4)为探究B中溶液颜色变化的原因,小组同学查阅资料并进行实验。
查阅资料: 和
和 在溶液中会发生反应:
在溶液中会发生反应: ,
, 显棕黄色且遇淀粉变蓝;
显棕黄色且遇淀粉变蓝; 可被氯气氧化为
可被氯气氧化为 (红色)和
(红色)和 (黄色),两种离子可继续被氧化成
(黄色),两种离子可继续被氧化成 (无色)。
(无色)。
进行实验:
①操作Ⅰ的实验目的是___________ 。
②写出 在水溶液中与氯气反应生成
在水溶液中与氯气反应生成 的离子方程式
的离子方程式___________ 。
③由以上实验可推断 中溶液颜色变成浅棕色的原因是
中溶液颜色变成浅棕色的原因是___________ 。
Ⅱ.84消毒液是一种常见的含氯消毒剂,其有效成分为次氯酸钠。
资料:84消毒液中含氯微粒主要有 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。某兴趣小组同学研究84消毒液的漂白性,实验如下。
;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。某兴趣小组同学研究84消毒液的漂白性,实验如下。
a.向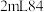 消毒液中加入
消毒液中加入 水后,放入红色纸片,观察到纸片慢慢褪色。
水后,放入红色纸片,观察到纸片慢慢褪色。
b.向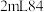 消毒液中加入
消毒液中加入 白醋后,放入红色纸片,观察到纸片迅速褪色。
白醋后,放入红色纸片,观察到纸片迅速褪色。
c.测得84消毒液在不同温度时ORP随时间的变化曲线如图。

(5)①已知白醋显酸性,不具有漂白性。实验a、b现象不同的原因是___________ 。
②由实验c可得出的结论是___________ 。
Ⅰ.为探究氯气与
 溶液的反应,某课外小组用下图装置进行实验(夹持仪器已略去)
溶液的反应,某课外小组用下图装置进行实验(夹持仪器已略去)
| 实验操作 | 实验现象 |
| 打开A中分液漏斗活塞,放下部分浓盐酸,加热 | 装置B中溶液变蓝色,随后蓝色褪去,溶液显浅棕色 |
(1)装置A中生成氯气的化学反应方程式为
(2)装置C中
 的作用是
的作用是(3)能证明氯气的氧化性强于碘的实验现象是
(4)为探究B中溶液颜色变化的原因,小组同学查阅资料并进行实验。
查阅资料:
 和
和 在溶液中会发生反应:
在溶液中会发生反应: ,
, 显棕黄色且遇淀粉变蓝;
显棕黄色且遇淀粉变蓝; 可被氯气氧化为
可被氯气氧化为 (红色)和
(红色)和 (黄色),两种离子可继续被氧化成
(黄色),两种离子可继续被氧化成 (无色)。
(无色)。进行实验:
| 实验操作 | 实验现象 |
Ⅰ.取反应后B中的溶液 分成两等份,第一份滴入1滴碘水;第二份滴入1滴淀粉溶液 分成两等份,第一份滴入1滴碘水;第二份滴入1滴淀粉溶液 | 第一份溶液变蓝色 第二份溶液颜色没有变化 |
Ⅱ.将 溶于 溶于 溶液中配制得碘总浓度为 溶液中配制得碘总浓度为 的溶液,取上述溶液 的溶液,取上述溶液 ,滴加1滴淀粉溶液,再通入氯气 ,滴加1滴淀粉溶液,再通入氯气 | 加淀粉后溶液变蓝,通入氯气后蓝色褪去,溶液显浅棕色 |
| Ⅲ.向Ⅱ所得溶液继续通入氯气 | 溶液几乎变为无色 |
②写出
 在水溶液中与氯气反应生成
在水溶液中与氯气反应生成 的离子方程式
的离子方程式③由以上实验可推断
 中溶液颜色变成浅棕色的原因是
中溶液颜色变成浅棕色的原因是Ⅱ.84消毒液是一种常见的含氯消毒剂,其有效成分为次氯酸钠。
资料:84消毒液中含氯微粒主要有
 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。某兴趣小组同学研究84消毒液的漂白性,实验如下。
;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。某兴趣小组同学研究84消毒液的漂白性,实验如下。a.向
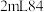 消毒液中加入
消毒液中加入 水后,放入红色纸片,观察到纸片慢慢褪色。
水后,放入红色纸片,观察到纸片慢慢褪色。b.向
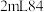 消毒液中加入
消毒液中加入 白醋后,放入红色纸片,观察到纸片迅速褪色。
白醋后,放入红色纸片,观察到纸片迅速褪色。c.测得84消毒液在不同温度时ORP随时间的变化曲线如图。

(5)①已知白醋显酸性,不具有漂白性。实验a、b现象不同的原因是
②由实验c可得出的结论是
您最近一年使用:0次
5 . 某小组同学探究不同条件下氯气与二价锰化合物的反应,
资料:i.Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、 (绿色)、
(绿色)、 (紫色);Mn(OH)2为不溶于水的白色固体。
(紫色);Mn(OH)2为不溶于水的白色固体。
ii.酸性条件下, 可被Cl-还原为Mn2+;浓碱条件下,
可被Cl-还原为Mn2+;浓碱条件下, 可被OH-还原为
可被OH-还原为 。
。
iii.Cl2的氧化性与溶液的酸碱性无关,Cl2与碱溶液反应可生成NaClO,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略):
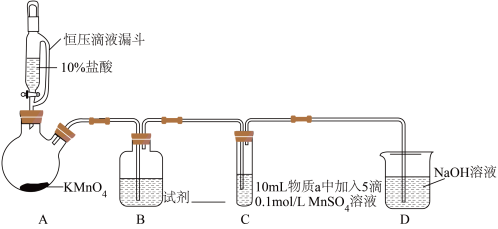
(1)A中制取Cl2的离子方程式为___________
(2)D装置的作用___________ 。
(3)通入Cl2前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为___________ 。
(4)对比实验Ⅰ、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是___________ 。
(5)根据资料ii,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二;可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①化学方程式表示可能导致溶液碱性减弱的原因___________ ,但通过实验测定溶液的碱性变化很小。
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深,溶液紫色变为绿色的离子方程式为___________ ,溶液绿色缓慢加深,原因是MnO2被NaClO氧化,可证明Ⅲ的悬浊液中氧化剂过量;
③取Ⅱ中放置后的1mL悬浊液,加入4mL水使溶液碱性减弱后,溶液紫色缓慢加深,发生的反应离子方程式是___________ 。
资料:i.Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、
 (绿色)、
(绿色)、 (紫色);Mn(OH)2为不溶于水的白色固体。
(紫色);Mn(OH)2为不溶于水的白色固体。ii.酸性条件下,
 可被Cl-还原为Mn2+;浓碱条件下,
可被Cl-还原为Mn2+;浓碱条件下, 可被OH-还原为
可被OH-还原为 。
。iii.Cl2的氧化性与溶液的酸碱性无关,Cl2与碱溶液反应可生成NaClO,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略):

| 序号 | 物质a | C中实验现象 | |
| 通入Cl2前 | 通入Cl2后 | ||
| Ⅰ | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| Ⅱ | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| Ⅲ | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(2)D装置的作用
(3)通入Cl2前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为
(4)对比实验Ⅰ、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是
(5)根据资料ii,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二;可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。①化学方程式表示可能导致溶液碱性减弱的原因
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深,溶液紫色变为绿色的离子方程式为
③取Ⅱ中放置后的1mL悬浊液,加入4mL水使溶液碱性减弱后,溶液紫色缓慢加深,发生的反应离子方程式是
您最近一年使用:0次
名校
6 . 高铁酸钾(K2FeO4)是一种新型高效无毒的多功能水处理剂。K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
I.制备K2FeO4

(1)写出A中发生反应的化学方程式:___________ 。
(2)除杂装置B中的试剂为___________ 。
(3)请写出装置C中制备K2FeO4的离子方程式___________ 。
II.探究K2FeO4的性质
取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2.为证明K2FeO4能氧化Cl-而产生Cl2设计以下方案:
(4)方案1中溶液变红可知溶液a中含有Fe3+,该离子的产生___________ (填“能”或“不能”)判断一定是由K2FeO4被Cl-还原而形成的,理由是___________ 。
(5)方案2可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是排除ClO-的干扰。根据K2FeO4的制备实验得出:氧化性Cl2___________ FeO (填“>”或“<”),而方案2实验表明,Cl2和FeO
(填“>”或“<”),而方案2实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是___________ 。
(6)资料表明,酸性溶液中的氧化性FeO >MnO
>MnO ,验证实验如下:
,验证实验如下:
将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象___________ (填“能”或“不能”)证明氧化性FeO >MnO
>MnO 。请说明理由:
。请说明理由:___________ 。
I.制备K2FeO4

(1)写出A中发生反应的化学方程式:
(2)除杂装置B中的试剂为
(3)请写出装置C中制备K2FeO4的离子方程式
II.探究K2FeO4的性质
取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2.为证明K2FeO4能氧化Cl-而产生Cl2设计以下方案:
| 方案1 | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色 |
| 方案2 | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量溶液b,滴加盐酸,有Cl2产生 |
(4)方案1中溶液变红可知溶液a中含有Fe3+,该离子的产生
(5)方案2可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是排除ClO-的干扰。根据K2FeO4的制备实验得出:氧化性Cl2
 (填“>”或“<”),而方案2实验表明,Cl2和FeO
(填“>”或“<”),而方案2实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是(6)资料表明,酸性溶液中的氧化性FeO
 >MnO
>MnO ,验证实验如下:
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象
 >MnO
>MnO 。请说明理由:
。请说明理由:
您最近一年使用:0次
名校
7 . 南高实验学习小组经查阅资料发现:K2FeO4(Mr=198)为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。现将他们制备高铁酸钾(K2FeO4),测定其纯度并探究其性质的过程展示如下。
(1)制备K2FeO4(夹持装置略)
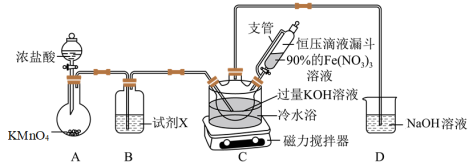
①A为氯气发生装置,盛KMnO4固体的仪器名称是___________ 。
②装置B中所用的试剂X为___________ 。
③装置C中首先制备KClO,然后在快速搅拌下将90%的Fe(NO3)3溶液分批加入装置C中,充分反应得K2FeO4固体,写出该反应的化学方程式___________ 。
(2)K2FeO4的纯度测定
向3mLCrCl3溶液中加入20mL饱和KOH溶液(Cr3++4OH-=CrO +2H2O),再加入5mL蒸馏水,冷却至室温,准确称取1.98g样品,加入上述溶液中使其溶解,充分反应(FeO
+2H2O),再加入5mL蒸馏水,冷却至室温,准确称取1.98g样品,加入上述溶液中使其溶解,充分反应(FeO +CrO
+CrO +2H2O=CrO
+2H2O=CrO +Fe(OH)3↓+OH-),过滤后加入稀硫酸酸化(2CrO
+Fe(OH)3↓+OH-),过滤后加入稀硫酸酸化(2CrO +2H+=Cr2O
+2H+=Cr2O +H2O),并加入1mL苯二胺磺酸钠作指示剂,用1.00mol/L的标准硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定(Cr2O
+H2O),并加入1mL苯二胺磺酸钠作指示剂,用1.00mol/L的标准硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定(Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O),至终点时,消耗(NH4)2Fe(SO4)2溶液的体积为27.00mL。则K2FeO4的质量分数为
+6Fe2++14H+=2Cr3++6Fe3++7H2O),至终点时,消耗(NH4)2Fe(SO4)2溶液的体积为27.00mL。则K2FeO4的质量分数为___________ (过程中杂质不参与反应)。
(3)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2.为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
Ⅰ.方案Ⅰ中溶液变红可知a中含有___________ 离子,但该离子的产生不能判断一定是K2FeO4被Cl-还原得到,还可能由___________ 产生(用离子反应方程式表示)。
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-,用KOH溶液洗涤的目的是___________ 。
②根据K2FeO4的制备实验得出:氧化性Cl2___________ FeO (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是___________ 。
(1)制备K2FeO4(夹持装置略)

①A为氯气发生装置,盛KMnO4固体的仪器名称是
②装置B中所用的试剂X为
③装置C中首先制备KClO,然后在快速搅拌下将90%的Fe(NO3)3溶液分批加入装置C中,充分反应得K2FeO4固体,写出该反应的化学方程式
(2)K2FeO4的纯度测定
向3mLCrCl3溶液中加入20mL饱和KOH溶液(Cr3++4OH-=CrO
 +2H2O),再加入5mL蒸馏水,冷却至室温,准确称取1.98g样品,加入上述溶液中使其溶解,充分反应(FeO
+2H2O),再加入5mL蒸馏水,冷却至室温,准确称取1.98g样品,加入上述溶液中使其溶解,充分反应(FeO +CrO
+CrO +2H2O=CrO
+2H2O=CrO +Fe(OH)3↓+OH-),过滤后加入稀硫酸酸化(2CrO
+Fe(OH)3↓+OH-),过滤后加入稀硫酸酸化(2CrO +2H+=Cr2O
+2H+=Cr2O +H2O),并加入1mL苯二胺磺酸钠作指示剂,用1.00mol/L的标准硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定(Cr2O
+H2O),并加入1mL苯二胺磺酸钠作指示剂,用1.00mol/L的标准硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定(Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O),至终点时,消耗(NH4)2Fe(SO4)2溶液的体积为27.00mL。则K2FeO4的质量分数为
+6Fe2++14H+=2Cr3++6Fe3++7H2O),至终点时,消耗(NH4)2Fe(SO4)2溶液的体积为27.00mL。则K2FeO4的质量分数为(3)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2.为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量b,滴加盐酸,有Cl2产生。 |
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-,用KOH溶液洗涤的目的是
②根据K2FeO4的制备实验得出:氧化性Cl2
 (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是
您最近一年使用:0次
解题方法
8 . 某小组探究Na2S溶液与KMnO4溶液反应,实验过程如下:
资料:i.MnO 在强酸性条件下被还原为Mn2+,在近中性条件下被还原为MnO2。
在强酸性条件下被还原为Mn2+,在近中性条件下被还原为MnO2。
ii.单质硫可溶于硫化钠溶液,溶液呈淡黄色。下列说法正确的是
| 实验序号 | I | II |
| 实验过程 | 滴加10滴(约0.3mL)0.1mol/L Na2S溶液 | 滴加10滴(约0.3mL)0.01mol/L酸性KMnO4溶液(H2SO4酸化至pH=0)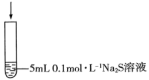 |
| 实验现象 | 紫色变浅(pH<1),生成棕褐色沉淀(MnO2) | 溶液呈淡黄色(pH≈8),生成浅粉色沉淀(MnS) |
 在强酸性条件下被还原为Mn2+,在近中性条件下被还原为MnO2。
在强酸性条件下被还原为Mn2+,在近中性条件下被还原为MnO2。ii.单质硫可溶于硫化钠溶液,溶液呈淡黄色。下列说法正确的是
A.取少量实验I所得溶液进行实验,检测到有SO ,说明S2-被MnO ,说明S2-被MnO 氧化为SO 氧化为SO |
B.实验I中生成棕褐色沉淀的原因: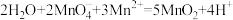 |
| C.实验II中所有参加反应的S2-均表现还原性 |
| D.实验现象说明:物质变化除与自身性质有关,还与浓度、用量、溶液的酸碱性有关 |
您最近一年使用:0次
名校
解题方法
9 .  是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。
资料:①锰酸钾( )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
②酸性条件下的氧化性: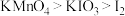
I. 的制备
的制备
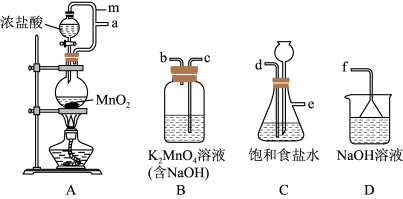
(1)从A~D中选择合适的装置制备 ,正确的连接顺序是a→
,正确的连接顺序是a→_______ (按气流方向,用小写字母表示):装置A中m的作用是_______ 。若没有使用装置C,造成的影响是_________ 。
II. 性质探究
性质探究
取适量制取的 溶液稀释至约0.01mol/L(用硫酸酸化至pH=1),取配制好的
溶液稀释至约0.01mol/L(用硫酸酸化至pH=1),取配制好的 溶液2mL于试管中,逐滴滴加0.1mol/L KI溶液,
溶液2mL于试管中,逐滴滴加0.1mol/L KI溶液, 紫色溶液迅速变为棕褐色悬浊液,然后沉淀逐渐消失,最终溶液变为棕黄色。
紫色溶液迅速变为棕褐色悬浊液,然后沉淀逐渐消失,最终溶液变为棕黄色。
(2)最终溶液呈现棕黄色推测生成了______________ (写化学式)。
实验小组对初始阶段的产物成分进行探究:
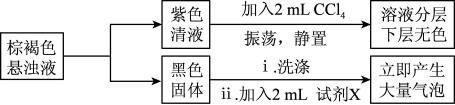
(3)黑色固体是 ,试剂X是
,试剂X是___________ (写化学式)。
(4)在“紫色清液”中存在 ,下列实验方案中,可用于检验“紫色清液”中是否存在
,下列实验方案中,可用于检验“紫色清液”中是否存在 的是
的是____ (填序号)。
A.用洁净的玻璃棒随取紫色清液滴在淀粉—KI试纸上,观察试纸是否变蓝色。
B.取少量紫色清液于试管中,向其中加入几滴淀粉溶液,溶液不变蓝,再加入过量 溶液,观察溶液是否变色。
溶液,观察溶液是否变色。
C.取少量紫色清液于试管中,加入稀硝酸酸化,再加入几滴硝酸银溶液,观察是否生成黄色沉淀。
探究实验II中棕褐色沉淀消失的原因:
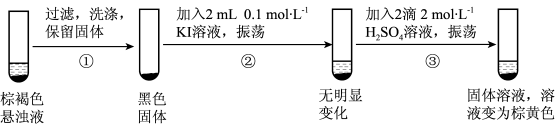
(5)用化学方程式解释步骤③中固体消失的原因_______________________ 。
(6)由上述实验可知, 的还原产物与
的还原产物与______ 有关。
 是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。资料:①锰酸钾(
 )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
②酸性条件下的氧化性:
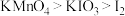
I.
 的制备
的制备
(1)从A~D中选择合适的装置制备
 ,正确的连接顺序是a→
,正确的连接顺序是a→II.
 性质探究
性质探究取适量制取的
 溶液稀释至约0.01mol/L(用硫酸酸化至pH=1),取配制好的
溶液稀释至约0.01mol/L(用硫酸酸化至pH=1),取配制好的 溶液2mL于试管中,逐滴滴加0.1mol/L KI溶液,
溶液2mL于试管中,逐滴滴加0.1mol/L KI溶液, 紫色溶液迅速变为棕褐色悬浊液,然后沉淀逐渐消失,最终溶液变为棕黄色。
紫色溶液迅速变为棕褐色悬浊液,然后沉淀逐渐消失,最终溶液变为棕黄色。(2)最终溶液呈现棕黄色推测生成了
实验小组对初始阶段的产物成分进行探究:

(3)黑色固体是
 ,试剂X是
,试剂X是(4)在“紫色清液”中存在
 ,下列实验方案中,可用于检验“紫色清液”中是否存在
,下列实验方案中,可用于检验“紫色清液”中是否存在 的是
的是A.用洁净的玻璃棒随取紫色清液滴在淀粉—KI试纸上,观察试纸是否变蓝色。
B.取少量紫色清液于试管中,向其中加入几滴淀粉溶液,溶液不变蓝,再加入过量
 溶液,观察溶液是否变色。
溶液,观察溶液是否变色。C.取少量紫色清液于试管中,加入稀硝酸酸化,再加入几滴硝酸银溶液,观察是否生成黄色沉淀。
探究实验II中棕褐色沉淀消失的原因:

(5)用化学方程式解释步骤③中固体消失的原因
(6)由上述实验可知,
 的还原产物与
的还原产物与
您最近一年使用:0次
解题方法
10 . 实验小组制备高铁酸钾( K2FeO4 )并进行相关探究。
资料:高铁酸钾为紫色固体,极易溶于水,微溶于KOH溶液,难溶于乙醇;在0~5° C、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2;198 °C以上易分解。

请回答下列问题:
(1)制备K2FeO4(夹持装置略)
①实验过程中B装置的作用是_____________________________________ 。
②A装置中发生反应时,氧化剂与还原剂的物质的量之比为___________ 。
③C装置中得到紫色固体和溶液。C装置中Cl2发生的反应有3Cl2 +2Fe(OH)3 +10KOH= 2K2FeO4 + 6KCl+8H2O、______ 。
④将装置C中粗产品溶于冷的KOH溶液,过滤,用无水乙醇洗涤,干燥即得粗产品。选择无水乙醇进行洗涤的优点是_________ (写一条)。
(2)为探究K2FeO4的性质,即证明K2FeO4是否能氧化Cl-而产生Cl2,该实验小组进行了如下实验:
①实验i中产生的“黄绿色气体”中,除含有Cl2,还可能含有____________________ ( 填化学式)。
②实验iii证明a中含有Fe3+,写出相应的操作以及现象:__________________ 。
③能证明K2FeO4氧化了Cl-的实验是____ (填“ i”“ii” “iii”或“iv”)。
④资料表明,酸性溶液中的氧化性 >
>  ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 >
>  ?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:_______________ 。
资料:高铁酸钾为紫色固体,极易溶于水,微溶于KOH溶液,难溶于乙醇;在0~5° C、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2;198 °C以上易分解。

请回答下列问题:
(1)制备K2FeO4(夹持装置略)
①实验过程中B装置的作用是
②A装置中发生反应时,氧化剂与还原剂的物质的量之比为
③C装置中得到紫色固体和溶液。C装置中Cl2发生的反应有3Cl2 +2Fe(OH)3 +10KOH= 2K2FeO4 + 6KCl+8H2O、
④将装置C中粗产品溶于冷的KOH溶液,过滤,用无水乙醇洗涤,干燥即得粗产品。选择无水乙醇进行洗涤的优点是
(2)为探究K2FeO4的性质,即证明K2FeO4是否能氧化Cl-而产生Cl2,该实验小组进行了如下实验:
实验方案与现象 | |
i | 取适量C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2 |
ii | 取少量a,滴加淀粉KI溶液,无明显现象 |
iii | |
iv | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液 b,取少量b,滴加盐酸,有Cl2产生 |
②实验iii证明a中含有Fe3+,写出相应的操作以及现象:
③能证明K2FeO4氧化了Cl-的实验是
④资料表明,酸性溶液中的氧化性
 >
>  ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 >
>  ?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
?若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
您最近一年使用:0次



