名校
解题方法
1 . 取某铁铝铜合金9.34g,溶于足量的稀硝酸中,金属无剩余,收集到的一种气体是唯一还原产物。向溶液中加过量的氢氧化钠溶液,小心收集沉淀洗涤干净称重11.23g,加热分解至衡重,得固体质量为8.80g。则下列说法不正确的是
| A.参加反应的氢氧化钠不一定比参加反应的硝酸的物质的量多 |
| B.合金中铁铝的物质的量之比为1:2 |
| C.收集到的气体在标准状况下为4.256L |
| D.与铁铝铜合金反应的硝酸的物质的量是0.57mol |
您最近一年使用:0次
名校
解题方法
2 . 关于非金属含氧酸及其盐的性质,下列说法正确的是
| A.Ag与浓硝酸反应比与稀硝酸反应快,所以实验室通常用浓硝酸洗涤附着在试管内壁上的银镜 |
| B.加热浓硫酸与NaCl固体的混合物可制备HCl,说明浓硫酸酸性强于HCl |
| C.将CO2通入Ba(NO3)2:溶液无明显现象,则将SO2通入Ba(NO3)2溶液也无明显现象 |
| D.向NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解反应 |
您最近一年使用:0次
2024-03-27更新
|
730次组卷
|
4卷引用:山东省济南市2023-2024学年高三下学期3月模拟(一模)考试化学试题
解题方法
3 . 下列离子方程式正确的是
A.向饱和Na2CO3溶液中通入过量CO2: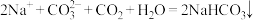 |
B.向稀硝酸中加入过量铁粉: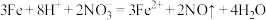 |
C.用KMnO4与浓盐酸反应制取氯气: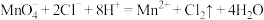 |
D.向NaClO溶液中通入少量SO2: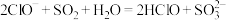 |
您最近一年使用:0次
解题方法
4 . 对下列事实的解释中,错误的是
| A.常温下,浓硝酸可以用铝质容器储存,说明铝与浓硝酸不反应 |
| B.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| C.浓硫酸能与灼热的木炭反应产生二氧化碳和二氧化硫,说明浓硫酸具有强氧化性 |
| D.氢氧化亚铁在空气中不稳定,会转化成氢氧化铁,说明氢氧化亚铁具有还原性 |
您最近一年使用:0次
5 . 物质的量是联系宏观量与微观粒子数量的重要桥梁。回答下列问题:
(1)某汽车安全气囊的气体发生剂为叠氮化钠(NaN3),在受到撞击时分解生成Na和N2,130 g NaN3分解产生的N2在标准状况下的体积为______ L。
(2)SO2和O2组成的混合气体在标准状况下的密度为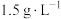 ,其中SO2的物质的量分数为
,其中SO2的物质的量分数为______ 。
(3)64 g铜与300 mL一定浓度的硝酸恰好完全反应,产生的NO和NO2混合气体在标准状况下的体积共22.4 L。NO与NO2的体积比为______ ,该硝酸的物质的量浓度为______  。
。
(4)实验室需使用240 mL物质的量浓度为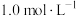 的稀硫酸进行有关实验,现用98%的浓硫酸进行配制。
的稀硫酸进行有关实验,现用98%的浓硫酸进行配制。
①需用量筒量取98%的浓硫酸(密度为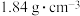 )
)______ mL。
②下列情况会导致所配溶液浓度偏高的是______ (填标号)。
a.定容后摇匀时有少量溶液溅出
b.定容时仰视容量瓶瓶颈上的刻度线
c.使用量筒量取浓硫酸时仰视刻度线
d.硫酸溶液移入容量瓶后没有洗涤烧杯
e.稀释后未冷却即进行移液、定容等操作
(1)某汽车安全气囊的气体发生剂为叠氮化钠(NaN3),在受到撞击时分解生成Na和N2,130 g NaN3分解产生的N2在标准状况下的体积为
(2)SO2和O2组成的混合气体在标准状况下的密度为
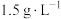 ,其中SO2的物质的量分数为
,其中SO2的物质的量分数为(3)64 g铜与300 mL一定浓度的硝酸恰好完全反应,产生的NO和NO2混合气体在标准状况下的体积共22.4 L。NO与NO2的体积比为
 。
。(4)实验室需使用240 mL物质的量浓度为
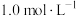 的稀硫酸进行有关实验,现用98%的浓硫酸进行配制。
的稀硫酸进行有关实验,现用98%的浓硫酸进行配制。①需用量筒量取98%的浓硫酸(密度为
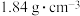 )
)②下列情况会导致所配溶液浓度偏高的是
a.定容后摇匀时有少量溶液溅出
b.定容时仰视容量瓶瓶颈上的刻度线
c.使用量筒量取浓硫酸时仰视刻度线
d.硫酸溶液移入容量瓶后没有洗涤烧杯
e.稀释后未冷却即进行移液、定容等操作
您最近一年使用:0次
解题方法
6 . 某溶液中可能含有K+、 、Fe2+、Cl-、
、Fe2+、Cl-、 、
、 中的若干种,且各离子浓度均为0.2 mol/L,为确定其组成,某同学进行了如下实验:
中的若干种,且各离子浓度均为0.2 mol/L,为确定其组成,某同学进行了如下实验:
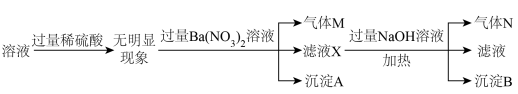
下列说法正确的是
 、Fe2+、Cl-、
、Fe2+、Cl-、 、
、 中的若干种,且各离子浓度均为0.2 mol/L,为确定其组成,某同学进行了如下实验:
中的若干种,且各离子浓度均为0.2 mol/L,为确定其组成,某同学进行了如下实验:
下列说法正确的是
| A.“气体M”与“气体N”中含有同种元素 |
| B.“沉淀A”和“沉淀B”都不溶于强酸 |
C.原溶液中含有的离子为 、Fe2+、Cl-、 、Fe2+、Cl-、 |
D.“滤液X”中大量存在的阳离子有 、Fe2+、Ba2+ 、Fe2+、Ba2+ |
您最近一年使用:0次
名校
解题方法
7 . 硫氰化钾(KSCN)在有机合成中具有重要应用,但会污染环境。预测浓硝酸能与KSCN反应以消除污染,现通过如下实验进行探究。
已知: 能被氧化为黄色的
能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。
【实验一】
取2 mL浓硝酸于试管中,向其中滴加5滴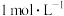 的KSCN溶液,溶液立即变红,静置一段时间后,试管内突然剧烈反应,红色退去,放出大量红棕色气体。
的KSCN溶液,溶液立即变红,静置一段时间后,试管内突然剧烈反应,红色退去,放出大量红棕色气体。
(1)向浓硝酸中滴加KSCN溶液,溶液立即变红是因为生成了______ (填化学式)。KSCN中S元素的化合价为-2,预测剧烈反应后含硫产物可能是______ 。
【实验二】
将实验一放出的气体通入 和NaOH的混合溶液中,有白色沉淀生成。将过滤、洗涤后的白色沉淀置于试管中,加入过量稀硝酸,沉淀完全溶解。
和NaOH的混合溶液中,有白色沉淀生成。将过滤、洗涤后的白色沉淀置于试管中,加入过量稀硝酸,沉淀完全溶解。
(2)该实验证实了红棕色气体中不含SO2,证据是______ ,白色沉淀为______ 。
【实验三】
(3)另取少量实验一最终所得溶液,______ (填操作和现象),证明溶液中含有 。
。
(4)经检验实验一放出的红棕色气体中含NO2,但NO2不一定是 的氧化产物,理由是
的氧化产物,理由是______ 。
【实验四】
(5)某同学向待测溶液中加入KSCN溶液,再加入浓硝酸,最终未得红色溶液,由此得出结论:待测液中不含 。
。
你认为该同学的结论是否正确:______ (填“是”或“否”),理由是______ 。
已知:
 能被氧化为黄色的
能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。【实验一】
取2 mL浓硝酸于试管中,向其中滴加5滴
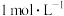 的KSCN溶液,溶液立即变红,静置一段时间后,试管内突然剧烈反应,红色退去,放出大量红棕色气体。
的KSCN溶液,溶液立即变红,静置一段时间后,试管内突然剧烈反应,红色退去,放出大量红棕色气体。(1)向浓硝酸中滴加KSCN溶液,溶液立即变红是因为生成了
【实验二】
将实验一放出的气体通入
 和NaOH的混合溶液中,有白色沉淀生成。将过滤、洗涤后的白色沉淀置于试管中,加入过量稀硝酸,沉淀完全溶解。
和NaOH的混合溶液中,有白色沉淀生成。将过滤、洗涤后的白色沉淀置于试管中,加入过量稀硝酸,沉淀完全溶解。(2)该实验证实了红棕色气体中不含SO2,证据是
【实验三】
(3)另取少量实验一最终所得溶液,
 。
。(4)经检验实验一放出的红棕色气体中含NO2,但NO2不一定是
 的氧化产物,理由是
的氧化产物,理由是【实验四】
(5)某同学向待测溶液中加入KSCN溶液,再加入浓硝酸,最终未得红色溶液,由此得出结论:待测液中不含
 。
。你认为该同学的结论是否正确:
您最近一年使用:0次
2024-02-04更新
|
162次组卷
|
2卷引用:山东省济南市2023-2024学年高一上学期1月期末考试化学试题
8 . 下图为氮及其化合物的“价—类”二维图,下列说法正确的是

| A.a转化为f的过程属于氮的固定 |
| B.从化合价角度预测,g可能通过分解反应转化为b |
| C.工业上以a为原料制取e需要经历四步氧化还原反应 |
| D.排放到大气中的c、d是形成光化学烟雾、雾霾及酸雨的重要原因 |
您最近一年使用:0次
2024-02-04更新
|
258次组卷
|
2卷引用:山东省济南市2023-2024学年高一上学期1月期末考试化学试题
9 . 下列实验方案可以达到实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 将溴蒸气和 分别通入硝酸银溶液中,产生淡黄色沉淀的是溴蒸气 分别通入硝酸银溶液中,产生淡黄色沉淀的是溴蒸气 | 鉴别溴蒸气和 |
| B | Cu和浓硫酸共热一段时间,待试管冷却后,向反应后的试管中加水,溶液呈蓝色 | 证明Cu被浓硫酸氧化为 |
| C | 向碳酸钠溶液中加入浓盐酸,将反应后的气体通入硅酸钠溶液中 | 判断C和Si的非金属性强弱 |
| D | 向浓硝酸中插入红热的木炭产生红棕色气体 | 验证木炭和浓硝酸反应生成红棕色气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 对某透明溶液分别进行下列操作,所得现象和结论均正确的是
A.加入硝酸钡溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,则原溶液中一定有 |
B.加入硝酸酸化的 溶液,无明显现象,再滴加 溶液,无明显现象,再滴加 溶液,有白色沉淀生成,则溶液中一定含有 溶液,有白色沉淀生成,则溶液中一定含有 |
C.滴加 溶液后再加入KSCN溶液,溶液呈红色,则原溶液中一定含有 溶液后再加入KSCN溶液,溶液呈红色,则原溶液中一定含有 |
D.加入稀NaOH溶液,将湿润的红色石蕊试纸靠近试管口,试纸不变蓝,该盐溶液中一定不含有 |
您最近一年使用:0次



