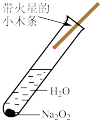名校
解题方法
1 . 关于非金属含氧酸及其盐的性质,下列说法正确的是
| A.Ag与浓硝酸反应比与稀硝酸反应快,所以实验室通常用浓硝酸洗涤附着在试管内壁上的银镜 |
| B.加热浓硫酸与NaCl固体的混合物可制备HCl,说明浓硫酸酸性强于HCl |
| C.将CO2通入Ba(NO3)2:溶液无明显现象,则将SO2通入Ba(NO3)2溶液也无明显现象 |
| D.向NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解反应 |
您最近一年使用:0次
2024-03-27更新
|
709次组卷
|
4卷引用:山东省泰安市新泰第一中学老校区(新泰中学)2023-2024学年高三下学期第二次模拟化学试题
2 . 常温下,下列溶液可以用铝槽车装运的是
| A.稀硫酸 | B.浓盐酸 | C.浓硫酸 | D.稀硝酸 |
您最近一年使用:0次
名校
3 . 按要求完成下列填空:
(1)写出 在水中的电离方程式
在水中的电离方程式___________ 。
(2)向新制氯水中滴加石蕊试液,溶液变红,起作用的微粒是___________ ;然后又褪色,起作用的微粒是___________ 。
(3)实验证明铜、不能在低温下与 反应,也不能与稀
反应,也不能与稀 共热发生反应,但工业上却是将废铜屑倒入热的稀
共热发生反应,但工业上却是将废铜屑倒入热的稀 中并通入空气来制备
中并通入空气来制备 溶液的。铜屑在此状态下被溶解的化学方程式为
溶液的。铜屑在此状态下被溶解的化学方程式为___________ 。
(4)过量铁粉与稀硝酸反应方程式为: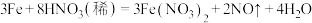 此反应中,被还原和未被还原的硝酸的物质的量之比为
此反应中,被还原和未被还原的硝酸的物质的量之比为___________ 。当产生 气体在标况下体积为
气体在标况下体积为 时,转移电子
时,转移电子___________  ,被还原的硝酸的物质的量为
,被还原的硝酸的物质的量为___________  。
。
(5)漂白粉是常用的消毒剂。漂白粉的有效成分是(填化学式)___________ 。
(1)写出
 在水中的电离方程式
在水中的电离方程式(2)向新制氯水中滴加石蕊试液,溶液变红,起作用的微粒是
(3)实验证明铜、不能在低温下与
 反应,也不能与稀
反应,也不能与稀 共热发生反应,但工业上却是将废铜屑倒入热的稀
共热发生反应,但工业上却是将废铜屑倒入热的稀 中并通入空气来制备
中并通入空气来制备 溶液的。铜屑在此状态下被溶解的化学方程式为
溶液的。铜屑在此状态下被溶解的化学方程式为(4)过量铁粉与稀硝酸反应方程式为:
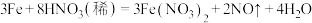 此反应中,被还原和未被还原的硝酸的物质的量之比为
此反应中,被还原和未被还原的硝酸的物质的量之比为 气体在标况下体积为
气体在标况下体积为 时,转移电子
时,转移电子 ,被还原的硝酸的物质的量为
,被还原的硝酸的物质的量为 。
。(5)漂白粉是常用的消毒剂。漂白粉的有效成分是(填化学式)
您最近一年使用:0次
名校
4 . 盐酸、硫酸、硝酸是工业生产中常用的三种强酸。回答下列问题:
(1)盐酸既有酸性,又能表现氧化性和还原性。若用浓盐酸制取氯气,需要与具有___________ (酸性、氧化性、还原性)的物质发生反应;若用0.6mol  与100 mL
与100 mL 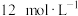 的浓盐酸加热反应,生成Cl2的物质的量
的浓盐酸加热反应,生成Cl2的物质的量___________ (填标号)。
A.等于0.6 mol B.大于0.3 mol C.等于0.3 mol D.小于0.3 mol
(2)以下为用硫酸制取硫酸铜的两种方法。①实验室常利用铜与浓硫酸加热反应制得硫酸铜;②工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来制备硫酸铜。方法②反应的离子方程式为___________ 。上述两种方法中,制取硫酸铜的最佳方法是___________ (填“①”或“②”)。
(3)将3.84 g铜与一定量的浓硝酸反应,当铜消耗完毕时产生NO和NO2气体的体积为2.24 L(标况),则参加反应的硝酸的物质的量为___________ mol。生成的NO在标况下的体积是___________ L,氧化剂与还原剂的物质的量之比是___________ 。
(4)Q为单质,X、Y、Z、E、M五种物质含有同一元素,一定条件下有以下的转化关系。
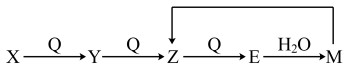
若M为酸。则M的化学式可能为___________ 。
(1)盐酸既有酸性,又能表现氧化性和还原性。若用浓盐酸制取氯气,需要与具有
 与100 mL
与100 mL 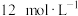 的浓盐酸加热反应,生成Cl2的物质的量
的浓盐酸加热反应,生成Cl2的物质的量A.等于0.6 mol B.大于0.3 mol C.等于0.3 mol D.小于0.3 mol
(2)以下为用硫酸制取硫酸铜的两种方法。①实验室常利用铜与浓硫酸加热反应制得硫酸铜;②工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来制备硫酸铜。方法②反应的离子方程式为
(3)将3.84 g铜与一定量的浓硝酸反应,当铜消耗完毕时产生NO和NO2气体的体积为2.24 L(标况),则参加反应的硝酸的物质的量为
(4)Q为单质,X、Y、Z、E、M五种物质含有同一元素,一定条件下有以下的转化关系。

若M为酸。则M的化学式可能为
您最近一年使用:0次
名校
5 . 下列类比或推理合理的是
| 选项 | 已知 | 方法 | 结论 |
| A | CO2通入Ba(NO3)2溶液无沉淀生成 | 类比 | SO2通入Ba(NO3)2溶液无沉淀生成 |
| B | 钠保存在煤油中 | 类比 | 锂保存在煤油中 |
| C | NaH2PO2是正盐 | 推理 | H3PO2是一元酸 |
| D | CO2与Na2O2反应生成Na2CO3和O2 | 类比 | SO2与Na2O2反应生成Na2SO3和O2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-30更新
|
233次组卷
|
2卷引用:山东省泰安市2023-2024学年高三上学期期中考试化学试题
名校
6 . 下列对有关实验现象的解释或所得结论错误的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将NaBiO3固体加入酸性MnSO4溶液中,充分振荡 | 溶液变为紫红色 | 氧化性:BiO >MnO >MnO |
| B | 用pH计测定室温下溶液pH:①CH3COONa②NaHCO3 | pH值①<② | 碳酸酸性弱于醋酸 |
| C | 将少量铜粉加入稀硫酸中,无明显现象,再加入硝酸铁溶液 | 铜粉溶解 | Fe3+与铜粉反应 |
| D | 向NaClO溶液中滴加酚酞试液 | 溶液先变红后褪色 | NaClO发生水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
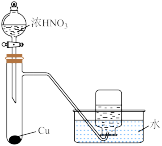
7 . 化学兴趣小组利用下图装置(夹持仪器已略去)验证浓、稀硝酸氧化性的相对强弱。已知:浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
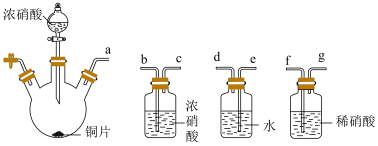
(1)为实现实验目的,上述装置的接口连接顺序依次为a________________ (填装置接口序号,装置不能重复使用),C的作用是__________ (用化学方程式表示)。
(2)该小组要得出“浓硝酸的氧化性强于稀硝酸”的实验结论,所依据的实验现象是__________ 。
(3)开始实验应进行的操作为__________ 。该实验装置存在明显缺陷,应该__________ 。
(4)实验过程中,小组同学发现A中铜片溶解,得到绿色溶液Ⅰ,放置较长时间后得到蓝色溶液Ⅱ。
①甲认为溶液呈现绿色的原因是Cu2+浓度较大,乙根据实验记录,认为观点不正确。乙的依据是__________ 。
②乙认为溶液呈绿色是由溶解的NO2引起的。实验验证:先将NO2通入溶液Ⅱ中,再鼓入N2,结果证实假设成立。则以上两步操作对应的现象分别是__________ 、__________ 。

(1)为实现实验目的,上述装置的接口连接顺序依次为a
(2)该小组要得出“浓硝酸的氧化性强于稀硝酸”的实验结论,所依据的实验现象是
(3)开始实验应进行的操作为
(4)实验过程中,小组同学发现A中铜片溶解,得到绿色溶液Ⅰ,放置较长时间后得到蓝色溶液Ⅱ。
①甲认为溶液呈现绿色的原因是Cu2+浓度较大,乙根据实验记录,认为观点不正确。乙的依据是
②乙认为溶液呈绿色是由溶解的NO2引起的。实验验证:先将NO2通入溶液Ⅱ中,再鼓入N2,结果证实假设成立。则以上两步操作对应的现象分别是
您最近一年使用:0次
名校
8 . 下列装置或操作一定能达到实验目的的是
| 选项 | A | B | C | D |
| 实验 装置 |
|
|
|
|
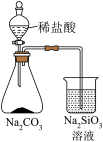
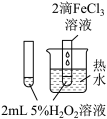
| 实验 目的 | 验证 与水反应生成 与水反应生成 | 验证非金属性强弱: | 验证 对 对 分解反应有催化作用 分解反应有催化作用 | 用Cu和浓硝酸制取并收集 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-14更新
|
313次组卷
|
4卷引用:山东省泰安市宁阳四中2023-2024学年高二上学期期末化学模拟试卷
名校
9 . 通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之一,下列实验操作、现象和解释或者结论正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| ① | 将金属钠在燃烧匙中点燃,迅速伸入集满 气体的集气瓶 气体的集气瓶 | 瓶中产生大量白烟和黑色颗粒 |  具有氧化性 具有氧化性 |
| ② | 向黄色的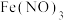 溶液中滴加氢碘酸 溶液中滴加氢碘酸 | 溶液颜色加深 | 氧化性: |
| ③ | 向某钾盐中滴加浓盐酸,产生的气体再通入品红溶液 | 品红溶液褪色 | 该钾盐为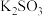 、 、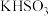 与 与 至少有一种 至少有一种 |
| ④ | 工业上用 与焦炭在高温条件下制备粗硅 与焦炭在高温条件下制备粗硅 | 生成可燃性气体,得到黑色固体粗硅 | 非金属性: |
| ⑤ | 用pH试纸测量饱和新制氯水的酸碱性 | pH试纸先变红色后褪色 | 饱和新制氯水呈酸性且具有漂白性 |
| A.①⑤ | B.①③⑤ | C.①③④ | D.①②③④⑤ |
您最近一年使用:0次
名校
解题方法
10 . 下列过程涉及的化学反应相应的离子方程式正确的是
A.向碘化亚铁溶液中滴加少量稀硝酸: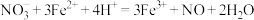 |
B.等浓度等体积的 溶液和HCl溶液混合: 溶液和HCl溶液混合: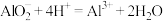 |
C.硅酸钠溶液中通入足量二氧化碳: |
D.少量 通入NaClO溶液中: 通入NaClO溶液中: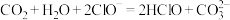 |
您最近一年使用:0次