名校
解题方法
1 . 下列关于浓硝酸和浓硫酸说法错误的是
| A.常温下,可用铁制容器储存浓硫酸、浓硝酸 |
| B.浓硫酸具有脱水性,可用做干燥剂 |
| C.浓硝酸通常保存在棕色试剂瓶中 |
| D.浓硫酸能与灼热的木炭反应生成二氧化碳和二氧化硫 |
您最近一年使用:0次
名校
解题方法
2 . 常温时下列各组离子在指定溶液中一定能大量共存的是
A.能使紫色石蕊试液变红的溶液: 、 、 、 、 、 、 |
B.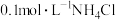 溶液: 溶液: 、 、 、 、 、 、 |
C.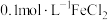 溶液: 溶液: 、 、 、 、 、 、 |
D.与Fe反应能产生 的溶液: 的溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
3 . 氮、硫及其化合物的价类二维图如下所示,下列说法正确的是

| A.b和v均可一步反应生成对应的各类氧化物 |
| B.a、b、u、v、w均能作还原剂 |
| C.d、w、x均可与水反应生成酸,都属于酸性氧化物 |
| D.e、z的浓溶液与铜反应分别生成氧化物d、x |
您最近一年使用:0次
名校
4 . I.某化学课外小组利用下图装置探究 的性质。
的性质。

请回答下列问题:
(1)装置甲中A仪器的名称是_________ ,烧瓶内发生反应的化学方程式为__________ 。
(2)装置乙中出现的现象是___________ 。可以证明 具有
具有___________ (填代号)。
A.氧化性 B.还原性 C.漂白性
(3)装置丙中发生的反应的化学方程式为________ ,可以证明 具有
具有_________ (填代号)
A.氧化性 B.还原性 C.漂白性
(4)收集 气体可以选择的装置为
气体可以选择的装置为___________ (填代号)。

(5)从环保的角度考虑,收集装置的出气口需要连接一个盛有___________ (填化学式)溶液的洗气瓶,发生反应的离子方程式为___________ 。
Ⅱ.将铜片放入到浓硝酸中:
(6)若铜有剩余,则反应开始时的离子反应方程式是___________ 。
(7)待反应停止后,再加入少量的25%的稀硫酸,加热,这时铜片上又有气泡产生,写出此时发生的离子反应方程式___________ 。
 的性质。
的性质。
请回答下列问题:
(1)装置甲中A仪器的名称是
(2)装置乙中出现的现象是
 具有
具有A.氧化性 B.还原性 C.漂白性
(3)装置丙中发生的反应的化学方程式为
 具有
具有A.氧化性 B.还原性 C.漂白性
(4)收集
 气体可以选择的装置为
气体可以选择的装置为
(5)从环保的角度考虑,收集装置的出气口需要连接一个盛有
Ⅱ.将铜片放入到浓硝酸中:
(6)若铜有剩余,则反应开始时的离子反应方程式是
(7)待反应停止后,再加入少量的25%的稀硫酸,加热,这时铜片上又有气泡产生,写出此时发生的离子反应方程式
您最近一年使用:0次
5 . 化学是以实验为基础的科学,下列有关仪器的使用和操作方法正确的是


| A.图①为实验室制取Fe(OH)2的操作 | B.图②为加热液体的操作 |
| C.用仪器③盛放NaOH溶液 | D.用仪器④盛放浓硝酸 |
您最近一年使用:0次
6 . 铁及其化合物在工业上用途广泛。部分含铁物质的分类与相应铁元素的化合价关系如图所示。回答下列问题:

(1)在高温条件下,Al粉可与a的粉末反应。写出该反应的一个用途______ 。
(2)电子工业中,人们常用b的溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板。该反应的离子方程式为______ ,设计实验证明腐蚀后的废液中含有b的阳离子:______ 。
(3)工业上可以用c制造的容器盛放冷的浓硝酸,体现了浓硝酸的______ 性;在加热条件下二者可剧烈反应,c与足量浓硝酸在加热条件下反应的化学方程式为______ 。
(4)d为K2FeO4,是一种新型、高效的水处理剂。已知湿法制备它的体系中参加反应的六种微粒为:d的阴离子、e、H2O、 、
、 、
、 。该反应的离子方程式为
。该反应的离子方程式为______ 。若要制备0.2mol ,理论上需要
,理论上需要______ gNaClO。

(1)在高温条件下,Al粉可与a的粉末反应。写出该反应的一个用途
(2)电子工业中,人们常用b的溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板。该反应的离子方程式为
(3)工业上可以用c制造的容器盛放冷的浓硝酸,体现了浓硝酸的
(4)d为K2FeO4,是一种新型、高效的水处理剂。已知湿法制备它的体系中参加反应的六种微粒为:d的阴离子、e、H2O、
 、
、 、
、 。该反应的离子方程式为
。该反应的离子方程式为 ,理论上需要
,理论上需要
您最近一年使用:0次
7 . 下列有关试剂存放的说法错误的是
| A.钠、钾保存在煤油中 | B.浓硝酸盛放在棕色细口试剂瓶中 |
| C.白磷保存在水中 | D.液溴贮存在橡胶塞的细口瓶中,加水封 |
您最近一年使用:0次
8 . 下列说法正确的是
| A.工业上常用MnS作沉淀剂除去废水中的Cu2+,证明Ksp(MnS)>Ksp(CuS) |
| B.将FeCl2溶液滴加到酸性KMnO4溶液中,紫色褪去,证明Fe2+具有还原性 |
| C.红热的炭插入浓硝酸中产生红棕色气体,证明炭与浓硝酸反应生成NO2气体 |
| D.苯、液溴与铁粉混合,生成气体通入AgNO3溶液中,若得到淡黄色沉淀则证明苯与液溴发生取代反应 |
您最近一年使用:0次
2023-02-21更新
|
267次组卷
|
2卷引用:山东省威海市2022-2023学年高三上学期期末考试化学试题
9 . 某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成 ,而稀硝酸不能氧化NO,由此得出的结论是浓硝酸的氧化性强于稀硝酸。
,而稀硝酸不能氧化NO,由此得出的结论是浓硝酸的氧化性强于稀硝酸。
可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、氢氧化钠溶液及氮气。
已知:氢氧化钠溶液不与NO反应,能与 反应:
反应:
_______ (选填“A、B、C、D”,药品可重复使用)。
A.蒸馏水B.浓硝酸C.3mol/L稀硝酸D.氢氧化钠溶液
(2)滴加浓硝酸之前的操作是:检验装置的气密性,加入药品,打开弹簧夹后,继续进行的操作是_______ ,然后关闭弹簧夹,将装置⑤中导管末端伸入倒置的烧瓶内。
(3)装置①中发生反应的化学方程式是_______ 。
(4)装置②发生反应的化学方程式是_______ 。
(5)该小组得出结论依据的实验现象是_______ 。
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个试验来判断两种看法是否正确。这些方案中可行的是_______ (填字母)。
a.加热该绿色溶液,观察颜色变化
b.向该绿色溶液中通入氮气,观察颜色变化
c.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
d.加水稀释绿色溶液,观察颜色变化
 ,而稀硝酸不能氧化NO,由此得出的结论是浓硝酸的氧化性强于稀硝酸。
,而稀硝酸不能氧化NO,由此得出的结论是浓硝酸的氧化性强于稀硝酸。可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、氢氧化钠溶液及氮气。
已知:氢氧化钠溶液不与NO反应,能与
 反应:
反应:

A.蒸馏水B.浓硝酸C.3mol/L稀硝酸D.氢氧化钠溶液
(2)滴加浓硝酸之前的操作是:检验装置的气密性,加入药品,打开弹簧夹后,继续进行的操作是
(3)装置①中发生反应的化学方程式是
(4)装置②发生反应的化学方程式是
(5)该小组得出结论依据的实验现象是
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个试验来判断两种看法是否正确。这些方案中可行的是
a.加热该绿色溶液,观察颜色变化
b.向该绿色溶液中通入氮气,观察颜色变化
c.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
d.加水稀释绿色溶液,观察颜色变化
您最近一年使用:0次
2023-01-14更新
|
751次组卷
|
4卷引用:山东省威海市乳山市银滩高级中学2023-2024学年高一上学期12月月考化学试题
名校
10 . 在100mL的混合液中,硝酸和硫酸的物质的量浓度分别是0.4mol/L、0.2mol/L,向该混合液中加入2.56g铜粉,加热,待充分反应后,所得溶液中铜离子的物质的量浓度是
| A.0.15mol/L | B.0.225mol/L | C.0.30mol/L | D.0.45mol/L |
您最近一年使用:0次
2023-01-14更新
|
682次组卷
|
5卷引用:山东省威海市乳山市银滩高级中学2023-2024学年高一上学期12月月考化学试题



