解题方法
1 . 下表是元素周期表的一部分。①~⑦分别对应七种元素,回答下列问题:___________ 。
(2)③和④两种元素的非金属性强弱关系:③___________ (填“>”或“<”)④。
(3)⑤和⑦两种元素组成的化合物中含有的化学键是___________ (填“共价”或“离子”)键。
(4)Cu与③的最高价氧化物对应的水化物的稀溶液反应的化学方程式为___________ 。

(2)③和④两种元素的非金属性强弱关系:③
(3)⑤和⑦两种元素组成的化合物中含有的化学键是
(4)Cu与③的最高价氧化物对应的水化物的稀溶液反应的化学方程式为
您最近一年使用:0次
2 . 合成氨以及氨催化氧化制硝酸的流程如图所示。
(1)“氧化”时,产生的主要气体为___________ (填“ ”或“NO”)。
”或“NO”)。
(2)物质A不可能为___________ (填“ ”或“
”或“ ”)。
”)。
(3)浓硝酸见光易分解,通常应保存在___________ (填“棕色”或“无色”)试剂瓶中。
(4)在一定条件下发生反应: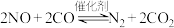 可以缓解大气中CO、NO污染问题。在1L密闭容器中加入2molNO、2molCO,在2min末测得
可以缓解大气中CO、NO污染问题。在1L密闭容器中加入2molNO、2molCO,在2min末测得 的物质的量为1mol。则:
的物质的量为1mol。则:
①2min末时NO的转化率为___________ ;
②催化剂___________ (填“可以”或“不可以”)提高反应物的转化率。

(1)“氧化”时,产生的主要气体为
 ”或“NO”)。
”或“NO”)。(2)物质A不可能为
 ”或“
”或“ ”)。
”)。(3)浓硝酸见光易分解,通常应保存在
(4)在一定条件下发生反应:
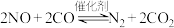 可以缓解大气中CO、NO污染问题。在1L密闭容器中加入2molNO、2molCO,在2min末测得
可以缓解大气中CO、NO污染问题。在1L密闭容器中加入2molNO、2molCO,在2min末测得 的物质的量为1mol。则:
的物质的量为1mol。则:①2min末时NO的转化率为
②催化剂
您最近一年使用:0次
3 . 小组同学探究 与水的反应。
与水的反应。
在注射器中充入 ,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。
,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。_______ 。
(2)进一步探究无色气体增多的原因。
【查阅资料】
ⅰ. 与水反应:
与水反应: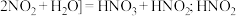 不稳定,分解产生气体。
不稳定,分解产生气体。
ⅱ. 能与KI反应生成
能与KI反应生成 。
。
【提出猜想】溶液A中含有 。
。
【进行实验】
①实验Ⅰ的目的是_______ 。
②实验Ⅱ中选择 溶液的依据是
溶液的依据是_______ (填字母)。
a. 具有氧化性,
具有氧化性, 具有还原性
具有还原性
b. 溶液有颜色,反应前后溶液颜色有变化
溶液有颜色,反应前后溶液颜色有变化
③甲同学认为,实验Ⅲ不能证明溶液A中含有 ,理由是
,理由是_______ 。
【实验反思】
本实验条件下, 与水反应生成了
与水反应生成了 ;
; 分解产生气体,且速率较小。
分解产生气体,且速率较小。
 与水的反应。
与水的反应。在注射器中充入
 ,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。
,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。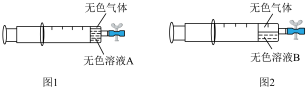
(2)进一步探究无色气体增多的原因。
【查阅资料】
ⅰ.
 与水反应:
与水反应: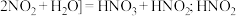 不稳定,分解产生气体。
不稳定,分解产生气体。ⅱ.
 能与KI反应生成
能与KI反应生成 。
。【提出猜想】溶液A中含有
 。
。【进行实验】
实验序号 | Ⅰ | Ⅱ | Ⅲ |
实验操作 |
|
|
|
实验现象 | 液体颜色变为浅红色 | 溶液颜色仍为无色 | 溶液颜色变为蓝色 |
②实验Ⅱ中选择
 溶液的依据是
溶液的依据是a.
 具有氧化性,
具有氧化性, 具有还原性
具有还原性b.
 溶液有颜色,反应前后溶液颜色有变化
溶液有颜色,反应前后溶液颜色有变化③甲同学认为,实验Ⅲ不能证明溶液A中含有
 ,理由是
,理由是【实验反思】
本实验条件下,
 与水反应生成了
与水反应生成了 ;
; 分解产生气体,且速率较小。
分解产生气体,且速率较小。
您最近一年使用:0次
4 . 无机物A~C在一定条件下的转化关系如图所示,A为淡黄色的固体化合物,B是地壳中含量最多的金属元素的单质,请回答下列问题:
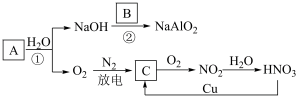
(1)写出A的化学式______ ,C的化学式______ 。
(2)写出稀HNO3与Cu反应生成C的离子方程式________ ;在该反应中,HNO3表现出酸性和强______ (填“氧化性”或“还原性”)。
(3)写出反应②的化学方程式________ 。

(1)写出A的化学式
(2)写出稀HNO3与Cu反应生成C的离子方程式
(3)写出反应②的化学方程式
您最近一年使用:0次
5 . 某实验小组的同学为探究一氧化氮的性质,欲选用下列实验装置来制取一氧化氮。
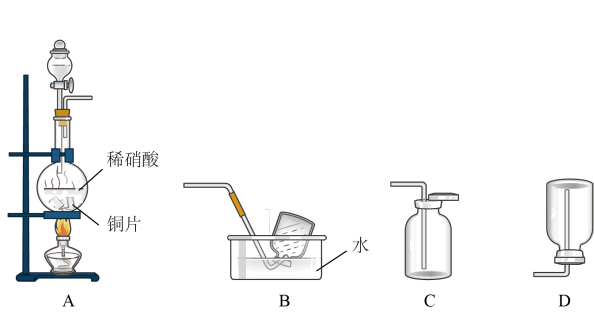
请回答下列问题:
(1)用上图中所示的装置制取一氧化氮,选用仪器连接的顺序应是 接
接___________ 。
(2)现欲用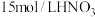 溶液配制
溶液配制 、
、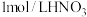 溶液时,要用到的仪器除烧杯、胶头滴管、玻璃棒、量筒外,还必须使用的一种玻璃仪器是
溶液时,要用到的仪器除烧杯、胶头滴管、玻璃棒、量筒外,还必须使用的一种玻璃仪器是___________ 。
(3)稀硝酸具有强氧化性,在常温下就可以和铜发生反应生成一氧化氮气体,写出该反应的化学方程式:___________ 。在实验过程中,该小组同学采用了微热的方法,目的是___________ 。
(4)实验开始时,该小组同学发现在烧瓶中有红棕色气体产生,请你用化学方程式来表示产生这种现象的原因:___________ 。
(5)一氧化氮和一氧化碳是汽车尾气中的主要污染物。目前,汽车尾气已成为许多大城市空气的主要污染源。治理汽车尾气中的 和
和 的一种方法是:在汽车的排气管上装一个催化转化装置,使
的一种方法是:在汽车的排气管上装一个催化转化装置,使 与
与 反应,生成
反应,生成 和
和 。反应的化学方程式是
。反应的化学方程式是___________ 。
(6)取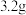 铜与一定体积、一定浓度的硝酸恰好完全反应,生成的混合气体(假设其组成仅为
铜与一定体积、一定浓度的硝酸恰好完全反应,生成的混合气体(假设其组成仅为 和
和 )在标准状况下的体积为
)在标准状况下的体积为 。则该硝酸中
。则该硝酸中 的物质的量为
的物质的量为___________  。
。

请回答下列问题:
(1)用上图中所示的装置制取一氧化氮,选用仪器连接的顺序应是
 接
接(2)现欲用
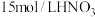 溶液配制
溶液配制 、
、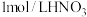 溶液时,要用到的仪器除烧杯、胶头滴管、玻璃棒、量筒外,还必须使用的一种玻璃仪器是
溶液时,要用到的仪器除烧杯、胶头滴管、玻璃棒、量筒外,还必须使用的一种玻璃仪器是(3)稀硝酸具有强氧化性,在常温下就可以和铜发生反应生成一氧化氮气体,写出该反应的化学方程式:
(4)实验开始时,该小组同学发现在烧瓶中有红棕色气体产生,请你用化学方程式来表示产生这种现象的原因:
(5)一氧化氮和一氧化碳是汽车尾气中的主要污染物。目前,汽车尾气已成为许多大城市空气的主要污染源。治理汽车尾气中的
 和
和 的一种方法是:在汽车的排气管上装一个催化转化装置,使
的一种方法是:在汽车的排气管上装一个催化转化装置,使 与
与 反应,生成
反应,生成 和
和 。反应的化学方程式是
。反应的化学方程式是(6)取
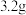 铜与一定体积、一定浓度的硝酸恰好完全反应,生成的混合气体(假设其组成仅为
铜与一定体积、一定浓度的硝酸恰好完全反应,生成的混合气体(假设其组成仅为 和
和 )在标准状况下的体积为
)在标准状况下的体积为 。则该硝酸中
。则该硝酸中 的物质的量为
的物质的量为 。
。
您最近一年使用:0次
解题方法
6 . 非金属单质A经如图所示的过程可转化为含氧酸D,已知D为强酸。请回答下列问题。

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①C的化学式是____________ ,D的化学式是____________ 。
②写出B转化为C的化学方程式____________________________________ 。
③在工业生产中,B气体大量排放,被雨水吸收后形成的______ 会污染环境。
④将适量的蔗糖放入烧杯中滴入几滴水,搅拌均匀;然后再加入适量D的浓溶液,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并生成含有B的刺激性气味气体。上述实验现象表明D的浓溶液具有____________ (填字母序号)。
A.酸性 B.吸水性 C.脱水性 D.强氧化性
(2)若A在常温下为气体,C是红棕色的气体。
①A的化学式是____________ ,D的化学式是____________ 。
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为_______ ;该反应_______ (填“属于”或“不属于”)氧化还原反应。
③将32.64 g铜与140 mL一定浓度的D溶液恰好完全反应,产生B和C的混合气体在标准状况下的体积为11.2 L,则该硝酸的浓度为____________ mol/L(计算结果精确至0.1)。

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①C的化学式是
②写出B转化为C的化学方程式
③在工业生产中,B气体大量排放,被雨水吸收后形成的
④将适量的蔗糖放入烧杯中滴入几滴水,搅拌均匀;然后再加入适量D的浓溶液,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并生成含有B的刺激性气味气体。上述实验现象表明D的浓溶液具有
A.酸性 B.吸水性 C.脱水性 D.强氧化性
(2)若A在常温下为气体,C是红棕色的气体。
①A的化学式是
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为
③将32.64 g铜与140 mL一定浓度的D溶液恰好完全反应,产生B和C的混合气体在标准状况下的体积为11.2 L,则该硝酸的浓度为
您最近一年使用:0次
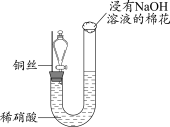
7 . 利用如下图所示装置进行铜与浓硝酸的实验(夹持装置略去)。回答下列问题:

(1)实验室中浓硝酸一般盛放在_______ 色试剂瓶中。
(2)仪器A的名称是_______ 。
(3)连接装置后,首先应检查装置的_______ 。
(4)反应开始后,铜丝逐渐变细,有红棕色气体产生。该反应的离子方程式为_______ 。
(5)NaOH溶液的作用是_______ 。

(1)实验室中浓硝酸一般盛放在
(2)仪器A的名称是
(3)连接装置后,首先应检查装置的
(4)反应开始后,铜丝逐渐变细,有红棕色气体产生。该反应的离子方程式为
(5)NaOH溶液的作用是
您最近一年使用:0次
解题方法
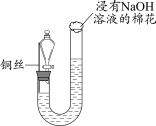
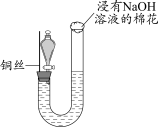
8 . 某同学研究铜与稀硝酸的反应,实验如下(夹持装置已略去,气密性良好)。
(1)HNO3中的氮元素为+5价,是氮元素的最高价态,HNO3具有_______ (填“氧化”或“还原”)性。
(2)步骤III中分液漏斗内的红棕色气体是_______ 。
(3)补全铜与稀硝酸反应的化学方程式:_______ 。_______ (写出一条即可)。
| 步骤I | 步骤II | 步骤III |
|
|
|
| 如图组装仪器并加入药品,分液漏斗旋塞关闭,U型管左侧无气体 | 将铜丝下移,一段时间后,U型管左侧产生无色气体,溶液逐渐变蓝,当液面低于铜丝时,反应逐渐停止 | 将铜丝上移,打开分液漏斗旋塞,U型管内气体进入分液漏斗立即变为红棕色,待气体全部进入分液漏斗后关闭旋塞 |
(2)步骤III中分液漏斗内的红棕色气体是
(3)补全铜与稀硝酸反应的化学方程式:
3Cu+8HNO3(稀)=3Cu(NO3)2+ _______↑+4H2O
_______↑+4H2O
您最近一年使用:0次
2023-01-17更新
|
222次组卷
|
2卷引用:北京市2022-2023学年高二上学期第二次合格考化学试题
9 . 已知A是空气中含量最高的一种气体,D是一种重要的无机化工原料,由A到D的转化过程如下图所示。
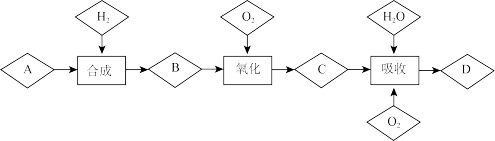
回答下列问题:
(1)物质A的电子式为_______ ,物质D的分子式为_______ 。
(2)“合成”需要在高温、高压和催化剂的条件下进行,其发生反应的化学方程式_______ 。
(3)“吸收”中通入过量O2的目的是_______ 。
(4)工业上贮存物质D的浓溶液可选择的罐体材料为(填标号)_______ 。
a.银 b.铜 c.铝 d.锌

回答下列问题:
(1)物质A的电子式为
(2)“合成”需要在高温、高压和催化剂的条件下进行,其发生反应的化学方程式
(3)“吸收”中通入过量O2的目的是
(4)工业上贮存物质D的浓溶液可选择的罐体材料为(填标号)
a.银 b.铜 c.铝 d.锌
您最近一年使用:0次
10 . 下图表示各物质之间的转化关系。已知:常温下B、D、F、G、I、J是气体,F、G是空气中的主要成分,D是一种碱性气体;A中阴、阳离子个数比是 ,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)
,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)

请按要求回答下列问题:
(1)A物质是_______ ;X物质是_______ ;K物质是_______ (均写化学式)。
(2)反应③的化学方程式是_______ 。
(3)反应①中产生标准状况下1.12L气体F,则转移的电子数目是_______ 。
(4)反应②的化学反应方程式为_______ ;作氧化剂的是_______ 。
(5)某小组同学用如图所示装置制取氨,并探究其性质。

①大试管中发生的反应的化学方程式是_______ 。
②请将方框中的收集装置补充完整_______ ,解释采用这种收集方法的原因是_______ 。
③甲同学用如图所示的装置进行尾气处理,乙同学认为不合理,其理由是:_______ 。

 ,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)
,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)
请按要求回答下列问题:
(1)A物质是
(2)反应③的化学方程式是
(3)反应①中产生标准状况下1.12L气体F,则转移的电子数目是
(4)反应②的化学反应方程式为
(5)某小组同学用如图所示装置制取氨,并探究其性质。

①大试管中发生的反应的化学方程式是
②请将方框中的收集装置补充完整
③甲同学用如图所示的装置进行尾气处理,乙同学认为不合理,其理由是:

您最近一年使用:0次