1 . 乙酰乙酸乙酯是一种重要的有机中间体,实验室制备乙酰乙酸乙酯的反应、装置示意图和有关数据如下:
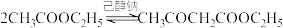 (乙酰乙酸乙酯)
(乙酰乙酸乙酯)
实验步骤:
ⅰ.向三颈烧瓶中加入4.0g钠、5.0g细砂和18mL二甲苯。加热使钠熔化,回流下搅拌5~6min,使其分散成小钠珠。静置冷却后,用倾析法除去上层液体。
ⅱ.迅速向三颈烧瓶中加入10mL环己烷、22.0g乙酸乙酯和极少量的乙醇,搅拌并加热,发生反应。
ⅲ.向反应后的体系中加入3mL乙醇,过滤。向滤液中加入50%乙酸至其呈弱酸性,再向其中加入饱和食盐水,分液。向有机层加入无水Na2SO4,过滤,蒸馏,收集到目标馏分10.4g。根据上述实验,下列说法不正确的是
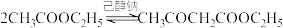 (乙酰乙酸乙酯)
(乙酰乙酸乙酯)
| 相对分子质量 | 沸点/℃ |
| |
| 乙醇 | 46 | 78 | |
| 乙酸乙酯 | 88 | 77 | |
| 乙酰乙酸乙酯 | 130 | 180.4 |
ⅰ.向三颈烧瓶中加入4.0g钠、5.0g细砂和18mL二甲苯。加热使钠熔化,回流下搅拌5~6min,使其分散成小钠珠。静置冷却后,用倾析法除去上层液体。
ⅱ.迅速向三颈烧瓶中加入10mL环己烷、22.0g乙酸乙酯和极少量的乙醇,搅拌并加热,发生反应。
ⅲ.向反应后的体系中加入3mL乙醇,过滤。向滤液中加入50%乙酸至其呈弱酸性,再向其中加入饱和食盐水,分液。向有机层加入无水Na2SO4,过滤,蒸馏,收集到目标馏分10.4g。根据上述实验,下列说法不正确的是
| A.步骤ⅰ中,细砂的作用是阻碍小颗粒钠聚结成大颗粒钠 |
| B.步骤ⅱ中,B处仪器应为球形冷凝管 |
| C.步骤ⅲ中,分液时乙酰乙酸乙酯粗品从下口流出 |
| D.步骤ⅲ中,蒸馏收集目标馏分时,温度计示数控制在180.4℃ |
您最近一年使用:0次
名校
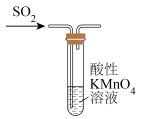
2 . 下列实验操作正确的是
|
|
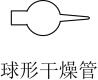
| A.验证SO2具有漂白性 | B.配制 NaOH溶液 NaOH溶液 |
|
|
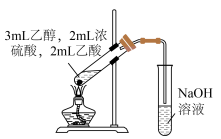
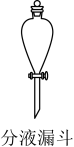
| C.苯萃取碘水中I2放出下层液体 | D.乙酸乙酯的制备和收集 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 下列实验室药品的保存或实验安全应急措施错误的是
| A.漂白粉要避光、密封保存在阴凉处 |
| B.浓溴水沾在皮肤上,先用大量水冲洗,再用酒精擦拭 |
| C.AgNO3溶液应当保存在棕色细口瓶中 |
| D.浓硫酸沾到皮肤上,先用大量水冲洗,然后涂抹稀NaOH溶液 |
您最近一年使用:0次
解题方法
4 . 某废催化剂含SiO2、ZnO、ZnS和CuS,欲“变废为宝”,实验室中从该废催化剂中回收锌和铜的一种流程如下图所示。
(1)在步骤①浸出反应中,生成气体的化学品标识是________(填标号)。
(2)下列叙述中涉及到与该流程中的“操作②”相同操作的是________
A.《肘后备急方》中治疟疾:“青蒿一握,以水升渍,绞取汁,尽服之”
B.《开宝本草》中获取硝酸钾:“冬月地上有霜,扫取以水淋汁后,乃煎炼而成”
C.《本草衍义》中精制砒霜:“将生砒就置火上,以器覆之,令砒烟上飞着覆器”
(3)步骤④中,获得晶体的实验操作步骤是________________ 、______________ 、过滤、洗涤、干燥。
(4)向盛有滤渣1的反应器中加入稀硫酸和过氧化氢溶液加热浸出,该过程应先加入的试剂为_______ ,步骤③中生成单质硫,写出该反应的离子方程式_________________ ,生成的铜离子对于过氧化氢的分解具有催化作用,其化学反应方程式为__________________ 。
(5)设计如图装置测定一定质量的废催化剂中硫化锌的含量。室温下,向恒压分液漏斗中加入足量0.5 mol/L H2SO4溶液,乙丙连通管中盛有饱和NaHS溶液,乙管实验前对应气体体积读数为V1 mL,甲中完全反应后乙管气体体积读数为V2 mL(V2>V1)。________________ 。
②若实验结束时,未调平乙管和丙管的液面,且丙管的液面高于乙管,所测得产品中硫化锌的含量________________ (填“偏高”或“偏低”)。
(6)已知该废催化剂中含12%的CuS,实验中称取20.0 g废催化剂最终得到4.0 gCuSO4·5H2O(M=250g/mol),则铜的回收率为________________ 。

(1)在步骤①浸出反应中,生成气体的化学品标识是________(填标号)。
A. | B. | C. | D. |
(2)下列叙述中涉及到与该流程中的“操作②”相同操作的是
A.《肘后备急方》中治疟疾:“青蒿一握,以水升渍,绞取汁,尽服之”
B.《开宝本草》中获取硝酸钾:“冬月地上有霜,扫取以水淋汁后,乃煎炼而成”
C.《本草衍义》中精制砒霜:“将生砒就置火上,以器覆之,令砒烟上飞着覆器”
(3)步骤④中,获得晶体的实验操作步骤是
(4)向盛有滤渣1的反应器中加入稀硫酸和过氧化氢溶液加热浸出,该过程应先加入的试剂为
(5)设计如图装置测定一定质量的废催化剂中硫化锌的含量。室温下,向恒压分液漏斗中加入足量0.5 mol/L H2SO4溶液,乙丙连通管中盛有饱和NaHS溶液,乙管实验前对应气体体积读数为V1 mL,甲中完全反应后乙管气体体积读数为V2 mL(V2>V1)。

②若实验结束时,未调平乙管和丙管的液面,且丙管的液面高于乙管,所测得产品中硫化锌的含量
(6)已知该废催化剂中含12%的CuS,实验中称取20.0 g废催化剂最终得到4.0 gCuSO4·5H2O(M=250g/mol),则铜的回收率为
您最近一年使用:0次
5 . 富马酸亚铁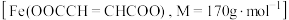 是一种治疗贫血的药物。其制备及纯度测定实验如下:
是一种治疗贫血的药物。其制备及纯度测定实验如下:
I.制备
步骤1:将 富马酸
富马酸 固体置于
固体置于 烧杯中,加水
烧杯中,加水 ,在加热搅拌下加入
,在加热搅拌下加入 溶液
溶液 ,使其
,使其 为
为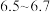 。
。
步骤2:将上述溶液转移至如图所示装置中(省略加热、搅拌和夹持装置),通 并加热一段时间后,维持温度100℃,缓慢滴加
并加热一段时间后,维持温度100℃,缓慢滴加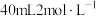 的
的 溶液,搅拌充分反应
溶液,搅拌充分反应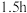 ;
; 。
。
Ⅱ.纯度测定
取 样品置于
样品置于 锥形瓶中,加入煮沸过的
锥形瓶中,加入煮沸过的 硫酸溶液
硫酸溶液 ,待样品完全溶解后,加入煮沸过的蒸馏水
,待样品完全溶解后,加入煮沸过的蒸馏水 和2滴邻二氮菲指示剂(邻二氮菲遇
和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色),立即用
呈无色),立即用 标准溶液滴定至终点(反应的离子方程式为
标准溶液滴定至终点(反应的离子方程式为 )。平行测定三次,消耗标准溶液的平均体积为
)。平行测定三次,消耗标准溶液的平均体积为 。
。
对于上述实验,下列说法正确的是
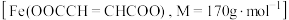 是一种治疗贫血的药物。其制备及纯度测定实验如下:
是一种治疗贫血的药物。其制备及纯度测定实验如下:I.制备
步骤1:将
 富马酸
富马酸 固体置于
固体置于 烧杯中,加水
烧杯中,加水 ,在加热搅拌下加入
,在加热搅拌下加入 溶液
溶液 ,使其
,使其 为
为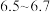 。
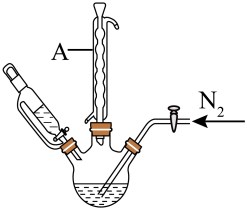
。步骤2:将上述溶液转移至如图所示装置中(省略加热、搅拌和夹持装置),通
 并加热一段时间后,维持温度100℃,缓慢滴加
并加热一段时间后,维持温度100℃,缓慢滴加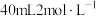 的
的 溶液,搅拌充分反应
溶液,搅拌充分反应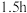 ;
;
 。
。Ⅱ.纯度测定
取
 样品置于
样品置于 锥形瓶中,加入煮沸过的
锥形瓶中,加入煮沸过的 硫酸溶液
硫酸溶液 ,待样品完全溶解后,加入煮沸过的蒸馏水
,待样品完全溶解后,加入煮沸过的蒸馏水 和2滴邻二氮菲指示剂(邻二氮菲遇
和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色),立即用
呈无色),立即用 标准溶液滴定至终点(反应的离子方程式为
标准溶液滴定至终点(反应的离子方程式为 )。平行测定三次,消耗标准溶液的平均体积为
)。平行测定三次,消耗标准溶液的平均体积为 。
。对于上述实验,下列说法正确的是
A.“步骤1”中发生反应的离子反应为 |
| B.为提高冷凝效果,仪器A可改用直形冷凝管 |
| C.锥形瓶溶液由红色变为无色即达到滴定终点 |
D.富马酸亚铁产品的纯度为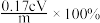 |
您最近一年使用:0次
6 . 富马酸亚铁[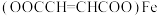 ]又称富马铁,是一种安全、高效的有机营养补铁剂,可由富马酸(
]又称富马铁,是一种安全、高效的有机营养补铁剂,可由富马酸( )与硫酸亚铁制取,其制备装置(夹持装置略)如图所示。
)与硫酸亚铁制取,其制备装置(夹持装置略)如图所示。
②柠檬酸易溶于水和乙醇,酸性较强,具有强还原性。
③富马酸亚铁易溶于水,性质稳定,难溶于无水乙醇。
实验步骤如下:
Ⅰ.打开活塞 、
、 ,关闭
,关闭 ,向d中通入气体,待d中空气被排尽后,将b中溶液压入d中。
,向d中通入气体,待d中空气被排尽后,将b中溶液压入d中。
Ⅱ.在50℃恒温条件下用电磁搅拌器不断搅拌,然后向d中滴加 溶液,调节溶液
溶液,调节溶液 ,使反应物充分反应。
,使反应物充分反应。
Ⅲ.反应完成后,向d中反应混合液中加入无水乙醇,生成白色沉淀,将沉淀过滤、洗涤得粗产品,将粗产品纯化后得精品。
回答下列问题:
(1)仪器a的名称是_______ ,相对于c,仪器a的优点是_______ 。
(2)步骤Ⅰ中将b中溶液压入d中的操作是_______ 。
(3)反应混合液中加入柠檬酸的作用是_______ 。
(4)写出步骤Ⅱ中生成富马酸亚铁的化学方程式:_______ 。
(5)步骤Ⅲ中加入无水乙醇的作用是_______ ,沉淀洗涤时用_______ 作洗涤剂。
(6)若富马酸的投料量为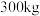 ,产出纯品
,产出纯品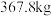 ,则富马酸亚铁的产率为
,则富马酸亚铁的产率为_______ (保留两位有效数字)。
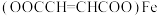 ]又称富马铁,是一种安全、高效的有机营养补铁剂,可由富马酸(
]又称富马铁,是一种安全、高效的有机营养补铁剂,可由富马酸( )与硫酸亚铁制取,其制备装置(夹持装置略)如图所示。
)与硫酸亚铁制取,其制备装置(夹持装置略)如图所示。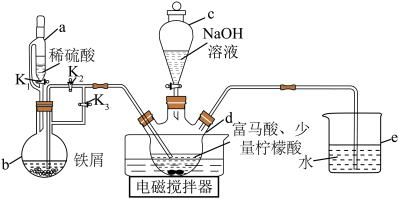
②柠檬酸易溶于水和乙醇,酸性较强,具有强还原性。
③富马酸亚铁易溶于水,性质稳定,难溶于无水乙醇。
实验步骤如下:
Ⅰ.打开活塞
 、
、 ,关闭
,关闭 ,向d中通入气体,待d中空气被排尽后,将b中溶液压入d中。
,向d中通入气体,待d中空气被排尽后,将b中溶液压入d中。Ⅱ.在50℃恒温条件下用电磁搅拌器不断搅拌,然后向d中滴加
 溶液,调节溶液
溶液,调节溶液 ,使反应物充分反应。
,使反应物充分反应。Ⅲ.反应完成后,向d中反应混合液中加入无水乙醇,生成白色沉淀,将沉淀过滤、洗涤得粗产品,将粗产品纯化后得精品。
回答下列问题:
(1)仪器a的名称是
(2)步骤Ⅰ中将b中溶液压入d中的操作是
(3)反应混合液中加入柠檬酸的作用是
(4)写出步骤Ⅱ中生成富马酸亚铁的化学方程式:
(5)步骤Ⅲ中加入无水乙醇的作用是
(6)若富马酸的投料量为
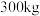 ,产出纯品
,产出纯品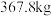 ,则富马酸亚铁的产率为
,则富马酸亚铁的产率为
您最近一年使用:0次
名校
解题方法
7 . 利用下列仪器(夹持装置略)和用品及试剂能达到相应实验目的的是
| 选项 | 实验目的 | 仪器和用品 | 试剂 |
| A | 检验 的存在 的存在 | 试管、滴瓶 | 稀硝酸、 溶液、待检溶液 溶液、待检溶液 |
| B | 实验室制备氯气 | 圆底烧瓶、分液漏斗、集气瓶、烧杯、导管、酒精灯、橡皮塞、陶土网 | 浓盐酸、 、NaOH溶液 、NaOH溶液 |
| C | 检验 的存在 的存在 | 烧杯、酒精灯、洁净的铁丝 | 盐酸、待检溶液 |
| D | 配制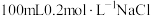 溶液 溶液 | 托盘天平、药匙、烧杯、量筒、玻璃棒、100mL容量瓶 | 蒸馏水、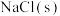 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 某粗苯甲酸样品中含有少量NaCl和泥沙,某实验小组提纯苯甲酸的实验流程如图(已知:常温下苯甲酸易溶于乙醇,25℃和75℃时苯甲酸在水中的溶解度分别为0.34g和2.2g)。下列说法不正确的是

| A.“过滤1”需趁热,以减少苯甲酸的析出 |
| B.“溶解”、“过滤”、“洗涤”操作中均使用了玻璃棒 |
| C.“洗涤”时,选用乙醇作洗涤剂有利于快速干燥 |
| D.将洗涤后的晶体铺在干燥的滤纸上,晾干后称量 |
您最近一年使用:0次
9 . 下列实验室废弃物处理得当的是
| A.废弃的钠屑分批加入乙醇中溶解,再加水稀释、用酸中和后方可排放 |
| B.向铜和浓硫酸反应后的废液中加水稀释、用碱中和后方可排放 |
| C.用适量浓氨水清洗银镜反应后的试管可得到能循环使用的银氨溶液 |
| D.废弃的白磷固体用纸包裹后直接放入垃圾桶中 |
您最近一年使用:0次