5. 为探究铁及其化合物的性质,某班几个兴趣小组做了以下实验。
(1)甲组同学利用下列试剂:铜粉、0.1mol/LFeCl
3溶液、0.1mol/LFeCl
2溶液、KSCN溶液、新制氯水等,探究Fe
2+、Fe
3+的性质,设计实验方案进行实验,完成下列表格。
| 探究内容 | 实验方案 | 实验现象 | 写出离子方程式 |
| 探究Fe2+具有还原性 | 取少量FeCl2溶液,加入少量KSCN溶液后,再往溶液中加入少量___________。 | 溶液先不变红,后变为血红色。 | Fe2+发生的反应:___________ |
| 探究Fe3+具有氧化性 | ①取少量FeCl3溶液,加入足量___________后,振荡、静置,再往溶液中加入少量KSCN | 溶液不变为血红色。 | Fe3+发生的反应:___________ |
| ②取少量FeCl3溶液,通入足量SO2,振荡、静置后滴入BaCl2溶液 | 溶液逐渐由黄色变为浅绿色,滴入BaCl2溶液,有白色沉淀生成 | Fe3+与SO2发生的反应:___________ |
上述反应①可用于刻蚀印刷电路板,若将反应设计为原电池(如图),可加快刻蚀的速率,请在图中补充相关信息。
___________
(2)乙组同学为了制备Fe(OH)
2沉淀且保持一段时间不变色,尝试用如图所示的装置进行实验。
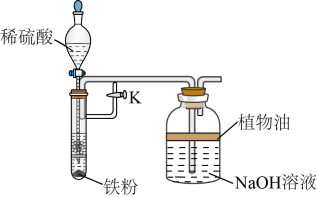
①Fe(OH)
2暴露在空气中的颜色变化为
___________,原因是
___________(用化学方程式表示)。
②实验时,先
___________(填“打开”或“关闭”)止水夹K,然后打开分液漏斗的活塞,一段时间后,
___________(填“打开”或“关闭”)K。
(3)向300mL0.2mol/L的FeSO
4溶液中加入足量的NaOH溶液,沉淀经过滤、加热灼烧至质量不再变化后,得到的固体质量为
___________g。