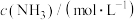人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第四节 化学反应的调控 方法帮
全国
高二
课后作业
2020-10-06
267次
整体难度:
适中
考查范围:
化学反应原理
人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第四节 化学反应的调控 方法帮
全国
高二
课后作业
2020-10-06
267次
整体难度:
适中
考查范围:
化学反应原理
一、解答题 添加题型下试题
解答题-原理综合题
|
适中(0.65)
解题方法
1. 哈伯发明用氮气和氢气合成氨的方法,获得了1918年诺贝尔化学奖。其原理为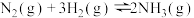
 ,
,
________ (填“>”“<”或“=”)0。
(1)下列关于工业合成氨的说法不正确的是__________ (填标号)。
A.因为 ,所以该反应一定能自发进行
,所以该反应一定能自发进行
B.采用高压是为了增大反应速率,但会使反应物的转化率降低
C.在高温下进行是为了提高反应物的转化率
D.使用催化剂增大反应速率是因为催化剂降低了反应的活化能
(2)在恒温恒容密闭容器中进行合成氨的反应,下列能说明该反应已达到平衡状态的是________ (填标号)。
a.容器内 、
、 、
、 的浓度之比为1∶3∶2
的浓度之比为1∶3∶2
b.
c.容器内压强保持不变
d.混合气体的密度保持不变
(3)工业上合成氨的部分工艺流程如图:
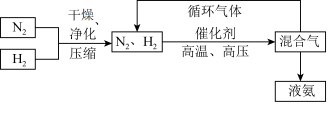
请用平衡移动原理解释在工艺流程中及时分离出氨气和将 分离后的原料气循环使用的原因
分离后的原料气循环使用的原因___________________ 。
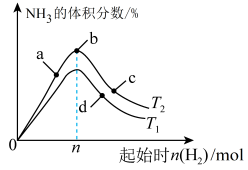
(4)某科研小组研究在其他条件不变的情况下,改变起始时氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示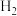 的物质的量)。
的物质的量)。
①图中 和
和 的关系:
的关系:
________ (填“>”“<”或“=”) 。
。
②a、b、c、d四点所处的平衡状态中, 的转化率最高的是
的转化率最高的是__________ (填字母)。
(5)恒温下,向一个4L的密闭容器中充入5.2mol 和2mol
和2mol ,反应过程中对
,反应过程中对 的浓度进行测定,得到的数据如表所示:
的浓度进行测定,得到的数据如表所示:
①此条件下该反应的化学平衡常数
________ 。
②若维持容器容积不变,温度不变,向原平衡体系中加入 、
、 和
和 各4mol,化学平衡将向
各4mol,化学平衡将向_______ (填“正”或“逆”)反应方向移动。
(6)已知: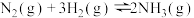
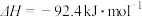
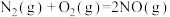
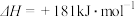
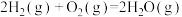
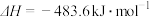
写出氨气催化氧化生成NO和水蒸气的热化学方程式________________ 。
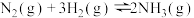
 ,
,
(1)下列关于工业合成氨的说法不正确的是
A.因为
 ,所以该反应一定能自发进行
,所以该反应一定能自发进行B.采用高压是为了增大反应速率,但会使反应物的转化率降低
C.在高温下进行是为了提高反应物的转化率
D.使用催化剂增大反应速率是因为催化剂降低了反应的活化能
(2)在恒温恒容密闭容器中进行合成氨的反应,下列能说明该反应已达到平衡状态的是
a.容器内
 、
、 、
、 的浓度之比为1∶3∶2
的浓度之比为1∶3∶2b.

c.容器内压强保持不变
d.混合气体的密度保持不变
(3)工业上合成氨的部分工艺流程如图:

请用平衡移动原理解释在工艺流程中及时分离出氨气和将
 分离后的原料气循环使用的原因
分离后的原料气循环使用的原因(4)某科研小组研究在其他条件不变的情况下,改变起始时氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示
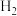 的物质的量)。
的物质的量)。①图中
 和
和 的关系:
的关系:
 。
。②a、b、c、d四点所处的平衡状态中,
 的转化率最高的是
的转化率最高的是
(5)恒温下,向一个4L的密闭容器中充入5.2mol
 和2mol
和2mol ,反应过程中对
,反应过程中对 的浓度进行测定,得到的数据如表所示:
的浓度进行测定,得到的数据如表所示:时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |

②若维持容器容积不变,温度不变,向原平衡体系中加入
 、
、 和
和 各4mol,化学平衡将向
各4mol,化学平衡将向(6)已知:
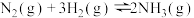
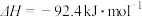
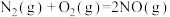
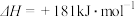
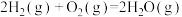
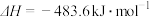
写出氨气催化氧化生成NO和水蒸气的热化学方程式
您最近一年使用:0次
2020-10-05更新
|
252次组卷
|
3卷引用:人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第四节 化学反应的调控 方法帮
人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第四节 化学反应的调控 方法帮(已下线)专题2.4 化学反应的调控(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)云南省昭通市2022-2023学年高二下学期期中考试化学试题
解答题-原理综合题
|
较易(0.85)
名校
解题方法
2. 合成氨反应 ,在
,在 时,
时, ,
, 。
。
(1)从平衡常数来看,合成氨反应的限度已经很大了,为什么还需要使用催化剂?_______ 。
(2) 、
、 时,在
时,在 的密闭容器中充入
的密闭容器中充入 、
、 和
和 ,开始的瞬间,反应向
,开始的瞬间,反应向_________ (填“正”或“逆”)反应方向进行,反应进行 后体系
后体系_________ (填“吸收”或“放出”)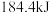 能量,容器内压强与初始压强之比为
能量,容器内压强与初始压强之比为_________ 。
(3)从开始至 时,用
时,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为_________ 。
 ,在
,在 时,
时, ,
, 。
。(1)从平衡常数来看,合成氨反应的限度已经很大了,为什么还需要使用催化剂?
(2)
 、
、 时,在
时,在 的密闭容器中充入
的密闭容器中充入 、
、 和
和 ,开始的瞬间,反应向
,开始的瞬间,反应向 后体系
后体系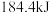 能量,容器内压强与初始压强之比为
能量,容器内压强与初始压强之比为(3)从开始至
 时,用
时,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为
您最近一年使用:0次
2020-09-19更新
|
282次组卷
|
5卷引用:鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化—工业合成氨
鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化—工业合成氨人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第四节 化学反应的调控 方法帮(已下线)第二章 化学反应速率与化学平衡(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)海南省海口市第四中学2020-2021学年高二上学期第一次月考化学试题湖北随州市第一中学2020-2021学年高二上学期期中考试化学试题
二、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
解题方法
3. 工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7% O2:11% N2:82%)。
(1)SO2的氧化反应是___ 反应(填“吸热”或“放热”)。
(2)根据图中所给信息,你认为工业上将SO2转化为SO3的适宜条件是___ 。
(3)选择适宜的催化剂,是否可以提高SO2的转化率?___ (填“是”或“否”)。
(4)若保持温度和容积不变,平衡后通入氧气,再达平衡时则SO2浓度___ 。(填“增大”或“减小”)
(5)若保持温度和压强不变,平衡后通入He气,SO3的含量___ 。(填“增大”或“减小”)
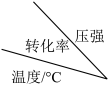 | 0.1个大气压 | 0.5个大气压 | 1个大气压 | 10个大气压 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
(2)根据图中所给信息,你认为工业上将SO2转化为SO3的适宜条件是
(3)选择适宜的催化剂,是否可以提高SO2的转化率?
(4)若保持温度和容积不变,平衡后通入氧气,再达平衡时则SO2浓度
(5)若保持温度和压强不变,平衡后通入He气,SO3的含量
您最近一年使用:0次
2020-01-17更新
|
136次组卷
|
2卷引用:海南省海南中学2019-2020学年高二上学期期末考试化学试题
三、单选题 添加题型下试题
单选题
|
适中(0.65)
4. 下图为工业合成氨的流程图。图中为提高原料转化率而采取的措施是


| A.①②③ | B.①③⑤ | C.②④⑤ | D.②③④ |
【知识点】 化学平衡的移动及其影响因素 转化率的相关计算及判断解读
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学反应原理
试卷题型(共 4题)
题型
数量
解答题
2
填空题
1
单选题
1
试卷难度
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、解答题 | |||
| 1 | 0.65 | 盖斯定律与热化学方程式 化学平衡常数的有关计算 与物质百分含量变化有关图像的分析 合成氨条件的选择 | 原理综合题 |
| 2 | 0.85 | 化学反应速率计算 化学平衡的移动及其影响因素 化学平衡常数的影响因素及应用 化学平衡常数的有关计算 | 原理综合题 |
| 二、填空题 | |||
| 3 | 0.65 | 浓度对化学平衡移动的影响 温度对化学平衡移动的影响 压强对化学平衡移动的影响 化学反应条件的控制及其应用 | |
| 三、单选题 | |||
| 4 | 0.65 | 化学平衡的移动及其影响因素 转化率的相关计算及判断 | |