已知下列热化学方程式:
①H2(g)+ O2(g)=H2O(l) ΔH=-285kJ/mol
O2(g)=H2O(l) ΔH=-285kJ/mol
②H2(g)+ O2(g)=H2O(g) ΔH=-241.8kJ/mol
O2(g)=H2O(g) ΔH=-241.8kJ/mol
③C(s)+ O2(g)=CO(g) ΔH=-110.4 kJ/mol
O2(g)=CO(g) ΔH=-110.4 kJ/mol
④C(s)+ O2(g)=CO2(g) ΔH=-393.5 kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是___________ 。
(2)C的燃烧热为_________________ 。
(3)燃烧10g H2生成液态水,放出的热量为_________________ 。
(4)CO燃烧的热化学方程式为________________________________________ 。
①H2(g)+
 O2(g)=H2O(l) ΔH=-285kJ/mol
O2(g)=H2O(l) ΔH=-285kJ/mol②H2(g)+
 O2(g)=H2O(g) ΔH=-241.8kJ/mol
O2(g)=H2O(g) ΔH=-241.8kJ/mol③C(s)+
 O2(g)=CO(g) ΔH=-110.4 kJ/mol
O2(g)=CO(g) ΔH=-110.4 kJ/mol④C(s)+ O2(g)=CO2(g) ΔH=-393.5 kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是
(2)C的燃烧热为
(3)燃烧10g H2生成液态水,放出的热量为
(4)CO燃烧的热化学方程式为
更新时间:2020-04-15 09:09:22
|
相似题推荐
【推荐1】化工生产中用烷烃和氧气或水蒸气反应可得到以 和
和 为主的混合气体,这种混合气体可用于生产甲醇或合成氨。对甲烷而言,有以下两个主要反应:
为主的混合气体,这种混合气体可用于生产甲醇或合成氨。对甲烷而言,有以下两个主要反应:
①

②

(1)反应②中参加反应的 与
与 的总能量
的总能量__________ (填“大于”“小于”或“等于”)生成的 与
与 的总能量。
的总能量。
(2)若氧气和水蒸气的混合气体中氧气的物质的量分数为 ,且甲烷恰好与二者完全反应,请填写下列空白:
,且甲烷恰好与二者完全反应,请填写下列空白:
(3)若某化工厂生产中反应的能量在利用过程中不计耗损,为使能量实现零排放和零补充,则进料气中水蒸气与空气( 的体积分数为
的体积分数为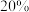 )的体积之比为
)的体积之比为__________ 。
 和
和 为主的混合气体,这种混合气体可用于生产甲醇或合成氨。对甲烷而言,有以下两个主要反应:
为主的混合气体,这种混合气体可用于生产甲醇或合成氨。对甲烷而言,有以下两个主要反应:①


②


(1)反应②中参加反应的
 与
与 的总能量
的总能量 与
与 的总能量。
的总能量。(2)若氧气和水蒸气的混合气体中氧气的物质的量分数为
 ,且甲烷恰好与二者完全反应,请填写下列空白:
,且甲烷恰好与二者完全反应,请填写下列空白:| 序号 |  | 与 反应的 反应的 | 与 反应的 反应的 | 总反应的 |
| I | 0.2 |  | ||
| II | 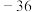 | 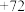 |
(3)若某化工厂生产中反应的能量在利用过程中不计耗损,为使能量实现零排放和零补充,则进料气中水蒸气与空气(
 的体积分数为
的体积分数为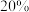 )的体积之比为
)的体积之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1) CO2与NH3反应可合成化肥尿素。已知:
①2NH3(g)+CO2(g) = NH2CO2NH4(s) ΔH= -159.5kJ•mol-1
②NH2CO2NH4(s) = CO(NH2)2(s)+H2O(g) ΔH= +116.5kJ•mol-1
③H2O(l) = H2O(g) ΔH= +44.0kJ•mol-1
写出CO2与NH3合成尿素[CO(NH2)2]和液态水的热化学反应方程式_____
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当1mol Cl2参与反应时释放145kJ的热量,写出这个反应逆反应的热化学方程式:______ 。
(3)下图是1mol NO2(g)与1mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________ (填“增大”“减小”或“不变”,下同),ΔH的变化是________ 。
(4)已知H—H键、N≡N键、N-H键的键能如下表所示:
则反应N2(g)+3H2(g)=2NH3(g)的 ΔH=________ 。
①2NH3(g)+CO2(g) = NH2CO2NH4(s) ΔH= -159.5kJ•mol-1
②NH2CO2NH4(s) = CO(NH2)2(s)+H2O(g) ΔH= +116.5kJ•mol-1
③H2O(l) = H2O(g) ΔH= +44.0kJ•mol-1
写出CO2与NH3合成尿素[CO(NH2)2]和液态水的热化学反应方程式
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当1mol Cl2参与反应时释放145kJ的热量,写出这个反应逆反应的热化学方程式:
(3)下图是1mol NO2(g)与1mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是

(4)已知H—H键、N≡N键、N-H键的键能如下表所示:
| 化学键 | H-H | N≡N | N-H |
| 键能/(kJ·mol-1) | 436 | 946 | 391 |
则反应N2(g)+3H2(g)=2NH3(g)的 ΔH=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】试从化学键的角度理解化学反应中的能量变化。(以2H2+O2=2H2O为例说明),已知:E反表示反应物(2H2+O2)所具有的总能量,E生表示生成物(2H2O)所具有的总能量。又知:拆开1moL H2中的化学键需要吸收436kJ能量,拆开1moL O2中的化学键需要吸收496kJ能量,形成水分子中的1moLH—O键能够释放463KJ能量。
(1)从微观角度看:断裂反应物中的化学键吸收的总能量为E吸=_______ kJ;形成生成物中的化学键放出的总能量为=________ kJ。所以该反应要_____ (填“吸收”或“放出”)能量,能量变化值的大小△E=_______ kJ(填数值)
(2)由图可知,化学反应的本质是_____ 化学反应中能量变化的主要原因是_____ (从总能量说明)
(1)从微观角度看:断裂反应物中的化学键吸收的总能量为E吸=
(2)由图可知,化学反应的本质是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某种发动机燃料由A、B两种物质混合而成,A、B两种物质含有C、H、O三种元素中的两种或三种。已知常温下A、B及CO、H2的燃烧热如下:
A、B按不同比例混合的燃料91.2g,在足量的氧气中燃烧时,放出的热量Q与B的物质的量分数x的关系如右图。

(1)A、B的相对分子质量为A________ ,B_______ 。
(2)等物质的量的A、B混合的燃料73g,在160LO2中完全燃烧,得到104L气体,通过碱石灰吸收后剩余3.2L(气体体积均在标准状况下测定)。由此可推得混合物中N(C)∶N(H)∶N(O)=__________ ,A分子式为_________ ,B分子式为_________ 。
(3)1mol等物质的量的A、B混合的燃料,在一定量的氧气中燃烧,放出热量2980kJ,则反应中生成CO_________ mol。
| 物 质 | A | B | CO | H2 |
| 燃烧热/kJ·mol-1 | 725 | 5518 | 283 | 286 |
A、B按不同比例混合的燃料91.2g,在足量的氧气中燃烧时,放出的热量Q与B的物质的量分数x的关系如右图。

(1)A、B的相对分子质量为A
(2)等物质的量的A、B混合的燃料73g,在160LO2中完全燃烧,得到104L气体,通过碱石灰吸收后剩余3.2L(气体体积均在标准状况下测定)。由此可推得混合物中N(C)∶N(H)∶N(O)=
(3)1mol等物质的量的A、B混合的燃料,在一定量的氧气中燃烧,放出热量2980kJ,则反应中生成CO
您最近一年使用:0次
【推荐2】CH4和CO2是引起温室效应的常见气体,CH4超干重整CO2是现在减少温室气体的一种有效方式,回答下面问题:
(1)实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式的书写正确的是_______ 。
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol-1
②CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
④2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
A.仅有②④ B.仅有④ C.仅有②③④ D.全部符合要求
(2)在25℃、101 kPa时,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5 kJ·mol-1、285.8 kJ·mol-1、870.3 kJ·mol-1,则2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=________ kJ·mol-1
(3)Ⅰ.CH4超干重整CO2过程中的能量变化图象如下图:
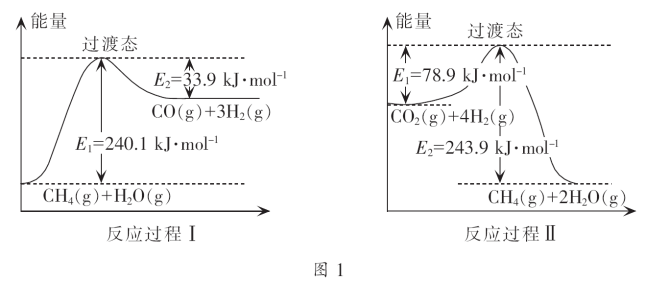
反应过程Ⅰ中发生的活化能是_______ kJ·mol-1,该反应的热化学方程式是______________ 。
反应过程Ⅱ中,CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH=____________ kJ·mol-1
Ⅱ.CH4在某催化剂作用下超干重整CO2的转化如图2所示:
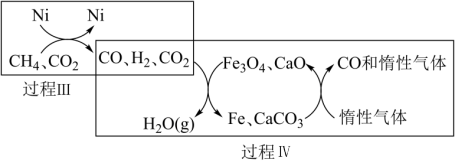
图2
①关于上述过程Ⅳ的说法不正确的是_____________ (填字母)。
a.实现了含碳物质与含氢物质的分离
b.可表示为CO2+H2=H2O(g)+CO
c.CO未参与反应
d.Fe3O4、CaO为催化剂,降低了反应的ΔH
②写出过程Ⅲ的热化学方程式为:___________________ 。
(1)实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式的书写正确的是
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol-1
②CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
④2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
A.仅有②④ B.仅有④ C.仅有②③④ D.全部符合要求
(2)在25℃、101 kPa时,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5 kJ·mol-1、285.8 kJ·mol-1、870.3 kJ·mol-1,则2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=
(3)Ⅰ.CH4超干重整CO2过程中的能量变化图象如下图:

反应过程Ⅰ中发生的活化能是
反应过程Ⅱ中,CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH=
Ⅱ.CH4在某催化剂作用下超干重整CO2的转化如图2所示:

图2
①关于上述过程Ⅳ的说法不正确的是
a.实现了含碳物质与含氢物质的分离
b.可表示为CO2+H2=H2O(g)+CO
c.CO未参与反应
d.Fe3O4、CaO为催化剂,降低了反应的ΔH
②写出过程Ⅲ的热化学方程式为:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)5.7g汽油(主要成分为C8H18,相对分子质量为114)完全燃烧生成液态水和CO2,放出275.9kJ的热量,则汽油的燃烧热为___________ ;
(2)已知:2H2(g)+ O2(g)=2H2O(g) △H=-483.6kJ/mol
H2O(l)= H2O(g) △H=+44kJ/mol
①写出H2与O2反应生成液态水时的热化学方程式____________ ;
②在通常情况下,若要得到857.4kJ的热量,需H2的质量为________ ,这些H2在标况下的体积为______ 。
(2)已知:2H2(g)+ O2(g)=2H2O(g) △H=-483.6kJ/mol
H2O(l)= H2O(g) △H=+44kJ/mol
①写出H2与O2反应生成液态水时的热化学方程式
②在通常情况下,若要得到857.4kJ的热量,需H2的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】研究燃料的燃烧效率和对污染气体产物的无害化处理,对于防止大气污染有重要意义。
⑴将煤转化为清洁气体燃料。已知:
H2(g)+1/2O2(g) = H2O(g) H= −242.0 kJ/mol
H= −242.0 kJ/mol
C(s)+1/2O2(g) = CO(g) H= −110.0 kJ/mol
H= −110.0 kJ/mol
①写出焦炭与水蒸气反应制H2和CO的热化学方程式___________________________ 。
②已知在101kPa时,CO、 H2和CH4的燃烧热分别为283kJ/mol、286 kJ/mol和892kJ/mol,则反应CH4(g)+ H2O(g) CO(g)+3H2(g)△H=
CO(g)+3H2(g)△H=______________ 。
⑵已知一定温度和压强下,由H2和CO反应合成优质燃料甲醇:
CO(g)+2H2(g) CH3OH(g)△H=-91kJ/mol
CH3OH(g)△H=-91kJ/mol
①在相同条件下要想得到182kJ热量,加入各物质的物质的量可能是_____________ 。
A.2mol CO和4mol H2 B.2mol CO、4mol H2和1mol CH3OH(g)
C.4mol CO和4mol H2 D.4mol CO和6mol H2
②将1mol CO和2mol H2充入一密闭容器中,保持恒温恒压时进行反应,达到平衡时,测得CO的转化率为20%,反应达到平衡时的热量变化是_______________ (填“吸收”或“放出”)_____________ kJ热量。
⑶用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1 ①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2 ②
若1 mol CH4还原NO2至N2,整个过程中放出的热量为867 kJ,则ΔH2=______ 。
⑴将煤转化为清洁气体燃料。已知:
H2(g)+1/2O2(g) = H2O(g)
 H= −242.0 kJ/mol
H= −242.0 kJ/molC(s)+1/2O2(g) = CO(g)
 H= −110.0 kJ/mol
H= −110.0 kJ/mol①写出焦炭与水蒸气反应制H2和CO的热化学方程式
②已知在101kPa时,CO、 H2和CH4的燃烧热分别为283kJ/mol、286 kJ/mol和892kJ/mol,则反应CH4(g)+ H2O(g)
 CO(g)+3H2(g)△H=
CO(g)+3H2(g)△H=⑵已知一定温度和压强下,由H2和CO反应合成优质燃料甲醇:
CO(g)+2H2(g)
 CH3OH(g)△H=-91kJ/mol
CH3OH(g)△H=-91kJ/mol①在相同条件下要想得到182kJ热量,加入各物质的物质的量可能是
A.2mol CO和4mol H2 B.2mol CO、4mol H2和1mol CH3OH(g)
C.4mol CO和4mol H2 D.4mol CO和6mol H2
②将1mol CO和2mol H2充入一密闭容器中,保持恒温恒压时进行反应,达到平衡时,测得CO的转化率为20%,反应达到平衡时的热量变化是
⑶用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1 ①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2 ②
若1 mol CH4还原NO2至N2,整个过程中放出的热量为867 kJ,则ΔH2=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)实验测得常温下16 g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25 kJ的热量,试写出甲醇燃烧热的热化学方程式:_______ 。
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。已知反应:N2(g)+3H2(g)⇌2NH3(g) △H=a kJ/mol。有关键能数据如下:
试根据表中所列键能数据估算a的数值_______ 。
(3)用盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算。已知:
C(s,石墨)+O2(g)=CO2(g) △H1=-393.5 kJ/mol
2H2(g)+O2(g)=2H2O(l) △H2=-571.6 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2599 kJ/mol
请写出由C(s,石墨)和H2(g)生成1 mol C2H2(g)的热化学方程式:_______ 。
(4)某金属氧化物的化学式为M2O,电子总数为30,已知氧原子核内有8个中子,M2O的相对分子质量为62,则M原子核内中子数为_______ 。
(1)实验测得常温下16 g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25 kJ的热量,试写出甲醇燃烧热的热化学方程式:
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。已知反应:N2(g)+3H2(g)⇌2NH3(g) △H=a kJ/mol。有关键能数据如下:
| 化学键 | H-H | N-H | N≡N |
| 键能(kJ/mol) | 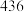 | 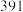 | 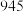 |
试根据表中所列键能数据估算a的数值
(3)用盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算。已知:
C(s,石墨)+O2(g)=CO2(g) △H1=-393.5 kJ/mol
2H2(g)+O2(g)=2H2O(l) △H2=-571.6 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2599 kJ/mol
请写出由C(s,石墨)和H2(g)生成1 mol C2H2(g)的热化学方程式:
(4)某金属氧化物的化学式为M2O,电子总数为30,已知氧原子核内有8个中子,M2O的相对分子质量为62,则M原子核内中子数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】按要求写热化学方程式:
(1)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式_______
(2)已知在25℃、101kPa下,1g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7kJ的热量,试写出乙醇燃烧热的热化学方程式_______
(3)1.7gNH3(g)发生催化氧化反应生成气态产物,放出22.67kJ的热量:_______ 。
(4)在25℃,101kPa下,已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则2molNH3完全分解生成N2与H2时,对应的热化学方程式为_______ ;
(5)已知: ;
;
 ;
;
 计算25℃时,由C(石墨,s)和H2(g)反应生成C2H2(g)的热化学方程式为
计算25℃时,由C(石墨,s)和H2(g)反应生成C2H2(g)的热化学方程式为_______ 。
(6)已知: ;1g液态水变成气态水要吸收2.44kJ的热量,则H2(g)燃烧生成H2O(l)的热化学方程式为
;1g液态水变成气态水要吸收2.44kJ的热量,则H2(g)燃烧生成H2O(l)的热化学方程式为_______
(1)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式
(2)已知在25℃、101kPa下,1g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7kJ的热量,试写出乙醇燃烧热的热化学方程式
(3)1.7gNH3(g)发生催化氧化反应生成气态产物,放出22.67kJ的热量:
(4)在25℃,101kPa下,已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则2molNH3完全分解生成N2与H2时,对应的热化学方程式为
(5)已知:
 ;
; ;
; 计算25℃时,由C(石墨,s)和H2(g)反应生成C2H2(g)的热化学方程式为
计算25℃时,由C(石墨,s)和H2(g)反应生成C2H2(g)的热化学方程式为(6)已知:
 ;1g液态水变成气态水要吸收2.44kJ的热量,则H2(g)燃烧生成H2O(l)的热化学方程式为
;1g液态水变成气态水要吸收2.44kJ的热量,则H2(g)燃烧生成H2O(l)的热化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】已知下列反应:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) ΔH=-266 kJ·mol-1
试回答:
(1)CO的燃烧热ΔH=________ 。
(2)在催化剂作用下,一氧化碳可与过氧化钠反应生成固体碳酸钠,该反应的热化学方程式为_______
(3)工业废气中的CO2可用碱液吸收。所发生的反应如下:
CO2(g)+2NaOH(aq)=Na2CO3(aq)+H2O(l) ΔH=-a kJ·mol-1
CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-b kJ·mol-1
则:①反应CO2(g)+H2O(l)+Na2CO3(aq)=2NaHCO3(aq)的ΔH=_____ kJ·mol-1(用含a、b的代数式表示)。
②标况下,11.2 L CO2与足量的NaOH溶液充分反应后,放出的热量为______ kJ(用含a或b的代数式表示)。
Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) ΔH=-266 kJ·mol-1
试回答:
(1)CO的燃烧热ΔH=
(2)在催化剂作用下,一氧化碳可与过氧化钠反应生成固体碳酸钠,该反应的热化学方程式为
(3)工业废气中的CO2可用碱液吸收。所发生的反应如下:
CO2(g)+2NaOH(aq)=Na2CO3(aq)+H2O(l) ΔH=-a kJ·mol-1
CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-b kJ·mol-1
则:①反应CO2(g)+H2O(l)+Na2CO3(aq)=2NaHCO3(aq)的ΔH=
②标况下,11.2 L CO2与足量的NaOH溶液充分反应后,放出的热量为
您最近一年使用:0次
【推荐3】(1)室温下,2 g 苯(C6H6)完全燃烧生成液态水和CO2,放出83.6 kJ的热量,写出 1 mol C6H6完全燃烧的热化学方程式:______________________ 。
(2)已知:Fe2O3(s)+ C(s)=
C(s)= CO2(g)+2Fe(s) ΔH=+a kJ/mol
CO2(g)+2Fe(s) ΔH=+a kJ/mol
C(s)+O2(g)=CO2(g) ΔH=-b kJ/mol
则2Fe(s)+ O2(g)=Fe2O3(s)的ΔH=
O2(g)=Fe2O3(s)的ΔH=_____ 。
(3)已知下列两个热化学方程式:
H2(g)+ O2(g) =H2O(l) ΔH=-285.8 kJ/mol
O2(g) =H2O(l) ΔH=-285.8 kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2220.0 kJ/mol
①实验测得H2和C3H8的混合气体共 5 mol,完全燃烧生成液态水时放热6264.5 kJ,则混合气体中H2和C3H8的体积之比为____________ 。
②已知:H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
求1mol丙烷燃烧生成CO2和气态水的ΔH=______ 。
(4)已知2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) ΔH=-1225 kJ/mol
则使 1 mol N2O4(l)完全分解成相应的原子时需要吸收的能量是________ 。
(2)已知:Fe2O3(s)+
 C(s)=
C(s)= CO2(g)+2Fe(s) ΔH=+a kJ/mol
CO2(g)+2Fe(s) ΔH=+a kJ/molC(s)+O2(g)=CO2(g) ΔH=-b kJ/mol
则2Fe(s)+
 O2(g)=Fe2O3(s)的ΔH=
O2(g)=Fe2O3(s)的ΔH=(3)已知下列两个热化学方程式:
H2(g)+
 O2(g) =H2O(l) ΔH=-285.8 kJ/mol
O2(g) =H2O(l) ΔH=-285.8 kJ/molC3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2220.0 kJ/mol
①实验测得H2和C3H8的混合气体共 5 mol,完全燃烧生成液态水时放热6264.5 kJ,则混合气体中H2和C3H8的体积之比为
②已知:H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
求1mol丙烷燃烧生成CO2和气态水的ΔH=
(4)已知2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) ΔH=-1225 kJ/mol
| 化学键 | N—H | N—N | N≡N | O—H |
| 键能 (kJ/mol) | 390 | 190 | 946 | 460 |
则使 1 mol N2O4(l)完全分解成相应的原子时需要吸收的能量是
您最近一年使用:0次



