填空
(1)1.7gNH3与标况下_________ LH2S中的氢原子数相同
(2)在标准状况(( ) ℃ 、_____________ KPa)下,CO和CO2的混合气体共4.48L,质量为7.2g。则两种气体的物质的量之和为____________ mol,该混合气体的平均相对分子质量为___________ ,其中CO2为___________ g.
(1)1.7gNH3与标况下
(2)在标准状况(
更新时间:2020-04-27 22:13:46
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】某状况下,2g二氧化碳气体的体积是 1120 mL,2g A 气体的体积是 770 mL,A的摩尔质量是__________ 。 某金属氯化物 MCl240.5 g含 0.6 mol Cl-,则该氯化物的摩尔质量为__________ ,金属M的相对原子质量为__________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在50℃和1.01×105Pa时,相同质量的SO2和SO3的体积比是________ ,密度比是___________
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】用100 g 9.8% H2SO4溶液和足量金属Zn反应,可以得到标准状况下气体_______ 升?(要求有简要步骤)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)在标准状况下,5.6L A气体的质量是15g,则A的摩尔质量为___ 。
(2)一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为:XY2(液)+ 3O2(气)= XO2(气)+2YO2(气),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是______ 。
②化合物XY2的摩尔质量是____ 。
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是_____ 和_____ 。(写元素符号)
(2)一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为:XY2(液)+ 3O2(气)= XO2(气)+2YO2(气),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是
②化合物XY2的摩尔质量是
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】电解26.8%的食盐水1500克,若只有87.3%的食盐发生了反应,求:(请写出相关反应的化学方程式及计算过程,按步骤得分)
(1)在标准状况下可制得氢气多少升?______
(2)这些氢气和氯气全部化合成氯化氢,溶于水制成31%的盐酸,其质量为多少克?(结果保留小数点后一位)______
(1)在标准状况下可制得氢气多少升?
(2)这些氢气和氯气全部化合成氯化氢,溶于水制成31%的盐酸,其质量为多少克?(结果保留小数点后一位)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题
(1)9 g H2O中含有_______ 个H原子。
(2)6.02×1023个OH-的质量为_______ g,含有电子的物质的量为_______ mol。
(3)18.6 g Na2R含0.6 mol Na+,则Na2R的摩尔质量为_______ g·mol-1
(4)0.5molCH4的质量是_______ g,在标准状况下的体积为_______ L。
(1)9 g H2O中含有
(2)6.02×1023个OH-的质量为
(3)18.6 g Na2R含0.6 mol Na+,则Na2R的摩尔质量为
(4)0.5molCH4的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】硫化钠由无水硫酸钠与炭粉在高温下反应制得的,反应的化学方程式为:
①Na2SO4+4C═Na2S+4CO↑;②Na2SO4+4CO═Na2S+4CO2↑.
(1)要制取Na2S 15.6g,需原料芒硝(Na2SO4•10H2O)__ g.
(2)已知在标准状况下,28gCO和44gCO2的体积相等都为22.4L.若在反应过程中,产生CO和CO2的混合气体在标准状况下的体积为44.8L,生成Na2S的质量为m,请通过计算确定m的取值范围__ .
①Na2SO4+4C═Na2S+4CO↑;②Na2SO4+4CO═Na2S+4CO2↑.
(1)要制取Na2S 15.6g,需原料芒硝(Na2SO4•10H2O)
(2)已知在标准状况下,28gCO和44gCO2的体积相等都为22.4L.若在反应过程中,产生CO和CO2的混合气体在标准状况下的体积为44.8L,生成Na2S的质量为m,请通过计算确定m的取值范围
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】填空。
(1)标准状况下11.2LH2S气体的质量为_______ ;
(2)已知3.01×1023个X气体分子的质量为8g,则X气体的摩尔质量是_______ ;
(3)与0.1molOH-含有相同电子数的NH3在标状况下的体积为_______ ;
(4)同质量的NH3和H2S中氢原子的个数比为_______ 。
(1)标准状况下11.2LH2S气体的质量为
(2)已知3.01×1023个X气体分子的质量为8g,则X气体的摩尔质量是
(3)与0.1molOH-含有相同电子数的NH3在标状况下的体积为
(4)同质量的NH3和H2S中氢原子的个数比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)0.5molSO2,含有的分子数为_______ 个,质量为_______ g,标准状况下体积为_______ L。
(2)标准状况下,14g N2所占有的体积为_______ L,所含氮原子个数为_______ 个。
(3)标准状况下,2mol NH3与_______ g CO2的体积相等。
(4)中和含0.2mol HCl的稀盐酸,需NaOH物质的量为_______ mol,如改用KOH,则所需KOH的质量为_______ g。
(5)已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的摩尔质量为_______ 。
(6)在22.2g某二价金属的氯化物(RCl2)中含Cl- 离子0.4mol,则RCl2的摩尔质量为_______ ,R的相对原子质量为_______ 。
(1)0.5molSO2,含有的分子数为
(2)标准状况下,14g N2所占有的体积为
(3)标准状况下,2mol NH3与
(4)中和含0.2mol HCl的稀盐酸,需NaOH物质的量为
(5)已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的摩尔质量为
(6)在22.2g某二价金属的氯化物(RCl2)中含Cl- 离子0.4mol,则RCl2的摩尔质量为
您最近一年使用:0次

 CaCl2(s)+2NH3↑+ 2H2O,现将107g NH4Cl晶体和111g熟石灰混合后,充分加热使之完全反应。求:
CaCl2(s)+2NH3↑+ 2H2O,现将107g NH4Cl晶体和111g熟石灰混合后,充分加热使之完全反应。求: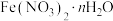 可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有
可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有 、
、 、
、 、
、 ,其中水的质量为6.300g,残留的固体产物是
,其中水的质量为6.300g,残留的固体产物是 ,质量为4.800g。
,质量为4.800g。 和
和 组成,测得混合气体在标准状况下的密度为
组成,测得混合气体在标准状况下的密度为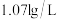 ,则混合气体中
,则混合气体中

