人们运用元素周期律和元素周期表,可以系统研究元素的性质。试回答:
(1)碱金属元素中,锂原子的结构示意图为__ 、其中6Li、7Li互为__ ,用电子式表示Li2O的形成过程___ 。
(2)金属钾19K位于元素周期表中的第__ 周期、第__ 族;钾的氧化物有多种,其中过氧化钾(K2O2)和超氧化钾(KO2)常作供氧剂,写出过氧化钾与CO2反应的化学方程式:___ ;超氧化钾与水反应如下,请配平该反应的化学方程式:
_ KO2+_ H2O=_ KOH+_ O2↑+_ H2O2
(3)第三周期元素中,酸性最强的HClO4中氯元素的化合价为__ 、可作半导体材料的元素是__ (填名称),当反应H2+Cl2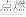 2HCl发生过程中,涉及到
2HCl发生过程中,涉及到___ 键断裂和__ 键的形成。(填:离子键或极性键或非极性键)
(1)碱金属元素中,锂原子的结构示意图为
(2)金属钾19K位于元素周期表中的第
(3)第三周期元素中,酸性最强的HClO4中氯元素的化合价为
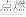 2HCl发生过程中,涉及到
2HCl发生过程中,涉及到
更新时间:2020-04-28 07:08:39
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】请回答:
(1)HCl的电子式是_____ 。
(2)S2-的离子结构示意图_____ 。
(3)P最高价氧化物对应的水化物______ (用化学式表示)。
(4)足量SO2通入品红溶液,可观察到的现象是_____ 。
(5)实验室制备氯气的离子方程式是_____ 。
(6)写出过氧化钠与水反应的化学方程式,并用双线桥标出电子移动方向_____ 。
(1)HCl的电子式是
(2)S2-的离子结构示意图
(3)P最高价氧化物对应的水化物
(4)足量SO2通入品红溶液,可观察到的现象是
(5)实验室制备氯气的离子方程式是
(6)写出过氧化钠与水反应的化学方程式,并用双线桥标出电子移动方向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】含氯物质在生产生活中有重要作用。
(1)与氯元素同族的短周期元素的原子结构示意图为_______ 。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是_______(填序号)。
(3)实验室用强氧化剂 制取
制取 的化学方程式
的化学方程式_______ 。
(4)实验室制取干燥 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为_______ 。

(5)用NaClO溶液也可以吸收工业尾气中的NO。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。

a.在酸性NaClO溶液中,HClO氧化NO生成 和
和 ,其离子方程式为
,其离子方程式为_______ 。
b.NaClO溶液的初始pH越小,NO转化率越高,其原因是_______ 。
(6)某温度下,将 通入NaOH溶液中,反应生成NaCl、NaClO、
通入NaOH溶液中,反应生成NaCl、NaClO、 的混合液,若溶液中
的混合液,若溶液中 、
、 、
、 的物质的量分别为a、b、c,则a、b、c之间的关系为
的物质的量分别为a、b、c,则a、b、c之间的关系为_______ 。
(1)与氯元素同族的短周期元素的原子结构示意图为
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是_______(填序号)。
A. 、 、 、 、 的熔点 的熔点 | B. 、 、 、 、 的氧化性 的氧化性 |
| C.HCI、HBr、HI的热稳定性 | D.HCl、HBr、HI的酸性 |
 制取
制取 的化学方程式
的化学方程式(4)实验室制取干燥
 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为
(5)用NaClO溶液也可以吸收工业尾气中的NO。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
a.在酸性NaClO溶液中,HClO氧化NO生成
 和
和 ,其离子方程式为
,其离子方程式为b.NaClO溶液的初始pH越小,NO转化率越高,其原因是
(6)某温度下,将
 通入NaOH溶液中,反应生成NaCl、NaClO、
通入NaOH溶液中,反应生成NaCl、NaClO、 的混合液,若溶液中
的混合液,若溶液中 、
、 、
、 的物质的量分别为a、b、c,则a、b、c之间的关系为
的物质的量分别为a、b、c,则a、b、c之间的关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出氮元素的原子结构示意图:_______ 。
(2)通常情况下,氮气性质不活泼,其原因是__________。
(3)N2的电子式:_______ ,将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是_______ 。
A.N2和H2在一定条件下反应生成NH3 B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO D.NH3和HNO3反应生成NH4NO3
(4)氨气的电子式:_______ 。
(5)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出此反应的化学方程式_____ 。
(1)写出氮元素的原子结构示意图:
(2)通常情况下,氮气性质不活泼,其原因是__________。
| A.氮分子是双原子分子 | B.氮元素的非金属性很强 |
| C.氮原子的半径较小 | D.破坏氮分子中的化学键很难 |
A.N2和H2在一定条件下反应生成NH3 B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO D.NH3和HNO3反应生成NH4NO3
(4)氨气的电子式:
(5)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出此反应的化学方程式
您最近一年使用:0次
【推荐1】以TiO2为催化剂用NaClO将CN-离子氧化成CNO-,CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200 mL(设其中CN-的浓度为0.2 mol•L-1)进行实验。
①写出CNO-在酸性条件下被NaClO氧化的离子方程式:________ ;
②若结果测得CO2的质量为1.408 g,则该实验中测得CN-被处理的百分率为______ 。
①写出CNO-在酸性条件下被NaClO氧化的离子方程式:
②若结果测得CO2的质量为1.408 g,则该实验中测得CN-被处理的百分率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】卤素互化物、拟卤素与卤素单质的结构,性质相似。常见的卤素互化物有ICl、IBr等,拟卤素有(CN)2、(SCN)2等。
(1)卤族元素位于元素周期表的_______ 。
(2)79Br和81Br这两种核素的中子数之差的绝对值为_______ 。
(3)①Cl2;②ICl;③IBr三种物质熔点由高到低的顺序为_______ 。
(4)①已知CN-与N2结构相似,CN-的电子式为______ 。
②推算HCN分子中σ键与π键数目之比为_______ 。
③关于氨基氰(N≡C-NH2)分子的说法中正确的是_______ 。
A.C原子采用sp3杂化
B.N原子的杂化形式有sp与sp3杂化
C.C≡N键的键长大于C-N键
D.所有原子满足8电子稳定结构
开采的金矿可用氰化法提取,步骤如下:
i.将金矿砂溶于pH为10.5~11的KCN溶液,并鼓入空气,过滤除去矿渣,得含K[Au(CN)2]的滤液;
ii.向滤液中加入足量金属锌,得单质金。Zn+2K[Au(CN)2]=2Au+K2[Zn(CN)4]
(5)K[Au(CN)2]中Au+的配体为______ 。
(6)K2[Zn(CN)4]中Au+的配位数为______ 。
(7)i中反应的离子方程式为:_______ 。
 Au+
Au+ CN-+
CN-+ _______+
_______+ _______=
_______= [Au(CN)2]-+
[Au(CN)2]-+ _______
_______
(8)已知Ka(HCN)=4.0×10-10。i中,pH<10.5会导致相同时间内Au的浸取率下降,原因_______ 。
(1)卤族元素位于元素周期表的
| A.s区 | B.p区 | C.d区 | D.f区 |
(3)①Cl2;②ICl;③IBr三种物质熔点由高到低的顺序为
| A.①>②>③ | B.③>②>① | C.②>①>③ | D.③>①>② |
②推算HCN分子中σ键与π键数目之比为
③关于氨基氰(N≡C-NH2)分子的说法中正确的是
A.C原子采用sp3杂化
B.N原子的杂化形式有sp与sp3杂化
C.C≡N键的键长大于C-N键
D.所有原子满足8电子稳定结构
开采的金矿可用氰化法提取,步骤如下:
i.将金矿砂溶于pH为10.5~11的KCN溶液,并鼓入空气,过滤除去矿渣,得含K[Au(CN)2]的滤液;
ii.向滤液中加入足量金属锌,得单质金。Zn+2K[Au(CN)2]=2Au+K2[Zn(CN)4]
(5)K[Au(CN)2]中Au+的配体为
(6)K2[Zn(CN)4]中Au+的配位数为
(7)i中反应的离子方程式为:
 Au+
Au+ CN-+
CN-+ _______+
_______+ _______=
_______= [Au(CN)2]-+
[Au(CN)2]-+ _______
_______(8)已知Ka(HCN)=4.0×10-10。i中,pH<10.5会导致相同时间内Au的浸取率下降,原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】高铁酸钾( )具有极强的氧化性,是一种优良的水处理剂。
)具有极强的氧化性,是一种优良的水处理剂。
(1)请完成 与水反应的方程式:
与水反应的方程式:
_______ 。 在处理水的过程中所起的作用是
在处理水的过程中所起的作用是_______ 和_______ 。
(2)常温下, 的
的 ,请写出
,请写出 在水中的溶解平衡方程式
在水中的溶解平衡方程式_____ 。
(3)将适量 配制成
配制成 的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定
的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定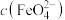 的变化,结果见图I。第(1)题中的反应为
的变化,结果见图I。第(1)题中的反应为 变化的主反应,则温度对该反应的反应速率和平衡移动的影响是
变化的主反应,则温度对该反应的反应速率和平衡移动的影响是_______ ;发生反应的
_______ 0(填“>”、“<”或“=”)。

(4) 在水溶液中的存在形态如图II所示。下列说法正确的是
在水溶液中的存在形态如图II所示。下列说法正确的是_______ (填字母)。
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向 的这种溶液中加KOH溶液至
的这种溶液中加KOH溶液至 ,
,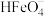 的分布分数先增大后减小
的分布分数先增大后减小
C.向 的这种溶液中加KOH溶液,发生反应的离子方程式为:
的这种溶液中加KOH溶液,发生反应的离子方程式为:
 )具有极强的氧化性,是一种优良的水处理剂。
)具有极强的氧化性,是一种优良的水处理剂。(1)请完成
 与水反应的方程式:
与水反应的方程式:
 在处理水的过程中所起的作用是
在处理水的过程中所起的作用是(2)常温下,
 的
的 ,请写出
,请写出 在水中的溶解平衡方程式
在水中的溶解平衡方程式(3)将适量
 配制成
配制成 的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定
的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定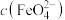 的变化,结果见图I。第(1)题中的反应为
的变化,结果见图I。第(1)题中的反应为 变化的主反应,则温度对该反应的反应速率和平衡移动的影响是
变化的主反应,则温度对该反应的反应速率和平衡移动的影响是

(4)
 在水溶液中的存在形态如图II所示。下列说法正确的是
在水溶液中的存在形态如图II所示。下列说法正确的是A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向
 的这种溶液中加KOH溶液至
的这种溶液中加KOH溶液至 ,
,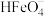 的分布分数先增大后减小
的分布分数先增大后减小C.向
 的这种溶液中加KOH溶液,发生反应的离子方程式为:
的这种溶液中加KOH溶液,发生反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)下列5种物质NeCaBr2H2O2④Na2O2⑤I2中,只含有离子键的是(填序号,下同)________ ;含有共价键的离子化合物是_______ ;含有共价键的共价化合物是_________ ;不存在化学键的是________ 。
(2)在下列变化中干冰的升华Na2O2溶于水氯化钾的溶解④HCl溶于水⑤O2溶于水⑥烧碱的熔化,未破坏化学键的是________ ;仅破坏离子键的是________ ;仅破坏共价键的是________ 。
(2)在下列变化中干冰的升华Na2O2溶于水氯化钾的溶解④HCl溶于水⑤O2溶于水⑥烧碱的熔化,未破坏化学键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.氢化钠(NaH) 是一种离子化合物,遇水后放出氢气并生成一种碱,主要应用在有机合成和储氢材料方面。根据信息完成下列各空:
(1)氢化钠的电子式为_____________________________ 。
(2)氢化钠与水反应的化学方程式为_____________________ ,反应的氧化剂为___________ 。该反应过程中,被破坏的化学键有_____________ (填序号,下同),形成的化学键有______________ 。
①离子键 ②极性共价键 ③非极性共价键
II.现有短周期元素X 形成的单质A与NaOH溶液反应,有如下转化关系:, (若产物中有水生成则省略未表示出来)。
(若产物中有水生成则省略未表示出来)。
(1)常温常压下,若A 为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为________________________________________________ ;
(2)若A 为金属单质,C 为气体,则A 与NaOH 溶液反应的离子方程式为_____________________________ ;A 最高价氧化物的水化物与NaOH 溶液反应的离子方程式为______________________________ 。
(1)氢化钠的电子式为
(2)氢化钠与水反应的化学方程式为
①离子键 ②极性共价键 ③非极性共价键
II.现有短周期元素X 形成的单质A与NaOH溶液反应,有如下转化关系:,
 (若产物中有水生成则省略未表示出来)。
(若产物中有水生成则省略未表示出来)。(1)常温常压下,若A 为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为
(2)若A 为金属单质,C 为气体,则A 与NaOH 溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学键
(1)化学键
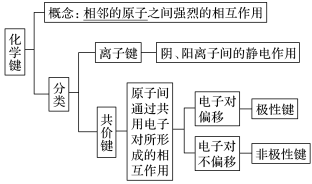
(2)离子键和共价键的比较
(3)化学反应的本质:一个化学反应过程,本质上就是____ 的断裂和____ 的形成过程。
(1)化学键

(2)离子键和共价键的比较
| 离子键 | 共价键 | ||
| 非极性键 | 极性键 | ||
| 概念 | 带相反电荷离子之间的相互作用 | 原子间通过共用电子对(电子云重叠)而形成的化学键 | |
| 成键粒子 | 阴、阳离子 | 原子 | |
| 成键实质 | 阴、阳离子的静电作用 | 共用电子对不偏向任何一方 | 共用电子对偏向一方原子 |
| 形成条件 | 活泼金属元素与活泼非金属元素经电子得失形成离子键 | 同种元素原子之间成键 | 不同种元素原子之间成键 |
| 形成的物质 | 离子化合物 | 非金属单质;某些共价化合物或离子化合物 | 共价化合物或离子化合物 |
(3)化学反应的本质:一个化学反应过程,本质上就是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下列物质中:N2、H2O、Na2O、KOH、NaF、Na2SO4
(1)只含有共价键的物质是__ ;
(2)只含有离子键的物质是__ ;
(3)既含有离子键,又含有共价键的物质__ 。
(1)只含有共价键的物质是
(2)只含有离子键的物质是
(3)既含有离子键,又含有共价键的物质
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列纯净物:
①Ne、②NH4Cl、③NaOH、④HCl、⑤MgCl2 。
(1)只含离子键的是_______ (填序号,下同)。
(2)只含共价键的是_______ 。
(3)不含化学键的是_______ 。
(4)只由非金属元素组成的离子化合物是_______ 。
①Ne、②NH4Cl、③NaOH、④HCl、⑤MgCl2 。
(1)只含离子键的是
(2)只含共价键的是
(3)不含化学键的是
(4)只由非金属元素组成的离子化合物是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下面是同学们熟悉的物质:
①O2 ②干冰 ③NaBr ④H2SO4 ⑤Na2CO3 ⑥NH4Cl ⑦NaHSO4 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,只含有共价键的是______ ;只含有离子键的是 ______ ;既含有共价键又含有离子键的是 ______ ;不存在化学键的是 ______ ;电解质有____________ ;
非电解质有___________ ( 填编号)
(2)将NaHSO4溶于水,破坏NaHSO4中的化学键是_____________ ,写出其电离方程式________ ;NaHSO4在熔融状态下电离,破坏的化学键是_____________ ,写出其电离方程式____________ .
(3)写出②与⑨发生反应的化学方程式:____________ .
(4)写出在稀溶液中⑥和⑩反应的离子方程式:____________ .
①O2 ②干冰 ③NaBr ④H2SO4 ⑤Na2CO3 ⑥NH4Cl ⑦NaHSO4 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,只含有共价键的是
非电解质有
(2)将NaHSO4溶于水,破坏NaHSO4中的化学键是
(3)写出②与⑨发生反应的化学方程式:
(4)写出在稀溶液中⑥和⑩反应的离子方程式:
您最近一年使用:0次



