铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)向沸水中逐滴滴加1mol·L-1FeCl3溶液至液体呈透明的红褐色,所得分散系中微粒直径的范围是______________ ,区别该液体和FeCl3溶液的方法是______________ 。
(2)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 Fe3O4+6SO2,氧化产物为
Fe3O4+6SO2,氧化产物为________ ,若有3mol FeS2参加反应,转移________ mol电子。
(3)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请配平该化学方程式:
___ FeSO4+____ KNO3+___ H2SO4═____ K2SO4+_____ Fe2(SO4)3+__ NO↑+_____ H2O。
(4)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160mL 5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L(标准状况)H2,经检测,溶液中无Fe3+,则参加反应的铁粉的质量为________ g。
(1)向沸水中逐滴滴加1mol·L-1FeCl3溶液至液体呈透明的红褐色,所得分散系中微粒直径的范围是
(2)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2
 Fe3O4+6SO2,氧化产物为
Fe3O4+6SO2,氧化产物为(3)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请配平该化学方程式:
(4)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160mL 5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L(标准状况)H2,经检测,溶液中无Fe3+,则参加反应的铁粉的质量为
更新时间:2020-04-27 16:41:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Fe2O3又称铁红,请根据要求完成下列问题.
(1)Fe2O3固体(红棕色)属于_____ (填纯净物或者混合物).将其加入适量盐酸,反应的化学方程式_____
(2)用上述所得溶液进行下列实验,取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,反应的离子方程式_____
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向烧杯中加入几滴FeCl3溶液,继续煮沸至出现_____ 色,即可制得Fe(OH)3胶体.
(4)另取一小烧杯也加入20mL蒸馏水,向烧杯中加入1mL FeCl3溶液,振荡摇匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到_____ 烧杯的液体中产生了丁达尔效应.
(1)Fe2O3固体(红棕色)属于
(2)用上述所得溶液进行下列实验,取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,反应的离子方程式
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向烧杯中加入几滴FeCl3溶液,继续煮沸至出现
(4)另取一小烧杯也加入20mL蒸馏水,向烧杯中加入1mL FeCl3溶液,振荡摇匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】FeCl3是中学实验室常用的试剂。
(1)写出氯化铁在水中的电离方程式:______ 。
(2)向FeCl3溶液中加入硫氰化钾(KSCN)溶液,溶液变红色。(已知:硫氰化铁为红色)写出该反应的离子方程式______ 。
(3)可利用氯化铁溶液制备氢氧化铁胶体,下列制备氢氧化铁胶体的操作方法正确的是
(4)为了探究离子反应的本质,设计如下实验:

①写出生成A的离子方程式:______ 。
②上述流程中,加入足量稀硝酸的目的是______ 。如何判定无色溶液B与稀硝酸发生了离子反应?______ 。
(1)写出氯化铁在水中的电离方程式:
(2)向FeCl3溶液中加入硫氰化钾(KSCN)溶液,溶液变红色。(已知:硫氰化铁为红色)写出该反应的离子方程式
(3)可利用氯化铁溶液制备氢氧化铁胶体,下列制备氢氧化铁胶体的操作方法正确的是
| A.向饱和氯化铁溶液中滴加适量的氢氧化钠稀溶液 |
| B.加热煮沸氯化铁饱和溶液 |
| C.在氨水中滴加氯化铁浓溶液 |
| D.在沸水中滴加饱和氯化铁溶液,煮沸至出现红褐色液体 |
(4)为了探究离子反应的本质,设计如下实验:

①写出生成A的离子方程式:
②上述流程中,加入足量稀硝酸的目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有甲、乙、丙三名同学分别进行 胶体的制备实验。
胶体的制备实验。
I.甲同学向饱和氯化铁溶液中加入少量的NaOH溶液;
II.乙同学直接加热饱和 溶液;
溶液;
III.丙同学向25mL沸水中逐滴加入5~6滴 饱和溶液,继续煮沸至液体呈红褐色,停止加热。
饱和溶液,继续煮沸至液体呈红褐色,停止加热。
(1)其中操作正确的同学是_______ ;他的操作中涉及到的化学反应方程式为_______ 。
(2)证明有 胶体生成的现象是
胶体生成的现象是_______ 。
(3)丁同学用所制得的 胶体进行下列实验:不断滴加稀硫酸,观察到的现象是
胶体进行下列实验:不断滴加稀硫酸,观察到的现象是_______ ,涉及的离子反应方程式为_______ 。
 胶体的制备实验。
胶体的制备实验。I.甲同学向饱和氯化铁溶液中加入少量的NaOH溶液;
II.乙同学直接加热饱和
 溶液;
溶液;III.丙同学向25mL沸水中逐滴加入5~6滴
 饱和溶液,继续煮沸至液体呈红褐色,停止加热。
饱和溶液,继续煮沸至液体呈红褐色,停止加热。(1)其中操作正确的同学是
(2)证明有
 胶体生成的现象是
胶体生成的现象是(3)丁同学用所制得的
 胶体进行下列实验:不断滴加稀硫酸,观察到的现象是
胶体进行下列实验:不断滴加稀硫酸,观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氯碱工厂生产的氯气和氢气可以进一步用于生产盐酸,主要过程如下:
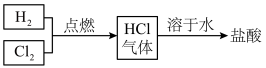
(1)其中关键的一步为氯气和氢气在燃烧管口燃烧生成HCl,氯气有毒,应采取的措施是____ 。合成盐酸厂要求合成气中的HCl的含量要大于97%,试用最简便的方法进行分析是否含量大于97%____ 。
(2)氯碱工厂生产的氯气和氢氧化钠溶液可以用于制取“84消毒液”,反应的化学方程式为__ 。
(3)某同学欲证明盐酸与氯化氢气体性质不同,他分别向A、B、C三支洁净试管中各放入一片干燥的蓝色石蕊试纸,然后往A试管内加入盐酸,试纸显___ 色,往B试管中通入干燥的氯化氢气体,试纸显___ 色.最后向C试管中加入物质___ (填化学式),他之所以加入这种物质的理由是____ 。

(1)其中关键的一步为氯气和氢气在燃烧管口燃烧生成HCl,氯气有毒,应采取的措施是
(2)氯碱工厂生产的氯气和氢氧化钠溶液可以用于制取“84消毒液”,反应的化学方程式为
(3)某同学欲证明盐酸与氯化氢气体性质不同,他分别向A、B、C三支洁净试管中各放入一片干燥的蓝色石蕊试纸,然后往A试管内加入盐酸,试纸显
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)配平下列化学反应方程式
Cu2S + HNO3—— Cu(NO3)2+ H2SO4+ NO + H2O________ ;
(2)标出电子转移的方向和数目________ ;
(3)在标准状况下生成2.24LNO时,转移电子物质的量为___________ 。
Cu2S + HNO3—— Cu(NO3)2+ H2SO4+ NO + H2O
(2)标出电子转移的方向和数目
(3)在标准状况下生成2.24LNO时,转移电子物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
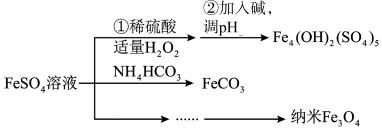
【推荐3】硫酸亚铁是重要的化工原料,以硫酸亚铁为原料可以获得下列物质:
(1)保存硫酸亚铁溶液时,为防止 溶液氧化变质,常在硫酸亚铁溶液加入少量
溶液氧化变质,常在硫酸亚铁溶液加入少量_______ 。
(2)制备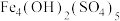 的两个步骤中,第①步反应的离子方程式为
的两个步骤中,第①步反应的离子方程式为_______ 。
(3)制备 ;向
;向 溶液中加入过量的
溶液中加入过量的 溶液,生成
溶液,生成 沉淀同时有气体放出,此气体可使澄清石灰水变浑浊。该反应的离子方程式为
沉淀同时有气体放出,此气体可使澄清石灰水变浑浊。该反应的离子方程式为_______ 。
(4)检验 中不同价态的铁元素,选用的试剂是
中不同价态的铁元素,选用的试剂是_______ (填字母代号)。
a.稀硝酸 b.稀硫酸 c.硫氰化钾溶液 d.高锰酸钾溶液 e.氢氧化钠溶液
(5)已知在酸性环境中几种离子之间会发生如下转化:
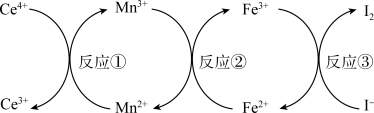
则按离子的还原性从弱到强排列,顺序应该是_______ 。
(1)保存硫酸亚铁溶液时,为防止
 溶液氧化变质,常在硫酸亚铁溶液加入少量
溶液氧化变质,常在硫酸亚铁溶液加入少量(2)制备
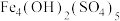 的两个步骤中,第①步反应的离子方程式为
的两个步骤中,第①步反应的离子方程式为(3)制备
 ;向
;向 溶液中加入过量的
溶液中加入过量的 溶液,生成
溶液,生成 沉淀同时有气体放出,此气体可使澄清石灰水变浑浊。该反应的离子方程式为
沉淀同时有气体放出,此气体可使澄清石灰水变浑浊。该反应的离子方程式为(4)检验
 中不同价态的铁元素,选用的试剂是
中不同价态的铁元素,选用的试剂是a.稀硝酸 b.稀硫酸 c.硫氰化钾溶液 d.高锰酸钾溶液 e.氢氧化钠溶液
(5)已知在酸性环境中几种离子之间会发生如下转化:

则按离子的还原性从弱到强排列,顺序应该是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】金属的性质
金属材料在人类社会发展中起到了举足轻重的作用,因为它具有比其他材料更优越的综合性能,能够更适应科技和生活方面提出的各种不同的要求。
(1)向滴有酚酞溶液的水中加入一块绿豆大的钠,下列实验现象描述错误的是___________
(2)我国自主研发的大飞机C919大量使用了铝锂合金。这是利用了铝锂合金的下列性质___________
(3)常温下,将铁片放到浓硫酸中,一段时间后___________
(4)下列关于碳酸钠和碳酸氢钠的叙述正确的是___________
(5)实验室测定氧化物X(FexOy)的组成实验如下:
金属材料在人类社会发展中起到了举足轻重的作用,因为它具有比其他材料更优越的综合性能,能够更适应科技和生活方面提出的各种不同的要求。
(1)向滴有酚酞溶液的水中加入一块绿豆大的钠,下列实验现象描述错误的是___________
| A.钠沉入水底 | B.钠熔成小球 |
| C.发出“嘶嘶”声音 | D.溶液变红 |
| A.低强度 | B.低密度 | C.导热性 | D.熔点低 |
| A.溶液呈棕黄色 | B.铁片质量减轻 |
| C.有大量气泡产生 | D.铁片表面生成致密氧化膜 |
| A.相同条件下,在水中的溶解性:碳酸钠<碳酸氢钠 |
| B.相同条件下,热稳定性:碳酸钠>碳酸氢钠 |
| C.相同条件下,与酸反应的速率:碳酸钠>碳酸氢钠 |
| D.一定条件下,碳酸钠不能转化为碳酸氢钠,而碳酸氢钠可以转化为碳酸钠 |

A.样品X中含有+2价铁元素 |
B.溶液 中 中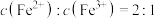 |
C.溶液 中的离子只有 中的离子只有 和 和 |
D.根据步骤I、II可判断 为 为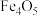 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)①在现代半导体工业生产中,常利 腐蚀铜的原理制作印刷线路板,该原理的离子方程式为
腐蚀铜的原理制作印刷线路板,该原理的离子方程式为_______ 。
②氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是_______ 。
A.有铁无铜 B.有铜无铁 C.有铁有铜 D.无铁无铜
(2)某同学在 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入
煤油,再于液面下依次加入 滴
滴 溶液和几滴氯水,溶液变红,煤油的作用是
溶液和几滴氯水,溶液变红,煤油的作用是_______ 。
(3)某同学取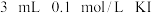 溶液,加入
溶液,加入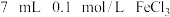 溶液混合。分别取此溶液于
溶液混合。分别取此溶液于 支试管中进行如下实验:
支试管中进行如下实验:
①第一支试管中加入 滴淀粉溶液,溶液显蓝色;
滴淀粉溶液,溶液显蓝色;
②第二支试管中加入 滴
滴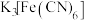 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;
③第三支试管中加入 滴
滴_______ 溶液,溶液变红。
实验②检验的离子可能是_______  填离子符号
填离子符号 ;写出
;写出 与
与 反应的离子方程式
反应的离子方程式_______ 。上述 和
和 溶充分反应后,溶液中
溶充分反应后,溶液中 浓度为
浓度为_______ 。
(4)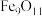 中铁元素形式为
中铁元素形式为 和
和 ,则
,则 和
和 离子质量之比为
离子质量之比为_______ 。
(1)①在现代半导体工业生产中,常利
 腐蚀铜的原理制作印刷线路板,该原理的离子方程式为
腐蚀铜的原理制作印刷线路板,该原理的离子方程式为②氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是
A.有铁无铜 B.有铜无铁 C.有铁有铜 D.无铁无铜
(2)某同学在
 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入
煤油,再于液面下依次加入 滴
滴 溶液和几滴氯水,溶液变红,煤油的作用是
溶液和几滴氯水,溶液变红,煤油的作用是(3)某同学取
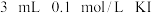 溶液,加入
溶液,加入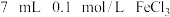 溶液混合。分别取此溶液于
溶液混合。分别取此溶液于 支试管中进行如下实验:
支试管中进行如下实验:①第一支试管中加入
 滴淀粉溶液,溶液显蓝色;
滴淀粉溶液,溶液显蓝色;②第二支试管中加入
 滴
滴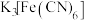 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;③第三支试管中加入
 滴
滴实验②检验的离子可能是
 填离子符号
填离子符号 ;写出
;写出 与
与 反应的离子方程式
反应的离子方程式 和
和 溶充分反应后,溶液中
溶充分反应后,溶液中 浓度为
浓度为(4)
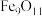 中铁元素形式为
中铁元素形式为 和
和 ,则
,则 和
和 离子质量之比为
离子质量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】合成氨工业生产中所用的α—Fe催化剂的主要成分是FeO、 。回答下列问题:
。回答下列问题:
(1) 的摩尔质量为
的摩尔质量为_______ 。
(2)室温下,将适量的FeO粉末投入足量的稀盐酸中:
①取少量上述反应后的溶液于试管中,静置一段时间后,可观察到溶液的颜色由绿色变为黄色,溶液由绿色变为黄色的原因为_______ (用离子方程式表示)。
②往①的试管的溶液中加入足量的氢氧化钠溶液,此时观察到溶液中的现象为_______ 。
③_______ (填“能”或“不能”)选用酸性高锰酸钾溶液检验①的试管中 的存在。
的存在。
(3)在FeO、 的混合物中:
的混合物中:
①若铁原子、氧原子的物质的量之比为7:8,则FeO与 的物质的量之比为
的物质的量之比为_______ 。
②当该混合物中+2价铁与+3价铁的物质的量之比为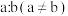 时,该混合物中铁元素的质量分数为
时,该混合物中铁元素的质量分数为_______ (用含a、b的代数式表示)。
 。回答下列问题:
。回答下列问题:(1)
 的摩尔质量为
的摩尔质量为(2)室温下,将适量的FeO粉末投入足量的稀盐酸中:
①取少量上述反应后的溶液于试管中,静置一段时间后,可观察到溶液的颜色由绿色变为黄色,溶液由绿色变为黄色的原因为
②往①的试管的溶液中加入足量的氢氧化钠溶液,此时观察到溶液中的现象为
③
 的存在。
的存在。(3)在FeO、
 的混合物中:
的混合物中:①若铁原子、氧原子的物质的量之比为7:8,则FeO与
 的物质的量之比为
的物质的量之比为②当该混合物中+2价铁与+3价铁的物质的量之比为
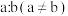 时,该混合物中铁元素的质量分数为
时,该混合物中铁元素的质量分数为
您最近一年使用:0次



