金属的性质
金属材料在人类社会发展中起到了举足轻重的作用,因为它具有比其他材料更优越的综合性能,能够更适应科技和生活方面提出的各种不同的要求。
(1)向滴有酚酞溶液的水中加入一块绿豆大的钠,下列实验现象描述错误的是___________
(2)我国自主研发的大飞机C919大量使用了铝锂合金。这是利用了铝锂合金的下列性质___________
(3)常温下,将铁片放到浓硫酸中,一段时间后___________
(4)下列关于碳酸钠和碳酸氢钠的叙述正确的是___________
(5)实验室测定氧化物X(FexOy)的组成实验如下:

下列有关说法正确的是___________
金属材料在人类社会发展中起到了举足轻重的作用,因为它具有比其他材料更优越的综合性能,能够更适应科技和生活方面提出的各种不同的要求。
(1)向滴有酚酞溶液的水中加入一块绿豆大的钠,下列实验现象描述错误的是___________
| A.钠沉入水底 | B.钠熔成小球 |
| C.发出“嘶嘶”声音 | D.溶液变红 |
| A.低强度 | B.低密度 | C.导热性 | D.熔点低 |
| A.溶液呈棕黄色 | B.铁片质量减轻 |
| C.有大量气泡产生 | D.铁片表面生成致密氧化膜 |
| A.相同条件下,在水中的溶解性:碳酸钠<碳酸氢钠 |
| B.相同条件下,热稳定性:碳酸钠>碳酸氢钠 |
| C.相同条件下,与酸反应的速率:碳酸钠>碳酸氢钠 |
| D.一定条件下,碳酸钠不能转化为碳酸氢钠,而碳酸氢钠可以转化为碳酸钠 |

下列有关说法正确的是___________
A.样品X中含有+2价铁元素 |
B.溶液 中 中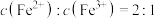 |
C.溶液 中的离子只有 中的离子只有 和 和 |
D.根据步骤I、II可判断 为 为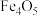 |
更新时间:2023-07-21 08:37:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】常温下足量金属锌与浓硫酸反应开始阶段生成硫酸锌、二氧化硫和水,反应进行到某个程度以后会发生另一个反应,请回答相关问题。
(1)请按反应的先后顺序写出前者的化学方程式和后者的离子方程式_____________________ 。
(2)整个过程中被还原的元素有_________ 。(填序号)
(3)第一阶段反应中电子转移的情况 是_________ 
_________ 。(填元素符号)
(4)若两个阶段反应的还原产物物质的量为1:1,则两个阶段转移电子数之比为________ 。
(5)检验最终所得溶液中主要阴离子的方法是________________ 。
(1)请按反应的先后顺序写出前者的化学方程式和后者的离子方程式
(2)整个过程中被还原的元素有
(3)第一阶段反应中电子转移的情况 是

(4)若两个阶段反应的还原产物物质的量为1:1,则两个阶段转移电子数之比为
(5)检验最终所得溶液中主要阴离子的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Zn和浓硫酸反应:Zn+2H+=H2↑+Zn2+。( )
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
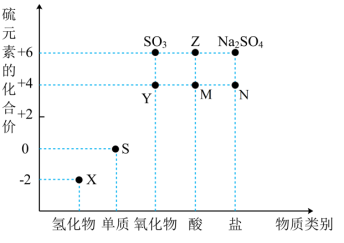
【推荐3】利用元素的化合价推测物质的性质是化学研究的重要手段。硫及其化合物的“价—类”二维图如下:___________ (填化学式)。
(2)将X与Y混合可生成淡黄色固体,该反应中还原剂与氧化剂的物质的量之比为___________ ;实验室常用热的氢氧化钠溶液洗去试管内壁附着的该淡黄色固体,其原理为___________ (用化学方程式表示)。
(3)检验N盐溶液是否变质的方法是___________ 。
(4)Z的浓溶液与碳单质在一定条件下可以发生化学反应,该反应的化学方程式为___________ 。
(5)已知 能被
能被 氧化为Na2SO4,则240mL0.05mol/L的Na2SO3溶液与200mL0.02mol/L的
氧化为Na2SO4,则240mL0.05mol/L的Na2SO3溶液与200mL0.02mol/L的 溶液恰好完全反应时,Cr元素在还原产物中的化合价为
溶液恰好完全反应时,Cr元素在还原产物中的化合价为___________ 。
(2)将X与Y混合可生成淡黄色固体,该反应中还原剂与氧化剂的物质的量之比为
(3)检验N盐溶液是否变质的方法是
(4)Z的浓溶液与碳单质在一定条件下可以发生化学反应,该反应的化学方程式为
(5)已知
 能被
能被 氧化为Na2SO4,则240mL0.05mol/L的Na2SO3溶液与200mL0.02mol/L的
氧化为Na2SO4,则240mL0.05mol/L的Na2SO3溶液与200mL0.02mol/L的 溶液恰好完全反应时,Cr元素在还原产物中的化合价为
溶液恰好完全反应时,Cr元素在还原产物中的化合价为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】钠元素在自然界都以化合物的形式存在。
(1)过氧化钠用于呼吸面具的反应方程式为___________ ,假设每分钟消耗氧气1.6g,若佩戴呼吸面具1小时,需要消耗 的质量
的质量___________ g。
(2)若要除去 溶液中的
溶液中的 ,发生反应的化学方程式为
,发生反应的化学方程式为___________ 。
(3)某课外活动小组为了检验钠与水反应的产物,设计了装置如下图(夹持装置省略)。首先在U形管内加入少量煤油和几小块钠,再从U形管高端加入水(含有酚酞),赶出空气,一会儿后加热铜丝。

①金属钠的变化:与水剧烈反应,在水和煤油的交界处上下浮动并逐渐变小
②U形管中溶液发生的离子反应方程式:___________ 。
③装置B中铜丝的变化:___________ ;该反应的化学方程式为:___________ 。
(1)过氧化钠用于呼吸面具的反应方程式为
 的质量
的质量(2)若要除去
 溶液中的
溶液中的 ,发生反应的化学方程式为
,发生反应的化学方程式为(3)某课外活动小组为了检验钠与水反应的产物,设计了装置如下图(夹持装置省略)。首先在U形管内加入少量煤油和几小块钠,再从U形管高端加入水(含有酚酞),赶出空气,一会儿后加热铜丝。

①金属钠的变化:与水剧烈反应,在水和煤油的交界处上下浮动并逐渐变小
②U形管中溶液发生的离子反应方程式:
③装置B中铜丝的变化:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钠与水反应时产生的各种现象如下:
①钠___________ 在水面;原因是___________ 。
②钠块___________ 成小球;原因是___________ 。
③钠球四处___________ ,发出嘶嘶的声音,最后消失;原因是___________ 。
④滴入酚酞后溶液___________ ,原因是___________ 。
①钠
②钠块
③钠球四处
④滴入酚酞后溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。
Ⅰ.下图为钠及其化合物的“价-类”二维图,请回答下列问题:
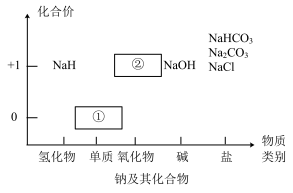
(1)物质①与水反应的离子方程式为___________ ,通常把物质①保存在___________ 中。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式:___________ 。
(3)下列关于 和
和 的说法不正确的是___________。
的说法不正确的是___________。
Ⅱ.下图为铁及其化合物的“价-类”二维图,箭头表示部分物质间的转化关系。
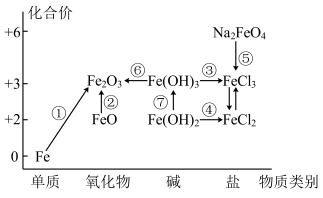
请回答以下问题:
(4)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:___________ 。
(5)已知 在强碱溶液中稳定存在,pH越小稳定性越差,则制备
在强碱溶液中稳定存在,pH越小稳定性越差,则制备 需在
需在___________ (填“酸性”“碱性”或“中性”)环境中进行; 也可以作为净水剂,能与水反应生成具有吸附性的
也可以作为净水剂,能与水反应生成具有吸附性的 胶体,且有氧气放出,写出其中离子方程式:
胶体,且有氧气放出,写出其中离子方程式:___________ 。其中检验溶液中 的试剂是
的试剂是___________ 。
Ⅰ.下图为钠及其化合物的“价-类”二维图,请回答下列问题:

(1)物质①与水反应的离子方程式为
(2)写出淡黄色固体②与二氧化碳反应的化学方程式:
(3)下列关于
 和
和 的说法不正确的是___________。
的说法不正确的是___________。A.相同条件下的溶解度: |
B.可以用澄清石灰水区别 溶液和 溶液和 溶液 溶液 |
C.可以用加热的方法除去 固体中的 固体中的 杂质 杂质 |
D.相同物质的量浓度下, 溶液的碱性比 溶液的碱性比 溶液的强 溶液的强 |
Ⅱ.下图为铁及其化合物的“价-类”二维图,箭头表示部分物质间的转化关系。

请回答以下问题:
(4)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(5)已知
 在强碱溶液中稳定存在,pH越小稳定性越差,则制备
在强碱溶液中稳定存在,pH越小稳定性越差,则制备 需在
需在 也可以作为净水剂,能与水反应生成具有吸附性的
也可以作为净水剂,能与水反应生成具有吸附性的 胶体,且有氧气放出,写出其中离子方程式:
胶体,且有氧气放出,写出其中离子方程式: 的试剂是
的试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知NaHCO3的溶解度较小。在饱和的NH3和NaCl的混合溶液中通入CO2,可析出NaHCO3(固体):NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。据此,我国杰出的化学家侯德榜设计出了生产纯碱的方法:
饱和NaCl(溶液) NaHCO3
NaHCO3 Na2CO3
Na2CO3
这种方法被人们称为侯氏制碱法,打破了帝国主义对我国经济的一种封锁,大长了中国人的民族志气。
试回答下列问题:
(1)写出由NaHCO3固体制取Na2CO3的化学方程式:__________________ 。
(2)如果Na2CO3(固体)中混有NaHCO3(固体),应如何除去?_____________ (写出方法);如果NaHCO3(溶液)中混有Na2CO3(溶液),应如何除去?________ (写出化学方程式)。
饱和NaCl(溶液)
 NaHCO3
NaHCO3 Na2CO3
Na2CO3这种方法被人们称为侯氏制碱法,打破了帝国主义对我国经济的一种封锁,大长了中国人的民族志气。
试回答下列问题:
(1)写出由NaHCO3固体制取Na2CO3的化学方程式:
(2)如果Na2CO3(固体)中混有NaHCO3(固体),应如何除去?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】研究物质时会涉及物质的组成、分类、性质和用途等方面。
(1)把一小块金属钠放入盛水(滴有酚酞)的烧杯中,可以观察到金属钠浮在水面上,迅速熔化成闪亮的小球,发出嘶嘶的声音,并四处游动,直到消失。烧杯中的溶液变成红色。通过分析这些实验现象,可以得出金属钠的具有如下的性质(写三条即可):
①___________ ;②___________ ;③___________ 。
(2)将包有少量Na2O2固体的棉花上滴几滴水,棉花立刻燃烧起来,反应原理化学方程式___________ ,从氧化还原角度分析在这个反应中Na2O2的作用___________ 。
(3)按下图组装好仪器(A为大试管,B为小试管)后,往试管中添加药品,则试管A中盛放的药品是___________ 。
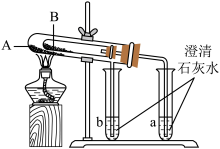
(1)把一小块金属钠放入盛水(滴有酚酞)的烧杯中,可以观察到金属钠浮在水面上,迅速熔化成闪亮的小球,发出嘶嘶的声音,并四处游动,直到消失。烧杯中的溶液变成红色。通过分析这些实验现象,可以得出金属钠的具有如下的性质(写三条即可):
①
(2)将包有少量Na2O2固体的棉花上滴几滴水,棉花立刻燃烧起来,反应原理化学方程式
(3)按下图组装好仪器(A为大试管,B为小试管)后,往试管中添加药品,则试管A中盛放的药品是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I .氯及其化合抝在生活中应用广泛。
(1)指出氯元素在周期表中的位置_____________ 。
(2)净水丸能对饮用水进行快速的杀菌消毒,外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等) 除去。
① 优氯净中氯元素的化合价为___________ 。
② 亚硫酸钠将水中多余次氯酸除去的离子方程式为___________________ 。
II.某无机盐M是一种优良的氧化剂,为确定其化学式,设计如下探究实验:
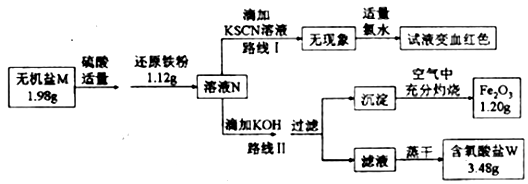
已知:
①无机盐M仅由钾离子和一种含氧酸根组成,其分子中的原子个数比为2:1:4;
②该小组同学将溶液N分为二等份,分别按路线I、路线II进行实验。每步部反应完全。
请按要求回答下列问题:
(1)由路线I的现象可知,溶液N中含有的阳离子是_________ 。
(2)由实验流程图可推得.含氧酸盐W的化学式是_______ ;由路线II可知,1.98g无机盐M中所含钾元素的质量为_______ g。
(3)无机盐M与1.12g还原铁粉恰好完全反应生成溶液N的化学反应方程为_______________ 。
(1)指出氯元素在周期表中的位置
(2)净水丸能对饮用水进行快速的杀菌消毒,外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等) 除去。
① 优氯净中氯元素的化合价为
② 亚硫酸钠将水中多余次氯酸除去的离子方程式为
II.某无机盐M是一种优良的氧化剂,为确定其化学式,设计如下探究实验:

已知:
①无机盐M仅由钾离子和一种含氧酸根组成,其分子中的原子个数比为2:1:4;
②该小组同学将溶液N分为二等份,分别按路线I、路线II进行实验。每步部反应完全。
请按要求回答下列问题:
(1)由路线I的现象可知,溶液N中含有的阳离子是
(2)由实验流程图可推得.含氧酸盐W的化学式是
(3)无机盐M与1.12g还原铁粉恰好完全反应生成溶液N的化学反应方程为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】黄铵铁矾 [化学式可表示为(NH4)xFey(SO4)z(OH)w,摩尔质量为480 g·mol-1]。Min Ristic等曾对黄铵铁矾进行热分解实验,其结果可用下图热重曲线表示(已知:黄铵铁矾在300 ℃前分解释放的物质为H2O,300~575 ℃之间只有NH3和H2O放出,此时残留固体只存在Fe、O、S三种元素,670 ℃以上得到的是纯净的红棕色粉末)。
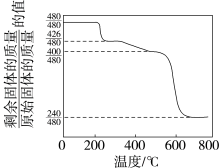
根据以上实验及图中数据确定黄铵铁矾的化学式为_______ 。

根据以上实验及图中数据确定黄铵铁矾的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将一定质量的含50%Fe2O3的赤铁矿装入一硬质试管中,通入CO,高温下充分反应,将生成的气体全部通入足量的澄清石灰水中,生成白色沉淀3g。将反应后留在试管中的剩余固体冷却后进行检验,结果是铁和赤铁矿的混合物,称重共4.8g。
(1)写出上述反应的化学方程式:___________ ;
(2)通入的CO在标况下的体积是___________;
(3)发生反应的赤铁矿是___________ g;
(4)原赤铁矿___________ g。
(1)写出上述反应的化学方程式:
(2)通入的CO在标况下的体积是___________;
| A.0.672L | B.大于0.672L | C.0.224L | D.小于0.224L |
(4)原赤铁矿
您最近一年使用:0次



