(1)Cu+基态核外电子排布式为__________ 。
(2)基态Fe原子有______ 个未成对电子,Fe3+的电子排布式为__________ 。
(3)S的基态原子核外有_____ 个未成对电子;Si的基态原子核外电子排布式为_______________ 。
(4)Cu的价层电子轨道示意图为_____ 。
(5)基态Si原子中,电子占据的最高能层符号为_____ ,该能层具有的原子轨道数为_____ ,电子数为_____ 。
(2)基态Fe原子有
(3)S的基态原子核外有
(4)Cu的价层电子轨道示意图为
(5)基态Si原子中,电子占据的最高能层符号为
更新时间:2020-05-01 16:26:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图如图,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。试回答下列问题:_______ 。
(2)用元素符号表示D所在周期第一电离能最大的元素是_______ ,电负性最大的元素是_______ 。
(3)已知元素周期表可按电子排布分为s区、p区等,则E元素在_______ 区,已知E3+离子比E2+离子稳定,解释其原因_______ E元素原子的核电荷数是_______ ,E元素在周期表中位于第_______ 周期第_______ 族;
(4)已知D氢化物比C的氢化物沸点高,原因是_______ 。

(2)用元素符号表示D所在周期第一电离能最大的元素是
(3)已知元素周期表可按电子排布分为s区、p区等,则E元素在
(4)已知D氢化物比C的氢化物沸点高,原因是
您最近半年使用:0次
【推荐2】A、B、C、D、E代表前4周期的五种元素,原子序数依次增大。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其电子轨道表示式为___________ 。
(2)B元素的负一价离子的电子层结构与氩相同,B离子的结构示意图为___________ 。
(3)C元素的正三价离子的3d能级为半充满,C的元素符号为___________ ,该元素在周期表中的位置为___________ 。
(4)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D的元素基态原子的电子排布式为___________ ,在元素周期表中的位置为___________ 。
(5)E元素基态原子中没有未成对电子,E的外围电子排布式是___________ 。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其电子轨道表示式为
(2)B元素的负一价离子的电子层结构与氩相同,B离子的结构示意图为
(3)C元素的正三价离子的3d能级为半充满,C的元素符号为
(4)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D的元素基态原子的电子排布式为
(5)E元素基态原子中没有未成对电子,E的外围电子排布式是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】第四周期中的18种元素具有重要的用途。
(1)已知四溴化锗是电子工业中的一种常用试剂,其熔点为26.1℃,沸点为186℃,则GeBr4晶体类型为_________ ,中心原子的杂化类型为_________ 。
(2)第四周期VA-ⅦA族的元素中,电负性由大到小的顺序为(用元素符号表示)_________ 。
(3)金属镍在材料科学上也有重要作用,它易形成配合物,如:Ni(CO)4、[Ni (NH3)6]2+等。写出一种与配体CO互为等电子体的阴离子_________ (用化学式表示);配体NH3分子的空间构型为_________ 。
(4)基态原子Ti有_________ 种能量不同的电子,基态Ti3+的未成对电子有_________ 个。
(5)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价电子排布式为_________ 。
(1)已知四溴化锗是电子工业中的一种常用试剂,其熔点为26.1℃,沸点为186℃,则GeBr4晶体类型为
(2)第四周期VA-ⅦA族的元素中,电负性由大到小的顺序为(用元素符号表示)
(3)金属镍在材料科学上也有重要作用,它易形成配合物,如:Ni(CO)4、[Ni (NH3)6]2+等。写出一种与配体CO互为等电子体的阴离子
(4)基态原子Ti有
(5)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价电子排布式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求书写
(1)炒菜用的铸铁锅不用时会因腐蚀而出现红褐色锈斑,这时铁锅的锈蚀主要是_______ (填“化学腐蚀”或“电化学腐蚀”)
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为_______
(3)书写基态铜原子价电子排布轨道表达式_______
(4)甲醇燃料电池(氢氧化钾作电解质溶液)负极电极方程式_______
(5)镓(Ga)与铝同族。写出镓的氯化物和氨水反应的化学方程式_______
(1)炒菜用的铸铁锅不用时会因腐蚀而出现红褐色锈斑,这时铁锅的锈蚀主要是
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为
(3)书写基态铜原子价电子排布轨道表达式
(4)甲醇燃料电池(氢氧化钾作电解质溶液)负极电极方程式
(5)镓(Ga)与铝同族。写出镓的氯化物和氨水反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】短周期元素A、B、C、D、E在元素周期表位置如下图所示,其中B元素最外层有两个未成对电子。回答下列问题:
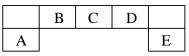
(1)E元素原子的价电子轨道表示式为_____
(2)比较A、D元素简单离子半径的大小:_____ (用微粒符号表示)。
(3)F与D同主族且相邻,比较D的氢化物和F的氢化物稳定性大小:_____ (用化学式表示)。

(1)E元素原子的价电子轨道表示式为
(2)比较A、D元素简单离子半径的大小:
(3)F与D同主族且相邻,比较D的氢化物和F的氢化物稳定性大小:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某杂志报道了一种用磁场远程开启化学反应的方法,一种含铁化合物纳米粒子在其中发挥了重要作用。
(1)基态C原子的价层电子轨道表达式为_____ ;其核外电子占据的最高能级的电子云轮廓图形为_____ 。
(2)写出与NO 互为等电子体的一种分子和一种离子:
互为等电子体的一种分子和一种离子:_____ 。
(3)[Fe(CN)6]4-与硝酸反应的离子方程式为:[Fe(CN)6]4-+4H++NO =CO2↑+[Fe(CN)5(NO)]2-(红色)+NH
=CO2↑+[Fe(CN)5(NO)]2-(红色)+NH 。
。
①红色离子中所含非金属元素的第一电离能由大到小的顺序为_____ 。
②CN-与亚铁离子之间的作用力为_____ ;NO 、NH
、NH 中氮原子的杂化方式分别为
中氮原子的杂化方式分别为_____ 、_____ ,键角∠ONO_____ (填“>”或“<”)∠HNH。
(1)基态C原子的价层电子轨道表达式为
(2)写出与NO
 互为等电子体的一种分子和一种离子:
互为等电子体的一种分子和一种离子:(3)[Fe(CN)6]4-与硝酸反应的离子方程式为:[Fe(CN)6]4-+4H++NO
 =CO2↑+[Fe(CN)5(NO)]2-(红色)+NH
=CO2↑+[Fe(CN)5(NO)]2-(红色)+NH 。
。①红色离子中所含非金属元素的第一电离能由大到小的顺序为
②CN-与亚铁离子之间的作用力为
 、NH
、NH 中氮原子的杂化方式分别为
中氮原子的杂化方式分别为
您最近半年使用:0次



