如图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )
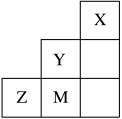

| A.电负性:Z>M>Y |
| B.离子半径:M->Z2->Y- |
| C.ZM2分子中各原子的最外层均满足8电子稳定结构 |
D.Z元素基态原子最外层电子轨道表示式为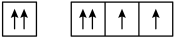 |
14-15高二上·宁夏银川·期末 查看更多[9]
广西蒙山县第一中学2018-2019学年高二下学期第二次月考化学试题四川省邛崃市高埂中学2019-2020学年度高二下学期期中考试化学试题四川省成都外国语学校2019-2020学年高二下学期开学考试化学试题天津市第二十中学2019-2020学年高二下学期阶段性检测化学试题2020届高三化学二轮物质结构题型专攻——元素性质的递变规律【选择提升专练】云南省普洱市墨江县民族学校2019—2020学年高二上学期期末考试化学试题四川省蓬溪县蓬南中学2019-2020学年高二上学期第四次月考化学试题人教版2017-2018学年高二化学选修三同步训练:第一章 原子结构与性质22014-2015宁夏回族自治区银川一中高二上学期期末考试化学试卷
更新时间:2020/05/06 09:28:26
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】W、X、Y、Z在元素周期表中的位置关系如图所示,且原子序数之和为43下列说法中错误的是
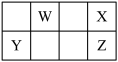

| A.W、X均存在同素异形体 |
| B.W或Z与X形成的二元共价化合物均不止一种 |
| C.Y与X形成的化合物能与酸反应,不能与碱反应 |
| D.四种元素中Y的原子半径最大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列叙述正确的是
| A.常压下HF的沸点低于HCl的沸点 |
| B.钠元素的第二电离能小于镁元素的第二电离能 |
| C.高氯酸的酸性与氧化性均大于次氯酸的酸性和氧化性 |
| D.某元素原子核外电子总数是最外层电子数的5倍,则其最高正价为+7 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】短周期主族元素W、X、Y、Z的原子序数依次增大。工业上以金红石(主要成分是TiO2)为原料制备金属钛的步骤:①在高温下,向金红石与W的单质组成的混合物中通入黄绿色气体单质Z,得到化合物甲和化学式为WX的气体乙,气体乙会与血红蛋白结合导致人体中毒;②金属Y形成的淡黄色氧化物可用于呼吸面具。在稀有气体环境和加热条件下,用Y的金属单质与甲反应可得钛。下列说法不正确的是( )
| A.W的氢化物的沸点一定小于X的氢化物 |
| B.简单离子半径:Z>X>Y |
| C.W与Z形成的化合物可用做工业上的重要有机溶剂 |
| D.含Z元素的某种盐具有强氧化性,可用于饮用水消毒 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是其电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是
| A.Y元素的最高价氧化物的水化物化学式为H2YO4 |
| B.它们形成的简单离子半径:X>W |
| C.X、Z两种元素的气态氢化物稳定性:Z>X |
| D.X与W形成的化合物中阴、阳离子个数比为1:1或1:2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列化学用语的表达正确的是( )
A.原子核内有10个中子的氧原子: |
B.氯原子的结构示意图: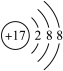 |
| C.次氯酸的结构式为H﹣O﹣Cl |
D.基态铜原子的外围电子轨道表示式: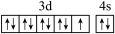 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
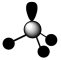
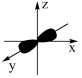
【推荐2】下列图示或化学用语表示不正确 的是
| A | B | C | D |
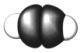 |  | 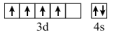 | 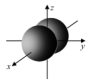 |
| 乙炔的空间结构模型 | p-pπ键电子云轮廓图 | 基态Cr的价层电子的轨道表示式 | 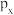 轨道的电子云轮廓图 轨道的电子云轮廓图 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,它们的原子的最外层电子数依次为2、2、1、7,其中A、C两元素原子的次外层电子数为8,B、D两元素原子的次外层电子数为18,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高。下列说法错误的是( )
| A.元素C核外电子占据10个原子轨道 |
| B.B元素在周期表中的d区 |
| C.E的气态氢化物沸点最高的原因是HE分子间形成氢键 |
| D.元素D 的电子排布式为[Ar]3d104s24p5 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】CrO2Cl2可作化工生产的氧化剂或氯化剂。制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑。下列说法正确的是
| A.CCl4为极性分子 | B.熔点:KCl>COCl2 |
| C.电负性:C>Cl | D.KCl含有非极性键 |
您最近半年使用:0次



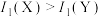
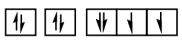 违反了洪特规则
违反了洪特规则

