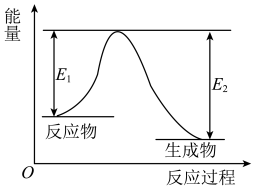
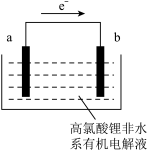
以饱和食盐水、NH3和CO2为原料,可以制取纯碱。下列说法正确的是( )
A.由反应N2(g)+3H2(g) 2NH3(g) ΔH<0可知反应物所含键能总和大于生成物所含键能总和 2NH3(g) ΔH<0可知反应物所含键能总和大于生成物所含键能总和 |
| B.常温常压下,电解饱和食盐水时,每生成2.24LCl2,电路中转移0.2mol电子 |
| C.室温下,稀释纯碱溶液时,溶液的pH减小 |
| D.反应Na2O(s)+CO2(g)=Na2CO3(s)常温下可自发进行,该反应为吸热反应 |
更新时间:2020-05-09 08:53:52
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】已知:H2 (g)+F2(g) =2HF(g) △H=- 270 kJ /mol,下列说法正确的是
| A.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ |
| B.1 mol 氢气与1 mol 氟气反应生成2mol 液态氟化氢放出的热量小于270kJ |
| C.在相同条件下,2 mol 氟化氢气体的总能量大于1 mol 氢气与1 mol 氟气的总能量 |
| D.2 mol氟化氢气体分解成1mol的氢气积1mol的氟气吸收270kJ热量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】根据能量变化示意图,下列说法正确的是

| A.拆开2molH2(g)和1 molO2(g)中的化学键,共放出1368 kJ能量 |
| B.1 molH2和0.5molO2的能量之和比1 molH2O(l)的能量大242 kJ |
| C.2H2O(g)=2H2(g)+O2(g) △H=484kJ/mol |
| D.2H2(g)+O2(g)=2H2O(l) △H=572kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是
| A.非自发反应在外加条件下可能实现 | B.吸热反应都不能自发进行 |
| C.熵增加的反应都是自发反应 | D.分子之间的碰撞一定能发生化学反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知,凡是气体分子总数增多的反应一定是熵增大的反应。根据所学知识判断,下列反应中,在较高温度下才能自发进行的是
| A.2O3(g)=3O2(g) ∆H<0 | B.2CO(g)=2C(s)+O2(g) ∆H>0 |
| C.N2(g)+3H2(g)=2NH3(g) ∆H<0 | D.CaCO3(s)=CaO(s)+CO2(g) ∆H>0 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】反应Cl2 + 2NaOH =NaCl + NaClO + H2O,可用于工业上制取漂白精。下列表示反应中相关微粒的化学用语正确的是
A.NaOH的电子式: | B.中子数为18的Cl原子: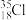 |
| C.NaClO水解的方程式:ClO- + H2O =HClO + OH- | D.Na的结构示意图: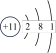 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】利用下列原电池,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列有关说法不正确的是
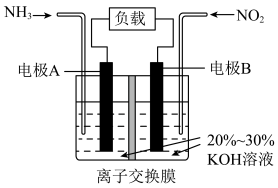

| A.电极A为负极,发生氧化反应 |
| B.电流从电极B经导线流向电极A |
| C.为使电池持续放电,离子交换膜需选用阴离子交换膜 |
| D.当有4.48LNO2(标准状况)被处理时,转移电子物质的量为0.6mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】锌锰电池的总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2。下列有关说法错误的是( )
| A.锌为负极材料 |
| B.该电解质溶液可能是稀硫酸 |
| C.正极反应式为MnO2+H2O+e-=MnOOH+OH- |
| D.消耗13g锌时电路中转移电子的物质的量为0.4mol |
您最近一年使用:0次

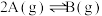 发生过程中的能量变化如图所示,下列有关说法正确的是
发生过程中的能量变化如图所示,下列有关说法正确的是