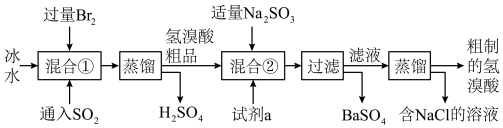
氢溴酸在医药和石化工业上有广泛用途。如图是模拟工业制备氢溴酸的流程图:
回答下列问题:
(1)混合①中发生反应的离子方程式为____ 。
(2)混合②中加入试剂a是____ 。
(3)工业氢溴酸常带有淡淡的黄色,可能的原因是:①含Fe3+,②含Br2,③含Fe3+和Br2,只用下列一种试剂就能分析产生淡黄色的原因,该试剂是_____ (填写字母)。
a.KMnO4溶液 b.NaOH溶液 c.KSCN溶液 d.淀粉KI溶液 e.CCl4
(4)加入Na2SO3的目的是除去过量的Br2,但要防止过量,原因是____ (请用离子方程式表示)。
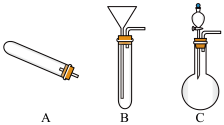
(5)实验室制取Br2的反应为:2NaBr+3H2SO4+MnO2 2NaHSO4+MnSO4+Br2↑+2H2O,制取Br2最好选用如图装置中的
2NaHSO4+MnSO4+Br2↑+2H2O,制取Br2最好选用如图装置中的____ (填写字母,固定和加热装置均已省略)。简述检验图所选装置气密性的方法_____ 。

回答下列问题:
(1)混合①中发生反应的离子方程式为
(2)混合②中加入试剂a是
(3)工业氢溴酸常带有淡淡的黄色,可能的原因是:①含Fe3+,②含Br2,③含Fe3+和Br2,只用下列一种试剂就能分析产生淡黄色的原因,该试剂是
a.KMnO4溶液 b.NaOH溶液 c.KSCN溶液 d.淀粉KI溶液 e.CCl4
(4)加入Na2SO3的目的是除去过量的Br2,但要防止过量,原因是
(5)实验室制取Br2的反应为:2NaBr+3H2SO4+MnO2
 2NaHSO4+MnSO4+Br2↑+2H2O,制取Br2最好选用如图装置中的
2NaHSO4+MnSO4+Br2↑+2H2O,制取Br2最好选用如图装置中的
更新时间:2020-05-12 07:36:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】物质分类和实验探究都是中学化学重要的学科思想。
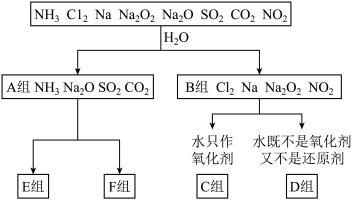
(一)以下是对“一些物质与水反应”的分类图,请按要求填空:
上述分类方法是______ ;A组物质中属于电解质的是_____ (填化学式);C组物质与水反应的离子方程式为_____ ;D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶2的物质是___ (填化学式)。
(二)用质量分数为98%的浓硫酸(密度为1.84 g·cm−3)配制240 mL浓度为0.5 mol·L-1的硫酸溶液,选用到的仪器正确的是______ (填序号)。
下列操作会使配制结果偏高的是_______ (填序号)
A 容量瓶用蒸馏水洗净后,未进行干燥处理
B 稀释的硫酸转移到容量瓶中后未洗涤烧杯
C 未冷却,即将溶液注入容量瓶并定容
D定容时,俯视容量瓶的刻度线
(三)某小组用如下装置比较氯、溴、碘的非金属性强弱实验(夹持仪器已略去,气密性已检验)。
实验步骤:
①打开弹簧夹,打开活塞a,滴加浓盐酸;
②当B和C中的溶液都变为黄色时,夹紧弹簧夹;
③当B中溶液由黄色变为棕红色时,关闭活塞a;
④打开活塞b,将少量C中溶液滴入试管D中,关闭活塞b,取下试管D振荡,静置后CCl4层变为紫红色。
请回答:
(1)装置A中证明氯的非金属性强于碘的实验现象是_________ 。
(2)B中溶液发生反应的离子方程式是_______________ 。
(3)步骤③实验的目的是确认C的黄色溶液中无_____ (填化学式)。步骤④能否说明非金属性:Br>I_______ (填“能”或“否”)
(一)以下是对“一些物质与水反应”的分类图,请按要求填空:
上述分类方法是
(二)用质量分数为98%的浓硫酸(密度为1.84 g·cm−3)配制240 mL浓度为0.5 mol·L-1的硫酸溶液,选用到的仪器正确的是
| 选项 | A | B | C | D |
| 仪器 及规 格 |  |  | 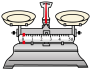 |  |
| 10 mL量筒 | 250 mL 容量瓶 | 托盘天平 | 锥形瓶 |
A 容量瓶用蒸馏水洗净后,未进行干燥处理
B 稀释的硫酸转移到容量瓶中后未洗涤烧杯
C 未冷却,即将溶液注入容量瓶并定容
D定容时,俯视容量瓶的刻度线
(三)某小组用如下装置比较氯、溴、碘的非金属性强弱实验(夹持仪器已略去,气密性已检验)。

实验步骤:
①打开弹簧夹,打开活塞a,滴加浓盐酸;
②当B和C中的溶液都变为黄色时,夹紧弹簧夹;
③当B中溶液由黄色变为棕红色时,关闭活塞a;
④打开活塞b,将少量C中溶液滴入试管D中,关闭活塞b,取下试管D振荡,静置后CCl4层变为紫红色。
请回答:
(1)装置A中证明氯的非金属性强于碘的实验现象是
(2)B中溶液发生反应的离子方程式是
(3)步骤③实验的目的是确认C的黄色溶液中无
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】I.油脂的不饱和度可通过油脂与碘的加成反应来测定,我们通常称为油脂的碘值,碘值越大,油脂的不饱和度越大.碘值是指100g油脂中所能吸收碘的克数.现称取xg某油脂,加入含y mol I2的溶液(韦氏液,碘值测定时使用的特殊试剂,含CH3COOH),充分振荡;过量的I2用c mol•L﹣1Na2S2O3溶液滴定(淀粉作指示剂),用去V mL Na2S2O3溶液,反应的方程式为: 2Na2S2O3+I2=Na2S4O6+2NaI。
(1)滴定终点时颜色的变化是________________
(2)该油脂的碘值为__ (用相关字母表示)
(3)韦氏液中CH3COOH也会消耗Na2S2O3,所以还要做相关实验进行校正,否则会引起测得的碘值偏__ (填“高”或“低”)
II.某同学现要从测定油脂碘值实验的含碘废液(除H2O外,含有油脂、I2、I﹣)中回收碘,设计了如下实验过程:
(4)A溶液是某还原剂,向含碘废液中加入稍过量A溶液的目的是___________ 。
(5)操作①用到的主要玻璃仪器为__________________________ 。
(6)操作②的方法是_____________________________ 。
(7)氧化时,在三颈瓶中将含I﹣的水溶液用盐酸调至pH约为2,缓慢通入适量Cl2,在30~40℃反应(实验装置如图所示).实验控制在30~40℃温度下进行的原因是______________ ,通入氯气不能过量的原因是____________ ,锥形瓶里盛放的溶液为_______ 。
(1)滴定终点时颜色的变化是
(2)该油脂的碘值为
(3)韦氏液中CH3COOH也会消耗Na2S2O3,所以还要做相关实验进行校正,否则会引起测得的碘值偏
II.某同学现要从测定油脂碘值实验的含碘废液(除H2O外,含有油脂、I2、I﹣)中回收碘,设计了如下实验过程:

(4)A溶液是某还原剂,向含碘废液中加入稍过量A溶液的目的是
(5)操作①用到的主要玻璃仪器为
(6)操作②的方法是
(7)氧化时,在三颈瓶中将含I﹣的水溶液用盐酸调至pH约为2,缓慢通入适量Cl2,在30~40℃反应(实验装置如图所示).实验控制在30~40℃温度下进行的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】ClO2是一种强氧化性气体(高浓度时呈红黄色,低浓度时呈黄色),在消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过下图所示装置(夹持装置略)对其进行制备、收集、吸收并制取NaClO2。
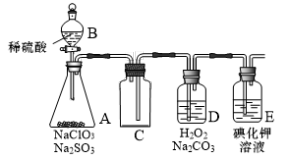
(1)仪器A的名称是______ 。
(2)图中装置有一明显错误,请指出:______ 。
(3)打开B的活塞,A中有ClO2生成,D中吸收ClO2后生成NaClO2和NaHCO3,写出D中所发生反应的离子方程式:______ 。
(4)E中溶液出现黄色能否说明ClO2未被H2O2和Na2CO3的混合溶液充分吸收,判断并说明理由:______ 。
(5)写出一种提高ClO2吸收率的方法:______ 。
(6)E装置吸收逸出的少量ClO2气体后所得溶液(pH为5.5~6.5)中存在少量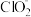 ,当pH≤2.0时,
,当pH≤2.0时,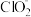 能被I-还原。请补充完整检验E装置溶液中存在少量
能被I-还原。请补充完整检验E装置溶液中存在少量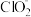 的实验方案:取一定体积E装置中的溶液于分液漏斗中,
的实验方案:取一定体积E装置中的溶液于分液漏斗中,______ ,则溶液中存在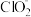 。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)
。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)

(1)仪器A的名称是
(2)图中装置有一明显错误,请指出:
(3)打开B的活塞,A中有ClO2生成,D中吸收ClO2后生成NaClO2和NaHCO3,写出D中所发生反应的离子方程式:
(4)E中溶液出现黄色能否说明ClO2未被H2O2和Na2CO3的混合溶液充分吸收,判断并说明理由:
(5)写出一种提高ClO2吸收率的方法:
(6)E装置吸收逸出的少量ClO2气体后所得溶液(pH为5.5~6.5)中存在少量
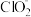 ,当pH≤2.0时,
,当pH≤2.0时,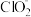 能被I-还原。请补充完整检验E装置溶液中存在少量
能被I-还原。请补充完整检验E装置溶液中存在少量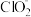 的实验方案:取一定体积E装置中的溶液于分液漏斗中,
的实验方案:取一定体积E装置中的溶液于分液漏斗中,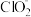 。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)
。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】以铬铁矿(含FeO·Cr2O3、Al2O3、SiO2等)为原料制备二草酸铬钾的实验步骤如下:
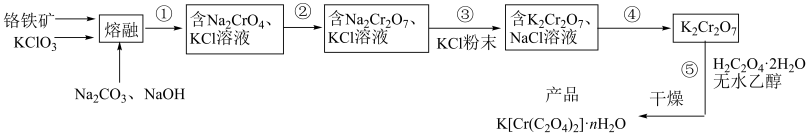
回答下列问题:
(1)若“熔融”在坩埚中进行,其材质可以是____ (填“铁”、“陶瓷”或“SiO2”)。
(2) FeO·Cr2O3与KClO3及Na2CO3发生反应,生成Fe2O3、KCl、Na2CrO4和CO2的化学方程式为____________________________ 。
(3)熔融后的固体中含Na2CrO4、Fe2O3、Na2SiO3、NaAlO2、KCl等, 步骤①包含两次过滤操作:一是水浸后过滤;二是调节所得滤液pH为7~8,加热煮沸半小时,趁热过滤。第一次过滤滤渣中的主要成分为______ ,第二次过滤滤渣的主要成分为_________ 。
(4)步骤②需加入酸,则加入稀硫酸时发生反应的离子方程式为___________ 。
(5)步骤④包含的具体操作有_____ 、_____ ,过滤、洗涤,再经干燥得到K2Cr2O7晶体。(有关物质的溶解度曲线如图所示)
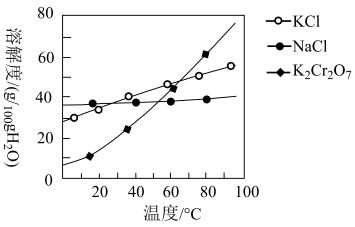
(6) 已知K[Cr(C2O4)2]的相对分子质量为267。采用热重分析法测定K[Cr(C2O4)2]·nH2O样品所含结晶水数目,将样品加热到80 ℃时,失掉全部结晶水,失重16.8%。K[Cr(C2O4)2]·nH2O晶体中n=____ 。

回答下列问题:
(1)若“熔融”在坩埚中进行,其材质可以是
(2) FeO·Cr2O3与KClO3及Na2CO3发生反应,生成Fe2O3、KCl、Na2CrO4和CO2的化学方程式为
(3)熔融后的固体中含Na2CrO4、Fe2O3、Na2SiO3、NaAlO2、KCl等, 步骤①包含两次过滤操作:一是水浸后过滤;二是调节所得滤液pH为7~8,加热煮沸半小时,趁热过滤。第一次过滤滤渣中的主要成分为
(4)步骤②需加入酸,则加入稀硫酸时发生反应的离子方程式为
(5)步骤④包含的具体操作有

(6) 已知K[Cr(C2O4)2]的相对分子质量为267。采用热重分析法测定K[Cr(C2O4)2]·nH2O样品所含结晶水数目,将样品加热到80 ℃时,失掉全部结晶水,失重16.8%。K[Cr(C2O4)2]·nH2O晶体中n=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某小组同学设计如图所示装置(夹持仪器略去)制备硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O]。
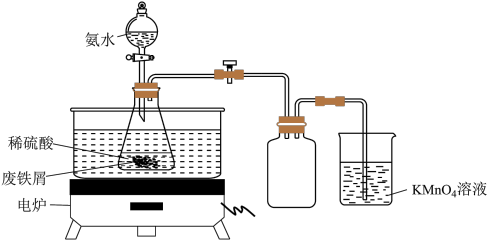
称取一定量的废铁屑于锥形瓶中,加入适量的稀硫酸,在通风橱中置于50~60℃热水浴中加热,充分反应。待锥形瓶中溶液冷却后加入氨水,搅拌使其反应完全,制得浅绿色悬浊液。
(1)废铁屑在使用前需要用热的饱和碳酸钠溶液进行洗涤,目的是_____ 。
(2)在实验中选择50~60℃热水浴的原因是_____ ,KMnO4溶液的作用是_____ 。
(3)若要确保获得浅绿色悬浊液,实验过程应注意的是_____ 。
A.保持铁屑过量 B.控制溶液呈强酸性 C.持续升高温度

称取一定量的废铁屑于锥形瓶中,加入适量的稀硫酸,在通风橱中置于50~60℃热水浴中加热,充分反应。待锥形瓶中溶液冷却后加入氨水,搅拌使其反应完全,制得浅绿色悬浊液。
(1)废铁屑在使用前需要用热的饱和碳酸钠溶液进行洗涤,目的是
(2)在实验中选择50~60℃热水浴的原因是
(3)若要确保获得浅绿色悬浊液,实验过程应注意的是
A.保持铁屑过量 B.控制溶液呈强酸性 C.持续升高温度
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
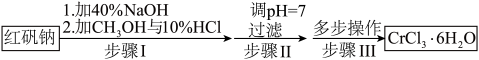
【推荐3】CrCl3·6H2O是中学化学中的常见物质,工业上用铬酸钠(Na2CrO4)来制备。某兴趣小组以实验室中的红矾钠(Na2Cr2O7)为原料来制备CrCl3·6H2O。流程如下:
已知:
a.CrCl3·6H2O不溶于乙醚,易溶于水、乙醇、易水解。
b.CrCl3·6H2O易升华,在高温下能被氧化。
(1)步骤Ⅰ中加入40%NaOH的目的是__________________________ 。步骤1中甲醇作为还原剂,反应后生成CO2,请写出反应的离子方程式_________________________ 。
(2)步骤Ⅲ,请补充完整由步骤Ⅱ得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:
ⅰ:将过滤后所得固体溶解于过量的盐酸中,ⅱ: ,ⅲ:过滤,ⅳ:洗涤,ⅴ:干燥,得到CrCl3·6H2O。
①操作ⅱ为_________________________________ 。
②操作ⅳ最合适的洗涤剂是_____________ 。
A.乙醇 B.乙醚 C.冷水
③操作ⅴ应选择的干燥方式为_____________ 。
(3)样品中三氯化铬质量分数的测定
称取样品,加水溶解并定容于容量瓶中。移取一定体积溶液于碘量瓶(一种带塞的锥形瓶)中,加入Na2O2,在一定条件下充分反应后,适当稀释,然后加入过量的稀H2SO4至溶液呈强酸性,此时铬以 存在。
存在。充分加热煮沸 后,加入KI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用硫代硫酸钠溶液滴定至终点。
①充分加热煮沸 的原因是 _______________________ 。
②在使用硫代硫酸钠溶液滴定过程中使用到碱式滴定管,选出其正确操作并按顺序列出字母:蒸馏水洗涤→加入待量液3~5mL→_____ →_____ →_____ →_____ →_____ →滴定,进行实验。
a.加液至“0”刻度以上2~3cm
b.倾斜转动滴定管,使液体润湿滴定管内壁,挤压玻璃球,放液
c.调整至“0”或“0”刻度以下,静止1min,读数
d.将滴定管尖端插入锥形瓶内约1cm
e.将滴定管尖端对准锥形瓶,且置于锥形瓶口上方约1cm处
f.右手拿住滴定管使它倾斜30°,左手迅速打开活塞
g.橡皮管向上弯曲,挤压玻璃球,放液
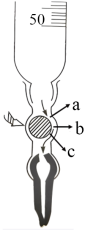
③下图是碱式滴定管的内部构造,滴定时,左手应该捏住乳胶管中玻璃球的______ 部位(填“a”、“b”或“c”),挤捏乳胶管,使其与玻璃球之间形成一条缝隙,溶液即可流出。

已知:
a.CrCl3·6H2O不溶于乙醚,易溶于水、乙醇、易水解。
b.CrCl3·6H2O易升华,在高温下能被氧化。
(1)步骤Ⅰ中加入40%NaOH的目的是
(2)步骤Ⅲ,请补充完整由步骤Ⅱ得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:
ⅰ:将过滤后所得固体溶解于过量的盐酸中,ⅱ: ,ⅲ:过滤,ⅳ:洗涤,ⅴ:干燥,得到CrCl3·6H2O。
①操作ⅱ为
②操作ⅳ最合适的洗涤剂是
A.乙醇 B.乙醚 C.冷水
③操作ⅴ应选择的干燥方式为
(3)样品中三氯化铬质量分数的测定
称取样品,加水溶解并定容于容量瓶中。移取一定体积溶液于碘量瓶(一种带塞的锥形瓶)中,加入Na2O2,在一定条件下充分反应后,适当稀释,然后加入过量的稀H2SO4至溶液呈强酸性,此时铬以
 存在。
存在。①
②在使用硫代硫酸钠溶液滴定过程中使用到碱式滴定管,选出其正确操作并按顺序列出字母:蒸馏水洗涤→加入待量液3~5mL→
a.加液至“0”刻度以上2~3cm
b.倾斜转动滴定管,使液体润湿滴定管内壁,挤压玻璃球,放液
c.调整至“0”或“0”刻度以下,静止1min,读数
d.将滴定管尖端插入锥形瓶内约1cm
e.将滴定管尖端对准锥形瓶,且置于锥形瓶口上方约1cm处
f.右手拿住滴定管使它倾斜30°,左手迅速打开活塞
g.橡皮管向上弯曲,挤压玻璃球,放液
③下图是碱式滴定管的内部构造,滴定时,左手应该捏住乳胶管中玻璃球的

您最近一年使用:0次



