某化学小组用下列装置制取收集纯净的氯气,并研究其性质。请回答下列问题。
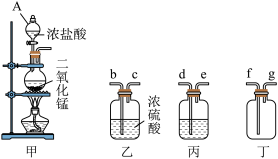
(1)装置甲中仪器A的名称是__ ,丙中应装的溶液是__ ,甲装置中发生反应的离子方程式为__ 。制取收集纯净氯气的装置接口连接顺序是a→…→g__ (补充完整)。
(2)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
①方案:采用酸碱中和滴定法测定。
②进行方案实验:准确量取残余清液稀释一定倍数后作为试样。
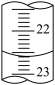
量取试样20.00mL于锥形瓶中,若锥形瓶中存有少量水,对实验结果是否有影响?__ (填“是”或“无”)。用0.10mol•L-1NaOH标准溶液滴定,消耗NaOH标准溶液的体积如右图所示,其读数为__ mL。
(3)某同学认为上述方案缺少尾气吸收装置,请在下面的方框中画出该装置并注明试剂___ 。

(1)装置甲中仪器A的名称是
(2)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
①方案:采用酸碱中和滴定法测定。
②进行方案实验:准确量取残余清液稀释一定倍数后作为试样。
量取试样20.00mL于锥形瓶中,若锥形瓶中存有少量水,对实验结果是否有影响?

(3)某同学认为上述方案缺少尾气吸收装置,请在下面的方框中画出该装置并注明试剂
更新时间:2020-05-12 14:20:47
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氯化氨基汞[Hg(NH2)Cl]是祛斑霜中常用的添加剂,可由反应:Hg+2NH3+Cl2=Hg(NH2)Cl↓+NH4Cl制备,某学习小组在实验室中利用下列装置制备氯化氨基汞,回答下列问题。


(1)A中发生反应的离子方程式为___________ 。
(2)F中发生反应的化学方程式为___________ 。
(3)盛装碱石灰的仪器名称为___________ ,其作用为___________ 。
(4)整个装置的仪器连接顺序为A→___________ (装置不能重复使用)。该实验的不足之处是___________ 。
(5)E中短导管a通入的气体是___________ ,导管ab采用长短不同的原因是___________ 。


(1)A中发生反应的离子方程式为
(2)F中发生反应的化学方程式为
(3)盛装碱石灰的仪器名称为
(4)整个装置的仪器连接顺序为A→
(5)E中短导管a通入的气体是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学小组用如图所示装置制备氯气并验证其性质。请回答下列问题:
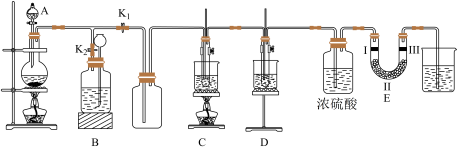
(1)氯气不再逸出时,圆底烧瓶固液混合物中仍有盐酸和MnO2,从氧化还原反应原理的角度分析反应结束后仍有盐酸和MnO2的原因是___________ ;装置B可贮存多余的气体,则装置B中所盛装的液体是___________ 。
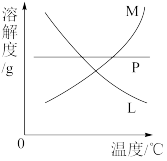
(2)可用C、D装置制取氯酸钾、次氯酸钠,反应完毕经冷却后,C的试管中有大量晶体析出。图中符合该晶体溶解度曲线的是___________ (填写编号字母);从C的试管中分离出该晶体的方法是___________ (填写操作名称)。
(3)D中生成的次氯酸钠是“84”消毒液的主要成分,现有以下物质:①熔融KNO3;②干冰;③Cu;④NaClO固体;⑤氢氧化铁胶体;⑥NaOH固体,其中能够导电的是___________ ,(填序号,下同);属于酸性氧化物的是___________ 。
(4)“84”消毒液是一种家用消毒剂,原因是NaClO具有强___________ 性,某同学欲配制4.0mol/L的“84”消毒液480mL,需称量NaClO固体___________ g;实验中所需要的玻璃仪器有___________ 。
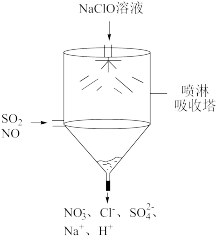
(5)以NaClO溶液作为吸收剂利用如图喷淋吸收塔进行一体化“脱硫”、脱硝”,当烟气中进入吸收塔SO2和NO的体积比为3:2时,若“脱硫率”、“脱硝率”均为100%,则流出的吸收液中c( ):c(
):c( ):c(Cl-)之比为
):c(Cl-)之比为___________ 。

(1)氯气不再逸出时,圆底烧瓶固液混合物中仍有盐酸和MnO2,从氧化还原反应原理的角度分析反应结束后仍有盐酸和MnO2的原因是
(2)可用C、D装置制取氯酸钾、次氯酸钠,反应完毕经冷却后,C的试管中有大量晶体析出。图中符合该晶体溶解度曲线的是

(3)D中生成的次氯酸钠是“84”消毒液的主要成分,现有以下物质:①熔融KNO3;②干冰;③Cu;④NaClO固体;⑤氢氧化铁胶体;⑥NaOH固体,其中能够导电的是
(4)“84”消毒液是一种家用消毒剂,原因是NaClO具有强
(5)以NaClO溶液作为吸收剂利用如图喷淋吸收塔进行一体化“脱硫”、脱硝”,当烟气中进入吸收塔SO2和NO的体积比为3:2时,若“脱硫率”、“脱硝率”均为100%,则流出的吸收液中c(
 ):c(
):c( ):c(Cl-)之比为
):c(Cl-)之比为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】舍勒在研究软锰矿(主要成分是 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿气体“氯气”。
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿气体“氯气”。
(1)实验室沿用含勒的方法制取 的化学方程式为
的化学方程式为_______ 。
(2)a、实验室制取干燥 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为_______ ; b、饱和食盐水的作用:_______ 。

(3)用NaOH吸收尾气时生成NaClO,NaClO是漂白液的主要成分,用离子方程式写出其漂白的原理(查资料可知生成了 ):
):_______ 。
(4)某兴趣小组在实验中发现浓盐酸与 混合加热生成氯气,稀盐酸与
混合加热生成氯气,稀盐酸与 混合加热不生成氯气。对用稀盐酸实验没有氯气生成的原因,兴趣小组经讨论后有如下猜想:
混合加热不生成氯气。对用稀盐酸实验没有氯气生成的原因,兴趣小组经讨论后有如下猜想:
猜想一:小明认为是 低导致。
低导致。
猜想二:小红认为是_______ 导致。
小组设计了以下实验方案进行验证:
a.稀盐酸滴入 中,然后通入HCl气体加热
中,然后通入HCl气体加热
b.稀盐酸滴入 中,然后加入NaCl固体加热
中,然后加入NaCl固体加热
c.稀盐酸滴入 中,然后加入浓硫酸加热
中,然后加入浓硫酸加热
d. 与NaCl的浓溶液混合加热
与NaCl的浓溶液混合加热
e.浓硫酸与NaCl固体、 固体共热
固体共热
实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。
由此可知猜想_______ 成立。
(5)若用8.7g 与足量浓盐酸混合加热,则被氧化的HCl的质量为
与足量浓盐酸混合加热,则被氧化的HCl的质量为_______ g,反应中转移的电子为_______ mol。
 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿气体“氯气”。
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿气体“氯气”。(1)实验室沿用含勒的方法制取
 的化学方程式为
的化学方程式为(2)a、实验室制取干燥
 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为
(3)用NaOH吸收尾气时生成NaClO,NaClO是漂白液的主要成分,用离子方程式写出其漂白的原理(查资料可知生成了
 ):
):(4)某兴趣小组在实验中发现浓盐酸与
 混合加热生成氯气,稀盐酸与
混合加热生成氯气,稀盐酸与 混合加热不生成氯气。对用稀盐酸实验没有氯气生成的原因,兴趣小组经讨论后有如下猜想:
混合加热不生成氯气。对用稀盐酸实验没有氯气生成的原因,兴趣小组经讨论后有如下猜想:猜想一:小明认为是
 低导致。
低导致。猜想二:小红认为是
小组设计了以下实验方案进行验证:
a.稀盐酸滴入
 中,然后通入HCl气体加热
中,然后通入HCl气体加热b.稀盐酸滴入
 中,然后加入NaCl固体加热
中,然后加入NaCl固体加热c.稀盐酸滴入
 中,然后加入浓硫酸加热
中,然后加入浓硫酸加热d.
 与NaCl的浓溶液混合加热
与NaCl的浓溶液混合加热e.浓硫酸与NaCl固体、
 固体共热
固体共热实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。
由此可知猜想
(5)若用8.7g
 与足量浓盐酸混合加热,则被氧化的HCl的质量为
与足量浓盐酸混合加热,则被氧化的HCl的质量为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图所示是一个制取Cl2并以Cl2为原料进行特定反应的装置 ,多余的Cl2可以贮存在b瓶中 ,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。
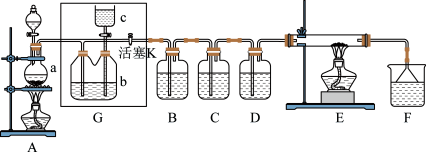
(1)若A中烧瓶中的固体为MnO2,液体为浓盐酸 ,则A中发生反应的化学方程式为_______ 。
(2)G中b瓶内宜加入的液体是_________ ,怎样检验装置G的气密性________ 。
(3)实验开始后B中的现象是______ ,C中的现象是__________ 。
(4)装置E中硬质玻璃管内盛有炭粉 ,若E中发生氧化还原反应 ,其产物为二氧化碳和氯化氢 ,写出E中反应的化学方程式_____ 。
(5)在F中 ,紫色石蕊试液的颜色由紫色变为红色 ,再变为无色 ,其原因是__ 。

(1)若A中烧瓶中的固体为MnO2,液体为浓盐酸 ,则A中发生反应的化学方程式为
(2)G中b瓶内宜加入的液体是
(3)实验开始后B中的现象是
(4)装置E中硬质玻璃管内盛有炭粉 ,若E中发生氧化还原反应 ,其产物为二氧化碳和氯化氢 ,写出E中反应的化学方程式
(5)在F中 ,紫色石蕊试液的颜色由紫色变为红色 ,再变为无色 ,其原因是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】如图1是钠及其化合物与水反应关系图,两圆圈相交的部分表示圆圈内的物质相互发生的反应,请按要求填空。
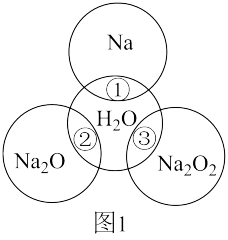
(1)反应①的化学方程式___________ 。
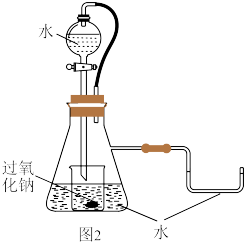
(2)研究性学习小组设计图2装置探究反应③是放热反应。
i、向烧杯内滴加水时,可观察到的现象是___________ 。
ⅱ、该反应的化学方程式为___________ 。
ⅲ、举例过氧化钠的用途___________ 。(写一种)
(3)超氧化钾(KO2)与过氧化钠一样能吸收CO2生成碳酸盐及O2,写出该反应的化学方程式___________ 。


(1)反应①的化学方程式
(2)研究性学习小组设计图2装置探究反应③是放热反应。
i、向烧杯内滴加水时,可观察到的现象是
ⅱ、该反应的化学方程式为
ⅲ、举例过氧化钠的用途
(3)超氧化钾(KO2)与过氧化钠一样能吸收CO2生成碳酸盐及O2,写出该反应的化学方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某研究性学习小组设计实验探究铝等金属的性质:将铝片(不除氧化膜)投入浓氯化铜溶液中,铝表面很快出现一层海绵状暗红色物质,接下来铝片上产生大量气泡,触摸容器知溶液温度迅速上升,收集气体,检验其具有可燃性。若用同样的铝片投入同浓度的硫酸铜溶液中,在短时间内铝片无明显变化。
(1)铝与氯化铜溶液能迅速反应,而与同浓度的硫酸铜溶液在短时间内不反应的原因可能是____ 。
a.氯化铜溶液酸性比同浓度的硫酸铜溶液酸性强
b.硫酸铜水解生成硫酸使铝钝化
c.氯离子能破坏氧化铝表面薄膜,而硫酸根离子不能
d.生成氯化铝溶于水,而生成硫酸铝不溶于水
请设计一个简单实验验证你的选择:_______ 。
(2)铝片表面出现的暗红色物质是_______ ,产生该物质的离子方程式是_______ ,用离子方程式解释产生气泡:_______ 。
(3)放出的气体是_______ ,请从有关物质的浓度、能量、是否有电化学作用等分析开始阶段产生气体的速率不断加快的原因是_______ 。
(4)某同学通过一定的实验操作,也能使铝片与硫酸铜溶液反应加快,他采取的措施可能是
(1)铝与氯化铜溶液能迅速反应,而与同浓度的硫酸铜溶液在短时间内不反应的原因可能是
a.氯化铜溶液酸性比同浓度的硫酸铜溶液酸性强
b.硫酸铜水解生成硫酸使铝钝化
c.氯离子能破坏氧化铝表面薄膜,而硫酸根离子不能
d.生成氯化铝溶于水,而生成硫酸铝不溶于水
请设计一个简单实验验证你的选择:
(2)铝片表面出现的暗红色物质是
(3)放出的气体是
(4)某同学通过一定的实验操作,也能使铝片与硫酸铜溶液反应加快,他采取的措施可能是
| A.用砂纸擦去铝片表面的氧化膜后投入硫酸铜溶液中 |
| B.把铝片投入热氢氧化钠溶液中一段时间后,取出洗涤,再投入硫酸铜溶液中 |
| C.向硫酸铜溶液中滴加氢氧化钠溶液,再投入铝片 |
| D.在铝片上捆上几枚铜钉后投入同浓度的硫酸铜溶液中 |
您最近半年使用:0次



