A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为_________________ 。写出E的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式________________________________ 。
(2)由A、B两种元素组成的18电子微粒的分子式为____________________ 。
(3)经测定A2W2为二元弱酸,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式_________________________________________ 。
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是_________ L(标准状况下)。
(1)E元素在周期表中的位置为
(2)由A、B两种元素组成的18电子微粒的分子式为
(3)经测定A2W2为二元弱酸,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是
更新时间:2020-05-20 11:14:03
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】七种由短周期元素构成的粒子a、b、c、d、e、f、g,它们都有18个电子,其结构特点如下:
请回答下列问题:
(1)a粒子带有一个单位的负电荷,则a粒子的离子结构示意图为_______ 。
(2)b粒子可以和水剧烈反应,请写出相应的化学方程式:_______ 。
(3)c粒子的水溶液常用作医用消毒液,请写出c粒子的电子式_______ 。
(4)d粒子常用作火箭燃料,且d粒子与NO2反应后产物对环境不产生污染,请写出对应的化学方程式:_______ 。
(5)e粒子的水溶液有毒,过量饮用可以使人失明,请写出e粒子的化学式_______ 。
(6)g粒子中有八个原子核,且在光照条件下与某种气体单质反应,可以生成f粒子,请写出g粒子与氧气,NaOH溶液为电解液构成的原电池中的负极电极反应式_______ 。
| 粒子符号 | a | b | c | d | e | f | g |
| 原子核数 | 单核 | 双核 | 多核 | 多核 | 多核 | 双核 | 多核 |
请回答下列问题:
(1)a粒子带有一个单位的负电荷,则a粒子的离子结构示意图为
(2)b粒子可以和水剧烈反应,请写出相应的化学方程式:
(3)c粒子的水溶液常用作医用消毒液,请写出c粒子的电子式
(4)d粒子常用作火箭燃料,且d粒子与NO2反应后产物对环境不产生污染,请写出对应的化学方程式:
(5)e粒子的水溶液有毒,过量饮用可以使人失明,请写出e粒子的化学式
(6)g粒子中有八个原子核,且在光照条件下与某种气体单质反应,可以生成f粒子,请写出g粒子与氧气,NaOH溶液为电解液构成的原电池中的负极电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】人体必需的一些元素在周期表中的分布情况如图:
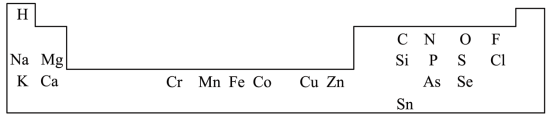
(1)请写出 Si 在周期表的位置_______
(2)S 、Cl 、K 元素对应的简单离子半径由小到大的顺序_______ (用离子符号表示)
(3)锡(Sn)与 C 为同一主族元素,Sn 原子比 C 原子多三个电子层, 则 Sn 的原子序数为_______
(4)X 射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是_______ (填字母)
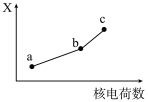
(5)前四周期同族元素的某种性质 X 随核电荷数的变化趋势如图所示, 则下列说法正确的是_______
(6)铬是胰岛素不可缺少的辅助成分,但食用不当也会带来很大的危害。六价铬的化合物有剧毒,所以要对 Cr(Ⅵ)(罗马数字表示元素的化合价, 下同)废水进行化学处理,可转化为重要产品磁性铁铬氧体(CrxFeyOz):先向含CrO 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气 (氧化部分Fe2+ )并加入 NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气 (氧化部分Fe2+ )并加入 NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
①写出CrO 在酸性条件下被Fe2+还原为Cr3+的离子方程式:
在酸性条件下被Fe2+还原为Cr3+的离子方程式:_______
②若处理含 1molCrO (不考虑其他含铬微粒)的污水时恰好消耗 10molFeSO4,则当铁铬氧体中n (Fe2+):n(Fe3+ )=3:2 时,铁铬氧体的化学式为
(不考虑其他含铬微粒)的污水时恰好消耗 10molFeSO4,则当铁铬氧体中n (Fe2+):n(Fe3+ )=3:2 时,铁铬氧体的化学式为_______

(1)请写出 Si 在周期表的位置
(2)S 、Cl 、K 元素对应的简单离子半径由小到大的顺序
(3)锡(Sn)与 C 为同一主族元素,Sn 原子比 C 原子多三个电子层, 则 Sn 的原子序数为
(4)X 射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是
| A | B | C | D |
| HCl |  | CO2 |  |
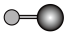 | 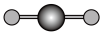 | 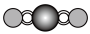 | 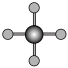 |
| 直线形 | 直线形 | 直线形 | 平面正方形 |

| A.若 a、b 、c 表示碱金属元素, 则 X 表示对应单质的密度 |
| B.若 a 、b 、c 表示卤族元素, 则 X 表示对应简单离子的还原性 |
| C.若 a 、b 、c 表示氧族元素, 则 X 表示对应氢化物的稳定性 |
| D.若 a、b 、c 表示第ⅡA 族元素,则 X 表示最高价氧化物对应水化物的碱性 |
 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气 (氧化部分Fe2+ )并加入 NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气 (氧化部分Fe2+ )并加入 NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。①写出CrO
 在酸性条件下被Fe2+还原为Cr3+的离子方程式:
在酸性条件下被Fe2+还原为Cr3+的离子方程式:②若处理含 1molCrO
 (不考虑其他含铬微粒)的污水时恰好消耗 10molFeSO4,则当铁铬氧体中n (Fe2+):n(Fe3+ )=3:2 时,铁铬氧体的化学式为
(不考虑其他含铬微粒)的污水时恰好消耗 10molFeSO4,则当铁铬氧体中n (Fe2+):n(Fe3+ )=3:2 时,铁铬氧体的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有A、B、C、D四种短周期主族元素,其原子序数依次增大,已知A、C位于同一主族,A元素在元素周期表中原子半径最小,B、D原子最外层电子数相等,且B、D原子序数之和是A、C原子序数之和的两倍。
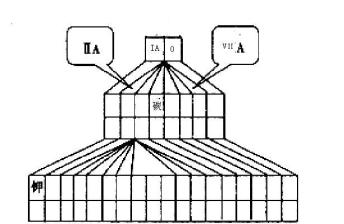
(1)请在如图塔式元素周期表(元素周期表的另一种画法)相应位置中标出A、B、C、D四种元素的元素符号。_____________
(2)图中将过渡元素涂黑。_______________
(3)由上述四种元素中的某几种所形成的具有漂白作用物质的化学式(写出两种):_______ 、______ 。

(1)请在如图塔式元素周期表(元素周期表的另一种画法)相应位置中标出A、B、C、D四种元素的元素符号。
(2)图中将过渡元素涂黑。
(3)由上述四种元素中的某几种所形成的具有漂白作用物质的化学式(写出两种):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)F2通入稀NaOH溶液中可生成OF2,OF2立体构型为___ ,其中氧原子的杂化方式为___ 。
(2)X、Y、Z、R为前四周期元素且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。XY2-的立体构型是___ ;X与Z形成化合物中含有的化学键是___ 、R2+的水合离子中,提供孤电子对的原子是___ 。
(3)ClO3-的立体构型为___ (用文字描述,下同);CO32-的立体构型是__ 。
(4)在BF3分子中:F—B—F的键角是___ ,B原子的杂化轨道类型为__ ,BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为___ 。
(5)用价层电子对互斥理论推断,SnBr2分子中Sn—Br键的键角___ (填“>”“<”或“=”)120°。其原因是___ 。
(2)X、Y、Z、R为前四周期元素且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。XY2-的立体构型是
(3)ClO3-的立体构型为
(4)在BF3分子中:F—B—F的键角是
(5)用价层电子对互斥理论推断,SnBr2分子中Sn—Br键的键角
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】X、Y、Z、M、R、Q、W均为短周期主族元素,部分信息如下表所示:
(1)Y在元素周期表中的位置是_____ 。
(2)写出化合物XRM的电子式:_____ ;比较Z、M、R三种元素对应的简单离子半径大小_____ 。(用离子符号和“>”表示)
(3)Z与Q相比,金属性较强的是_____ (用元素符号表示),下列事实能证明这一结论的是
_____ (选填字母序号)。
a.Z的熔点低于Q
b.常温下,Z与水剧烈反应而Q不能
c.最高价氧化物对应的水化物碱性:ZOH > Q(OH)3
d.最外层电子数:Q > Z
X | Y | Z | M | R | Q | W | |
原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | 0.077 | ||
主要化合价 | -4,+4 | -2 | -1,+7 | +3 | -4,+4 | ||
其它 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(1)Y在元素周期表中的位置是
(2)写出化合物XRM的电子式:
(3)Z与Q相比,金属性较强的是
a.Z的熔点低于Q
b.常温下,Z与水剧烈反应而Q不能
c.最高价氧化物对应的水化物碱性:ZOH > Q(OH)3
d.最外层电子数:Q > Z
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】物质的类别和核心元素的化合价是研究物质性质的两个基本视角。

(1)Y的分子式________ 。
(2)图中X的电子式为_________ ;其水溶液长期在空气中放置容易变浑浊,原因是______________________ (用化学方程式表示)。该变化体现出:S非金属性比O__________ (填“强”或“弱”)。用原子结构解释原因:同主族元素最外层电子数相同,从上到下,__________ ,得电子能力逐渐减弱。
(3) Z与图表中某物质反应生成SO2的化学方程式_____________________________ 。

(1)Y的分子式
(2)图中X的电子式为
(3) Z与图表中某物质反应生成SO2的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】针对表中10种元素及由这些元素形成的单质和化合物,完成以下问题。
(1)最活泼的金属元素是___________ (填元素符号),酸性最强的最高价氧化物对应水化物是___________ (填化学式)。
(2)写出⑤和⑨两种元素组成的化合物的电子式________ ,该化合物中含有________ (填“离子键”“共价键”)
(3)③④⑤⑧的简单离子半径由大到小的顺序为___________ (填离子符号)。
(4)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式___________ 。
(5)能够比较元素⑧与⑨的非金属性强弱的依据是___________ (填序号)。
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与 反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(2)写出⑤和⑨两种元素组成的化合物的电子式
(3)③④⑤⑧的简单离子半径由大到小的顺序为
(4)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式
(5)能够比较元素⑧与⑨的非金属性强弱的依据是
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与
 反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为_________ ,基态Cu3+的核外电子排布式为______
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合做录音磁带磁粉原料的为________ (填序号)。
A.V2O5 B.CrO2
C.PbO D.ZnO
(3)屠呦呦因在抗疟药青蒿素研究中的杰出贡献,成为我国首获科学类诺贝尔奖的人。青蒿素的结构简式如图所示,其组成元素的电负性由大到小的顺序为_______ 。

(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合做录音磁带磁粉原料的为
A.V2O5 B.CrO2
C.PbO D.ZnO
(3)屠呦呦因在抗疟药青蒿素研究中的杰出贡献,成为我国首获科学类诺贝尔奖的人。青蒿素的结构简式如图所示,其组成元素的电负性由大到小的顺序为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有A、B、C、D、E、F六种短周期元素,其中B,C、D、E四种元素在化学反应中均能形成简单的阴、阳离子,且B、C、D离子具有相同的电子层结构。已知:
①A是形成物质种类最多的元素,F和A同主族;
②C的氢化物分子G是具有10电子的微粒,且可以发生下图转化:

③E和D是同主族元素;
④B和D可形成个数比为1:1和2:1的离子化合物X和Y。
请回答下列问题:
(1)B与D形成离子化合物Y具有漂白性,写出Y的电子式______ ,该化合物和元素A的最高价氧化物O反应的化学方程式为:__________ ;一定量的Y与O反应后得到的固体物质,能恰好与含400 mL 2 mol/L的稀盐酸反应,并收集到0.25 mol气体,则该固体物质的组成为________ (用物质的量表示)。
(2)G气体的检验方法为_________ ;13.44 L气体G(标准状况下测定)按照上图转化方式可以获得M物质的量分别为__________ mol。
(3)某化学兴趣小组欲采用右图装置证明A、C、F三种元素性质的递变性,其中甲装置中锥形瓶内所加试剂为石灰石:
①甲装置中发生反应的离子方程式为________________ ;
②乙装置中应添加的试剂为______________ ;
③丙装置中可能发生的实验现象为___________________________ 。
①A是形成物质种类最多的元素,F和A同主族;
②C的氢化物分子G是具有10电子的微粒,且可以发生下图转化:

③E和D是同主族元素;
④B和D可形成个数比为1:1和2:1的离子化合物X和Y。
请回答下列问题:
(1)B与D形成离子化合物Y具有漂白性,写出Y的电子式
(2)G气体的检验方法为
(3)某化学兴趣小组欲采用右图装置证明A、C、F三种元素性质的递变性,其中甲装置中锥形瓶内所加试剂为石灰石:

①甲装置中发生反应的离子方程式为
②乙装置中应添加的试剂为
③丙装置中可能发生的实验现象为
您最近一年使用:0次



