X、Y、Z、W、Q、E、R是7种短周期元素。已知X、Y、Z、W在周期表中相对位置如图所示,且W原子最外层电子数是其内层电子数的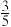 ,Q元素组成的单质是最理想的气体燃料,E的原子最外层电子数是次外层电子数的3倍,R的单质通常用于自来水的消毒。
,Q元素组成的单质是最理想的气体燃料,E的原子最外层电子数是次外层电子数的3倍,R的单质通常用于自来水的消毒。
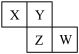
请回答下列问题:
(1)E在周期表中的位置是______ ;R的单质与镁形成的化合物电子式为____ 。
(2)由X和Q组成的一种气体,其密度与相同条件下的Y单质密度相同,则该气体使溴水褪色的化学方程式为__________ ;该反应类型为_______ 。
(3)关于以上元素说法正确的是_______ (填字母)。
a.Y的最简单氢化物分解比Z的难
b.X元素是自然界中能形成化合物种类最多的元素,是因为X在自然界含量最丰富
c.R的单质通常用于自来水的消毒是因为该单质有毒性,可以“以毒攻毒”
d.Z的一种单质可用于制火柴
(4)可利用如图装置(烧瓶B下面的加热装置未画出)验证元素非金属性的强弱关系。

现用药品Na2S溶液、浓盐酸、MnO2来设计实验验证R的非金属性强于W,则:实验中能够说明R的非金属性强于W的主要现象是__________ ;B中反应离子方程式为________ 。
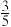 ,Q元素组成的单质是最理想的气体燃料,E的原子最外层电子数是次外层电子数的3倍,R的单质通常用于自来水的消毒。
,Q元素组成的单质是最理想的气体燃料,E的原子最外层电子数是次外层电子数的3倍,R的单质通常用于自来水的消毒。
请回答下列问题:
(1)E在周期表中的位置是
(2)由X和Q组成的一种气体,其密度与相同条件下的Y单质密度相同,则该气体使溴水褪色的化学方程式为
(3)关于以上元素说法正确的是
a.Y的最简单氢化物分解比Z的难
b.X元素是自然界中能形成化合物种类最多的元素,是因为X在自然界含量最丰富
c.R的单质通常用于自来水的消毒是因为该单质有毒性,可以“以毒攻毒”
d.Z的一种单质可用于制火柴
(4)可利用如图装置(烧瓶B下面的加热装置未画出)验证元素非金属性的强弱关系。

现用药品Na2S溶液、浓盐酸、MnO2来设计实验验证R的非金属性强于W,则:实验中能够说明R的非金属性强于W的主要现象是
更新时间:2020-05-19 22:43:44
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】两个化学兴趣小组拟通过实验探究同主族元素性质的递变规律。
I.第一小组同学探究元素 的非金属性强弱,设计的实验方案如下:
的非金属性强弱,设计的实验方案如下:
(1)补充下列实验报告中的实验现象和离子方程式
(2)该小组设计的实验方案___________ (填“合理”或“不合理”),理由是______ 。
II.第二小组同学探究元素C、 的非金属性强弱,设计的实验方案如下:
的非金属性强弱,设计的实验方案如下:

(3)球形干燥管D的作用为___________ 。
(4)该小组同学用盐酸、 和
和 溶液,按图装置进行实验,观察到试管C中溶液有白色沉淀生成,甲同学认为非金属性
溶液,按图装置进行实验,观察到试管C中溶液有白色沉淀生成,甲同学认为非金属性 。但乙同学认为此方案不合理,理由是
。但乙同学认为此方案不合理,理由是___________ 。改进措施:在B、C两装置之间接一个盛有___________ 溶液的洗气瓶。
I.第一小组同学探究元素
 的非金属性强弱,设计的实验方案如下:
的非金属性强弱,设计的实验方案如下:(1)补充下列实验报告中的实验现象和离子方程式
| 实验步骤 | 实验现象 | 实验结论及离子方程式 |
 | 甲中溶液由无色变成橙色乙中溶液 | 离子方程式 甲: 乙:  结论:卤素单质的氧化性由强到弱的顺序为  |
II.第二小组同学探究元素C、
 的非金属性强弱,设计的实验方案如下:
的非金属性强弱,设计的实验方案如下:
(3)球形干燥管D的作用为
(4)该小组同学用盐酸、
 和
和 溶液,按图装置进行实验,观察到试管C中溶液有白色沉淀生成,甲同学认为非金属性
溶液,按图装置进行实验,观察到试管C中溶液有白色沉淀生成,甲同学认为非金属性 。但乙同学认为此方案不合理,理由是
。但乙同学认为此方案不合理,理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学兴趣小组的同学学习了同周期元素性质的递变规律后,设计了一套实验方案进行实验探究,并记录了有关实验现象,如下表。
请你帮助该同学整理并完成实验报告。
(1)实验目的:__________________ 。
(2)实验仪器:①________ ;②________ ;③________ ;④试管夹;⑤镊子;⑥小刀;⑦玻璃片;⑧砂纸;⑨胶头滴管等。
(3)实验药品:钠、镁带、铝条、2 mol·L-1盐酸、新制的氯水、硫化氢饱和溶液、氯化铝溶液、氢氧化钠溶液等。
(4)请你写出上述的实验操作对应的现象(用A~F表示):①________ ;②________ ;③________ ;④________ ;⑤________ ;⑥________ 。
(4)写出实验操作②、⑥中有关反应的离子方程式:实验②__________ ,实验⑥___________ 。
(5)实验结论:__________________________ 。
| 实验操作 | 实验现象 |
| 1、用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 (B)产生气体,可在空气中燃烧,溶液变成浅红色 (C)反应不十分强烈,产生的气体可以在空气中燃烧 (D)剧烈反应,产生可燃性气体 (E)生成白色胶状沉淀,进而沉淀消失 (F)生成淡黄色沉淀 |
| 2、向新制的H2S饱和溶液中滴加新制的氯水 | |
| 3、钠与滴有酚酞试液的冷水反应 | |
| 4、镁带与2 mol·L-1的盐酸反应 | |
| 5、铝条与2 mol·L-1的盐酸反应 | |
| 6、向AlCl3溶液滴加NaOH溶液至过量 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:
(2)实验仪器:①
(3)实验药品:钠、镁带、铝条、2 mol·L-1盐酸、新制的氯水、硫化氢饱和溶液、氯化铝溶液、氢氧化钠溶液等。
(4)请你写出上述的实验操作对应的现象(用A~F表示):①
(4)写出实验操作②、⑥中有关反应的离子方程式:实验②
(5)实验结论:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学设计如图装置,研究非金属元素性质变化规律。
(1)已知硅酸(H2Si03)是一种难溶于水的弱酸,呈白色。在化学反应中,强酸一般能制取弱酸。现有硫酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择所给试剂,用如图装置来证明酸性:H2S04>H2C03>H2Si03。①A、B、C中盛装的试剂分别为_______________ 、_______________ 、________ 。
②产生什么现象即可证明酸性H2S04>H2C03>H2Si03:_______________ ;
③如果将硫酸换成盐酸,能否证明非金属性Cl>C>Si,原因是:_____________________________ 。
(2)①如果C中盛装饱和的氢硫酸(H2S饱和水溶液),A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀。写出C中产生淡黄色沉淀反应的化学方程式:______________ ;
由此可以证明氧化性:_______________ 。如果将B中固体改为Mn02,滴加A中液体能否看到C中产生淡黄色沉淀原因是:_____________________________________________ 。
②如果将SO2气体通入到饱和氢硫酸溶液中,也会产生淡黄色沉淀,该过程体现SO2的_____________ (填字母)。
A.漂白性 B.氧化性C.还原性D.酸性。

(1)已知硅酸(H2Si03)是一种难溶于水的弱酸,呈白色。在化学反应中,强酸一般能制取弱酸。现有硫酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择所给试剂,用如图装置来证明酸性:H2S04>H2C03>H2Si03。①A、B、C中盛装的试剂分别为
②产生什么现象即可证明酸性H2S04>H2C03>H2Si03:
③如果将硫酸换成盐酸,能否证明非金属性Cl>C>Si,原因是:
(2)①如果C中盛装饱和的氢硫酸(H2S饱和水溶液),A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀。写出C中产生淡黄色沉淀反应的化学方程式:
由此可以证明氧化性:
②如果将SO2气体通入到饱和氢硫酸溶液中,也会产生淡黄色沉淀,该过程体现SO2的
A.漂白性 B.氧化性C.还原性D.酸性。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】随着原子序数的递增,A~G七种短周期元素的最高正价或最低负价与原子序数的关系如图所示。

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为___________ 。
(2)A、B、F三种元素的原子半径由大到小的顺序是___________ (填元素符号)。
(3)D元素最高价氧化物的水化物与E元素的最高价氧化物反应的离子方程式是___________ 。
(4)元素A与C形成的电子总数为22的分子的电子式为___________ ,B元素的单质的结构式为___________ 。
(5)用电子式表示元素D与G组成的化合物的形成过程___________ ,D元素最高价氧化物的水化物所含的化学键有___________ (填化学键类型)。
(6)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是___________ (填序号)。
a、与水反应比钠更剧烈
b、Rb2O在空气中易吸收水和二氧化碳
c、Rb2O2与水能剧烈反应并释放出O2
d、单质具有很强的氧化性
e、RbOH的碱性比同浓度的NaOH弱

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(2)A、B、F三种元素的原子半径由大到小的顺序是
(3)D元素最高价氧化物的水化物与E元素的最高价氧化物反应的离子方程式是
(4)元素A与C形成的电子总数为22的分子的电子式为
(5)用电子式表示元素D与G组成的化合物的形成过程
(6)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是
a、与水反应比钠更剧烈
b、Rb2O在空气中易吸收水和二氧化碳
c、Rb2O2与水能剧烈反应并释放出O2
d、单质具有很强的氧化性
e、RbOH的碱性比同浓度的NaOH弱
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】物质A由原子序数依次增大的短周期元素X、Y、Z组成,其中Z为地壳含量最高的金属元素,X、Y、Z简单离子的核外电子排布相同,物质A的结构式如下图所示:
回答下列问题:

(1)Y、Z元素的名称为徐寿确定并使用至今,Y在周期表中的位置是_________ ,写出YX的电子式_________ 。
(2)比较X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示)_________ 。
(3)在YZO2与YX的混合液中,通入足量CO2是工业制取A的一种方法,写出该反应的化学方程式_____________________________________________ 。
回答下列问题:

(1)Y、Z元素的名称为徐寿确定并使用至今,Y在周期表中的位置是
(2)比较X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示)
(3)在YZO2与YX的混合液中,通入足量CO2是工业制取A的一种方法,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】构建知识网络是学习化学的重要方法。下列物质的转化网络可以概括几类反应,其中A、B、D、E、M、N、X、Y均表示一种中学化学中常见的无机物,反应①是置换反应,反应②、③、④、⑤的生成物可以是一种或几种。

请回答下列问题:
(1)若A为固态非金属单质时,反应①同主族元素的单质间的置换反应,Y为NaOH溶液,则M为________ ,反应①化学方程式为______________________ 。
(2)若A为金属单质时, X为NaOH溶液,N为棕黄色溶液,则M为_______ 溶液,反应①化学方程式为__________ ,Y为稀溶液,反应⑤的离子方程式是_______________________ ,检验N中的金属阳离子所用试剂是__ , 反应的离子方程是____________________ 。

请回答下列问题:
(1)若A为固态非金属单质时,反应①同主族元素的单质间的置换反应,Y为NaOH溶液,则M为
(2)若A为金属单质时, X为NaOH溶液,N为棕黄色溶液,则M为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素周期表的一部分如图,其中字母代表对应的元素,请回答下列问题:

(1)图中出现的元素,金属性最强的是_______ (填元素符号),该元素的单质与水反应的离子方程式为_______ ,此反应产物中含有三种元素的化合物的电子式为_______ ,该化合物中含有的化学键类型为_______ 。
(2)A分别与B、C、G形成的最简单化合物中,最稳定的是_______ (填化学式,下同),水溶液显碱性的是_______ ,水溶液显酸性的是_______ 。
(3)F和G形成的化合物是_______ (填“离子”或“共价”)化合物。

(1)图中出现的元素,金属性最强的是
(2)A分别与B、C、G形成的最简单化合物中,最稳定的是
(3)F和G形成的化合物是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F、G是原子序数依次增大的短周期元素,它们的相关信息如表所示。
请回答下列问题:
(1)A的原子结构示意图为______ 。
(2)简单气态氢化物的稳定性A______ B(填“>”“<”或“=”)。
(3)C的简单气态氢化物的空间结构呈______ 形。
(4)C、E、F三种元素对应的简单离子半径由大到小的顺序为______ (用元素的离子符号表示)。
(5)C与D形成的含有非极性共价键的化合物的电子式为______ 。
(6)E的最高价氧化物与D的最高价氧化物对应的水化物反应的离子方程式为______ 。
(7)下列各项能说明非金属性F<G的是______ (填标号)。
a.含氧酸的酸性:F<G
b.G的单质能与F的简单气态氢化物反应,置换出F的单质
c.单质与Fe发生化合反应,生成物中Fe的化合价:F<G
d.单质的熔沸点:F>G
| 序号 | 相关信息 |
| ① | A的一种同位素常在考古时测定文物的年代 |
| ② | B的最高正价与最低负价的代数和等于2 |
| ③ | C的核电荷数是F的核电荷数的一半 |
| ④ | D、E、F的最高价氧化物对应的水化物两两之间均可反应 |
| ⑤ | G的最外层电子数比次外层电子数少1 |
(1)A的原子结构示意图为
(2)简单气态氢化物的稳定性A
(3)C的简单气态氢化物的空间结构呈
(4)C、E、F三种元素对应的简单离子半径由大到小的顺序为
(5)C与D形成的含有非极性共价键的化合物的电子式为
(6)E的最高价氧化物与D的最高价氧化物对应的水化物反应的离子方程式为
(7)下列各项能说明非金属性F<G的是
a.含氧酸的酸性:F<G
b.G的单质能与F的简单气态氢化物反应,置换出F的单质
c.单质与Fe发生化合反应,生成物中Fe的化合价:F<G
d.单质的熔沸点:F>G
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B、D、E、G、H、J都是周期表中前四周期的元素,它们的原子序数依次增大。其中A元素原子的最外层电子数是次外层电子数的2倍,B元素的最高正价与最低负价代数和为2,D是非金属性最强的元素,D、H同主族,E是同周期元素中离子半径最小的元素,G元素的最高价含氧酸为二元强酸,J是第Ⅷ族元素,是生活中最常用的金属元素。请回答:
(1)阴离子GAB-与CO2结构相似,GAB-的电子式为______ 。
(2)D的氢化物水溶液中存在的氢键有______ 种,画出其中一种______ 。(用“…表示氢键,用短线表示共价键)
(3)检验J3+的离子方程式为_________________
(4)H与E能形成化合物Z。在1.01×105Pa、T1℃时,气体摩尔体积为53.4L·mol-1,实验测得Z的气态密度为5.00 g·L-1,则此时Z的化学式为______ 。
(1)阴离子GAB-与CO2结构相似,GAB-的电子式为
(2)D的氢化物水溶液中存在的氢键有
(3)检验J3+的离子方程式为
(4)H与E能形成化合物Z。在1.01×105Pa、T1℃时,气体摩尔体积为53.4L·mol-1,实验测得Z的气态密度为5.00 g·L-1,则此时Z的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D为同一周期的四种元素,原子序数依次增大,已知0.2摩A与酸充分反应时,在标况下可生成2.24升氢气;B的氧化物既可溶于强酸又可溶于强碱溶液;C、D阴离子的电子层结构与氩原子相同,C的气态氢化物与C的低价氧化物反应,又可得到C的单质。试回答:
(1)A、B、C、D的元素符号分别为______ 、_____ 、_____ 、______ 。
(2)用电子式表示A与C形成化合物的过程:__________________ 。
(3)写出B的氧化物与A的氢氧化物反应的离子方程式:__________________ 。
(4)写出实验室制备D的单质的化学反应方程式:________________________ 。
(1)A、B、C、D的元素符号分别为
(2)用电子式表示A与C形成化合物的过程:
(3)写出B的氧化物与A的氢氧化物反应的离子方程式:
(4)写出实验室制备D的单质的化学反应方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A,B,C,D,E,F,G为7种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下,其中:B的离子半径大于E的离子半径;D是由极性键构成的4原子分子;C与F可形成D和G分子。
(1)A粒子的结构示意图是_________ 。
(2)用电子式表示D的形成过程:________________________
(3)比较B与E相应元素的最高价氧化物对应水化物的碱性强弱,为______ >_______ (用化学式表示)。
(4)D与G反应的化学方程式是_________________ 。
(5)C粒子是_________ ,F粒子是_________ (用电子式表示)。
微粒 | A | B | C | D | E | F | G |
原子核数 | 单核 | 单核 | 多核 | 多核 | 单核 | 多核 | 多核 |
电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
(1)A粒子的结构示意图是
(2)用电子式表示D的形成过程:
(3)比较B与E相应元素的最高价氧化物对应水化物的碱性强弱,为
(4)D与G反应的化学方程式是
(5)C粒子是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】第三周期几种氧化物(不包括过氧化物和超氧化物)的离子键成分的百分数如图所示。回答下列问题:_______ (填化学式)。
(2)MgO的熔点_______ (填“高于”或“低于”)Na2O,原因是_______ 。
(3)根据图示推知,第三周期主族元素最高价氧化物中离子键成分的百分数最低的是_______ (填化学式),下列化合物中离子键成分的百分数最高的是_______ (填标号)。
A.CsF B.LiCl C.CaO D.AlBr3
(4)NaCl晶胞结构如图所示,设晶胞的边长为apm,NA为阿伏加德罗常数的值。_______ g。
②与Cl—最近且等距离的Na+数为_______ 。
③阳离子填充在阴离子构成的_______ (填标号)空隙中。
A.正八面体 B.正四边形
C.正四面体 D.正三角锥形

(2)MgO的熔点
(3)根据图示推知,第三周期主族元素最高价氧化物中离子键成分的百分数最低的是
A.CsF B.LiCl C.CaO D.AlBr3
(4)NaCl晶胞结构如图所示,设晶胞的边长为apm,NA为阿伏加德罗常数的值。

②与Cl—最近且等距离的Na+数为
③阳离子填充在阴离子构成的
A.正八面体 B.正四边形
C.正四面体 D.正三角锥形
您最近一年使用:0次



