N2O、CO与Fe+体系中存在如图甲、乙所示的物质转变和能量关系。

下列说法错误的是( )

下列说法错误的是( )
| A.由图甲可知,反应过程中存在ΔH=ΔH1+ΔH2+ΔH3 |
| B.Fe+在反应中作催化剂,能降低反应的活化能 |
| C.若已知ΔH与ΔH3均小于0,则可知ΔH1与ΔH2也均小于0 |
| D.由图乙可知,反应Fe+(s)+N2O(g)=FeO+(s)+N2(g)的ΔH4<0 |
更新时间:2020/06/10 15:33:11
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】相同温度和压强下,关于反应的 ,下列判断正确的是
,下列判断正确的是
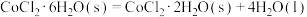

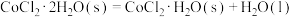

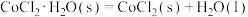
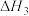
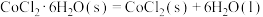
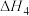
 ,下列判断正确的是
,下列判断正确的是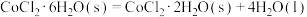

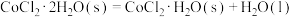

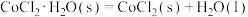
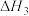
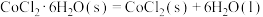
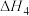
A.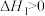 , ,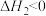 | B.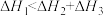 |
C.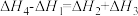 | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知H2(g)+Br2(l)=2HBr(g) △H=—72 kJ/mol,蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
则下列说法正确的是( )
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
则下列说法正确的是( )
| A.Br2(l)=Br2(g) △S<0 |
| B.Br2(l)=Br2(g) △H=—30 kJ/mol |
| C.H-H键的键能为436 kJ |
| D.a=200 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】HBr被 氧化依次由如下Ⅰ、Ⅱ、Ⅲ三步反应组成:
氧化依次由如下Ⅰ、Ⅱ、Ⅲ三步反应组成:
Ⅰ.HBr(g)+O2(g)=HOOBr(g);
Ⅱ.HOOBr(g)+HBr(g)=2HOBr(g);
Ⅲ.HOBr(g)+HBr(g)=H2O(g)+Br2(g)
1mol HBr(g)被氧化为 (g)放出
(g)放出 热量,其能量与反应进程的关系如图所示:
热量,其能量与反应进程的关系如图所示:
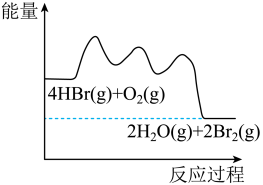
下列说法正确的是

 氧化依次由如下Ⅰ、Ⅱ、Ⅲ三步反应组成:
氧化依次由如下Ⅰ、Ⅱ、Ⅲ三步反应组成:Ⅰ.HBr(g)+O2(g)=HOOBr(g);
Ⅱ.HOOBr(g)+HBr(g)=2HOBr(g);
Ⅲ.HOBr(g)+HBr(g)=H2O(g)+Br2(g)
1mol HBr(g)被氧化为
 (g)放出
(g)放出 热量,其能量与反应进程的关系如图所示:
热量,其能量与反应进程的关系如图所示:
下列说法正确的是


| A.反应Ⅰ、Ⅱ、Ⅲ均为放热反应 |
| B.Ⅰ的反应速率最慢 |
C.HOOBr比HBr和 稳定 稳定 |
D.热化学方程式为:4HBr(g)+O2(g)=2H2O(g)+2Br2(g) 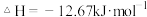 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】 可通过下列方法回收处理,并加以利用:
可通过下列方法回收处理,并加以利用:
反应①:

反应②: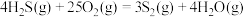
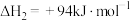
反应③: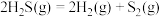

下列说法正确的是
 可通过下列方法回收处理,并加以利用:
可通过下列方法回收处理,并加以利用:反应①:


反应②:
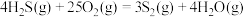
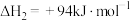
反应③:
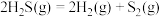

下列说法正确的是
| A.反应①可在任意温度下自发进行 |
B.反应②使用催化剂时 减小 减小 |
C.反应③的化学平衡常数表达式为 |
D.由上述反应可得 的 的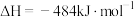 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在丁烯(C4H8)催化裂解为丙烯(C3H6)、乙烯(C2H4)的反应体系中,主要发生反应的热化学方程式为:反应I: △H1=a kJ/mol;反应II:
△H1=a kJ/mol;反应II: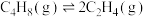 △H2=b kJ/mol。在0.1 MPa的恒压密闭容器中,丁烯催化裂解体系中各组分
△H2=b kJ/mol。在0.1 MPa的恒压密闭容器中,丁烯催化裂解体系中各组分平衡时 的质量分数随温度变化的关系如图所示。下列说法错误 的是
 △H1=a kJ/mol;反应II:
△H1=a kJ/mol;反应II: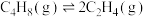 △H2=b kJ/mol。在0.1 MPa的恒压密闭容器中,丁烯催化裂解体系中各组分
△H2=b kJ/mol。在0.1 MPa的恒压密闭容器中,丁烯催化裂解体系中各组分
A.反应: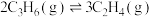  kJ/mol kJ/mol |
| B.由图可知:a<0<b |
| C.在催化剂许可的前提下,温度控制在450℃左右有利于制取丙烯 |
| D.其他条件相同时,适当充入惰性气体,有利于提高乙烯和丙烯的产量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列说法正确的是
| A.已知:①C(s,石墨)+O2(g)=CO2(g) ΔH=-393.5kJ/mol,②C(s,金刚石)+O2(g)=CO2(g) ΔH=-395.0kJ/mol,则C(s,石墨)=C(s,金刚石) ΔH=+1.5kJ/mol |
B.由C(s)+ O2(g)=CO(g) ΔH=-110.5kJ/mol,可知碳的燃烧热为110.5kJ/mol O2(g)=CO(g) ΔH=-110.5kJ/mol,可知碳的燃烧热为110.5kJ/mol |
| C.常温常压下,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol,则HF(aq) +NaOH(aq)=NaF(aq)+H2O(1) ΔH=-57.3kJ/mol |
| D.ΔH>0和ΔS>0的反应,在任何温度下都不能自发进行 |
您最近一年使用:0次



