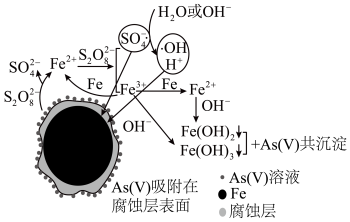
《环境科学》刊发了我国科研部门采用零价铁活化过硫酸钠(Na2S2O8,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示(SO ·、·OH表示自由基)。设阿伏加 德罗常数的值为NA。下列叙述错误的是()
·、·OH表示自由基)。设阿伏加 德罗常数的值为NA。下列叙述错误的是()
 ·、·OH表示自由基)。设阿伏加 德罗常数的值为NA。下列叙述错误的是()
·、·OH表示自由基)。设阿伏加 德罗常数的值为NA。下列叙述错误的是()
| A.过硫酸钠中-2价氧与-1价氧的个数比为3:1 |
| B.若56gFe参加反应,共有1.5NA个S2O82−被还原 |
| C.碱性条件下硫酸根自由基发生反应的方程式为SO4-·+OH-=SO42-+·OH |
| D.pH越小,越有利于去除废水中的正五价砷 |
2020·山东烟台·模拟预测 查看更多[3]
山东省烟台市2020届高三适应性练习(一)化学试题(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编(已下线)专题04 氧化还原反应-2020年高考真题和模拟题化学分项汇编
更新时间:2020-06-25 12:19:57
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】用 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.所含共价键数目均为0.4 的白磷( 的白磷( )和甲烷的物质的量相等 )和甲烷的物质的量相等 |
B.常温下,向1L 0.1 醋酸钠溶液中加入醋酸至中性,则溶液中 醋酸钠溶液中加入醋酸至中性,则溶液中 的数目为0.1 的数目为0.1 |
C.通入了1mol  的新制氯水中,HClO、 的新制氯水中,HClO、 、 、 粒子数目之和为2 粒子数目之和为2 |
D.向 溶液中通入适量 溶液中通入适量 ,当有1mol ,当有1mol 被氧化时,反应转移的电子数为 被氧化时,反应转移的电子数为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.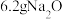 中含有的阴离子数为 中含有的阴离子数为 |
B.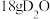 和 和 中含有的质子数均为 中含有的质子数均为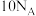 |
C. 分子中含有的共用电子对数为 分子中含有的共用电子对数为 |
D.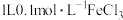 溶液与 溶液与 锌充分反应,转移的电子数为 锌充分反应,转移的电子数为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】NA为阿伏加德罗常数的值。下列说法正确的是
| A.1 mol Cl2与足量的铁充分反应,转移的电子数为2NA |
| B.标准状况下,2.24 L SO3所含氧原子数为0.3NA |
| C.常温常压下,7.8 g过氧化钠所含阴离子数为0.2NA |
| D.常温下,1 L0.1 mol·L-1 NH4NO3溶液中氮原子数为0.2NA |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】已知: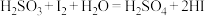 ,
, 。将0.1 mol
。将0.1 mol  通入100 mL含等物质的量的HI与
通入100 mL含等物质的量的HI与 的混合溶液中,充分反应后有一半的HI被氧化。则下列说法正确的是
的混合溶液中,充分反应后有一半的HI被氧化。则下列说法正确的是
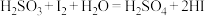 ,
, 。将0.1 mol
。将0.1 mol  通入100 mL含等物质的量的HI与
通入100 mL含等物质的量的HI与 的混合溶液中,充分反应后有一半的HI被氧化。则下列说法正确的是
的混合溶液中,充分反应后有一半的HI被氧化。则下列说法正确的是A.物质的还原性: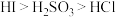 |
B.HI与 的物质的量浓度均为0.6 mol·L 的物质的量浓度均为0.6 mol·L |
C.通入0.1 mol  发生反应的化学方程式为: 发生反应的化学方程式为: |
D.若再通入0.02 mol  ,恰好能将HI和 ,恰好能将HI和 完全氧化 完全氧化 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】“铬鞣制法”可以使皮革变的柔软和耐用,为检测皮革中 的含量,可以采取碘量法测定,过程如下:
的含量,可以采取碘量法测定,过程如下:
①高温熔融: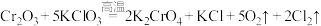
②酸化: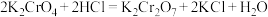
③加碘化钾滴定: 、
、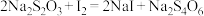
若皮革样品质量为 ,滴定过程共消耗
,滴定过程共消耗 的
的 。下列说法正确的是
。下列说法正确的是
 的含量,可以采取碘量法测定,过程如下:
的含量,可以采取碘量法测定,过程如下:①高温熔融:
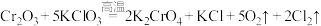
②酸化:
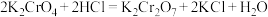
③加碘化钾滴定:
 、
、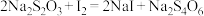
若皮革样品质量为
 ,滴定过程共消耗
,滴定过程共消耗 的
的 。下列说法正确的是
。下列说法正确的是| A.反应①中氧化剂与还原剂的物质的量比为5∶1 |
B. 元素参与了3个氧化还原过程 元素参与了3个氧化还原过程 |
C.实验过程中,所得 与 与 的物质的量比可能大于5∶2 的物质的量比可能大于5∶2 |
D.皮革中 的含量为 的含量为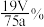 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取10mL废液加入足量的AgNO3溶液,生成沉淀 8.61g。(2)另取10mL废液放入铜片充分反应,铜片质量减少了0.256g。下列关于原废液组成的判断不正确 的是
| A.一定含有Fe 2+、Fe 3+、Cu2+、Clˉ | B.c(Clˉ) = 6mol / L,c(Fe 2+) = 0.6mol /L |
| C.c(Fe2+)︰c(Fe3+) = 3︰1 | D.c(Fe2+)︰c(Cu2+) = 2︰1 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】NH3可消除NO的污染,反应方程式为:6NO+4NH3→5N2+6H2O.现有NO与NH3的混合物1mol充分反应,若还原产物比氧化产物多1.4g.则下列判断中正确的是( )
| A.产生氮气为5.6 L |
| B.有0.3 mol NO被还原 |
| C.生成氧化产物2.8 g |
| D.原混合物中NO与NH3的物质的量之比可能为3:2 |
您最近一年使用:0次

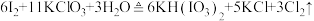 。下列说法错误的是
。下列说法错误的是 的存在
的存在 可以支持镁燃烧发生以下反应:
可以支持镁燃烧发生以下反应: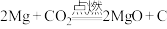 。下列关于该反应的判断正确的是
。下列关于该反应的判断正确的是 元素化合价由0价升高到+2价,
元素化合价由0价升高到+2价, 是还原产物
是还原产物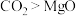 ,还原性:
,还原性:


