浓硫酸和碳在一定温度下反应会生成二氧化碳和二氧化硫和水。
(1)其化学方程式为___ 。
(2)浓硫酸在反应中表现出来的性质是___ 。
(3)产生0.1molCO2,转移电子的物质的量为___ mol。
(4)若在反应中共转移了4mol电子,则标况下生成气体的总体积为___ L。
(1)其化学方程式为
(2)浓硫酸在反应中表现出来的性质是
(3)产生0.1molCO2,转移电子的物质的量为
(4)若在反应中共转移了4mol电子,则标况下生成气体的总体积为
更新时间:2020-07-05 15:12:21
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】将6.5 g锌放入足量的稀硫酸中充分反应,得到80 mL密度为1.25 g/mL的溶液。试计算回答:
①所得溶液中硫酸锌的物质的量浓度为________ ,质量分数为____ 。
②生成的气体在标准状况下的体积为________ 。
①所得溶液中硫酸锌的物质的量浓度为
②生成的气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氧化还原反应在生产、生活等领域有广泛的应用。
(1)铝热反应可用于焊接钢轨,其反应原理为: 。在该反应中
。在该反应中___________ 元素(填元素符号)的化合价升高,通过此反应的分析可知规律:氧化还原反应中元素化合价升高总数___________ (填“>”、“<”或“=”)元素化合价降低总数。
(2)汽车常装有安全气囊,当发生强烈碰撞时,瞬间引发以下反应: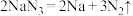 ,所产生的气体快速充满气囊,可以达到保护车内人员的目的。某安全气囊
,所产生的气体快速充满气囊,可以达到保护车内人员的目的。某安全气囊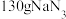 完全分解,反应中转移电子的物质的量为
完全分解,反应中转移电子的物质的量为___________  ,在标准状况下,气囊膨胀的体积约为
,在标准状况下,气囊膨胀的体积约为___________  。
。
(3)钠—钾合金(化学式为 )可在核反应堆中用作热交换液。合金与水反应原理为:
)可在核反应堆中用作热交换液。合金与水反应原理为: ,现将
,现将 加入
加入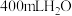 中充分反应,忽略溶液体积的变化。
中充分反应,忽略溶液体积的变化。
①反应生成 的质量为
的质量为___________ 。
②所得溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(1)铝热反应可用于焊接钢轨,其反应原理为:
 。在该反应中
。在该反应中(2)汽车常装有安全气囊,当发生强烈碰撞时,瞬间引发以下反应:
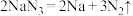 ,所产生的气体快速充满气囊,可以达到保护车内人员的目的。某安全气囊
,所产生的气体快速充满气囊,可以达到保护车内人员的目的。某安全气囊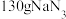 完全分解,反应中转移电子的物质的量为
完全分解,反应中转移电子的物质的量为 ,在标准状况下,气囊膨胀的体积约为
,在标准状况下,气囊膨胀的体积约为 。
。(3)钠—钾合金(化学式为
 )可在核反应堆中用作热交换液。合金与水反应原理为:
)可在核反应堆中用作热交换液。合金与水反应原理为: ,现将
,现将 加入
加入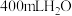 中充分反应,忽略溶液体积的变化。
中充分反应,忽略溶液体积的变化。①反应生成
 的质量为
的质量为②所得溶液中
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】工业上常用2C+SiO2  Si+2CO制备硅单质。
Si+2CO制备硅单质。
(1)该反应中氧化剂是_________ 。(填化学式)
(2)在该反应中还原剂与氧化剂的物质的量之比为_________ 。
(3)若反应中转移的电子数目为4mol, 则理论上可得到_________ g硅。
 Si+2CO制备硅单质。
Si+2CO制备硅单质。(1)该反应中氧化剂是
(2)在该反应中还原剂与氧化剂的物质的量之比为
(3)若反应中转移的电子数目为4mol, 则理论上可得到
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)在一定条件下,RO 和氯气可发生如下反应:RO
和氯气可发生如下反应:RO +Cl2+2OH-=RO
+Cl2+2OH-=RO +2Cl-+H2O;由以上反应可知在RO
+2Cl-+H2O;由以上反应可知在RO 中,元素R的化合价是
中,元素R的化合价是_______ 。
(2)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;当有0.10mol电子发生转移时,生成氯气的体积(标准状况)_______ ,发生反应的高锰酸钾的质量为_______ ,被还原的氯化氢的物质的量_______ 。
 和氯气可发生如下反应:RO
和氯气可发生如下反应:RO +Cl2+2OH-=RO
+Cl2+2OH-=RO +2Cl-+H2O;由以上反应可知在RO
+2Cl-+H2O;由以上反应可知在RO 中,元素R的化合价是
中,元素R的化合价是(2)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;当有0.10mol电子发生转移时,生成氯气的体积(标准状况)
您最近一年使用:0次
【推荐1】①Fe+ H2SO4(稀)=FeSO4+H2↑②Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O。
(1)反应①中元素___________ 被氧化,反应②中元素___________ 被还原。(填元素符号)
(2)当反应①生成1 moL H2时,消耗H2SO4的质量是___________ g。
(3)反应②中生成32g SO2气体时,在标准状况下的体积为___________ L ,转移的电子数为___________ 。
(1)反应①中元素
(2)当反应①生成1 moL H2时,消耗H2SO4的质量是
(3)反应②中生成32g SO2气体时,在标准状况下的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】现有下列反应:
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)用单线桥标出①中电子转移的方向和数目________________ ;氧化剂是_____________ ,氧化产物是__________________________ 。
(2)写出②的离子化方程式_____________________________ ;
(3) Cl2、SO2和KMnO4的氧化性由强到弱的顺序为_______________ ;
(4)反应②中氯化氢表现出的性质是______________ 。
a.还原性 b.酸性 c.氧化性
若生成5个Cl2分子则转移电子总数是_______ 个
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)用单线桥标出①中电子转移的方向和数目
(2)写出②的离子化方程式
(3) Cl2、SO2和KMnO4的氧化性由强到弱的顺序为
(4)反应②中氯化氢表现出的性质是
a.还原性 b.酸性 c.氧化性
若生成5个Cl2分子则转移电子总数是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】按要求填空。
(1)高铁酸钠(Na2FeO4)是一种新型的净水剂,可以通过下述反应制取:
①Na2FeO4中Fe元素的化合价是___________ ,该反应中被还原的物质是___________ (用化学式表示)
②用双线桥法表示反应中电子转移的方向和数目:___________ 。
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以用化学方法处理
的浓度,可以用化学方法处理 ,其化学方程式为
,其化学方程式为 。
。
①上述反应中,被氧化的元素是___________ (用元素符号表示)
②在上述反应中,每生成1个 分子,转移电子数目为
分子,转移电子数目为___________ 个。
(3)氢氧化铁胶体也可作为净水剂,氢氧化铁胶体的实验室制法是向沸水中滴加几滴饱和氯化铁溶液,继续加热至液体呈现红褐色,停止加热;书写该反应的化学方程式:___________ 。
(1)高铁酸钠(Na2FeO4)是一种新型的净水剂,可以通过下述反应制取:

①Na2FeO4中Fe元素的化合价是
②用双线桥法表示反应中电子转移的方向和数目:
(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以用化学方法处理
的浓度,可以用化学方法处理 ,其化学方程式为
,其化学方程式为 。
。①上述反应中,被氧化的元素是
②在上述反应中,每生成1个
 分子,转移电子数目为
分子,转移电子数目为(3)氢氧化铁胶体也可作为净水剂,氢氧化铁胶体的实验室制法是向沸水中滴加几滴饱和氯化铁溶液,继续加热至液体呈现红褐色,停止加热;书写该反应的化学方程式:
您最近一年使用:0次



