某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。
(1)硫酸铜溶液可以加快氢气生成速率的原因是____ 。
(2)25℃,该同学设计三个实验探究影响锌粉(足量)与稀硫酸反应速率的因素,有关数据如下表所示:
①本实验待测数据可以是____ 。
②利用实验I和实验I来探究硫酸浓度对锌粉与稀硫酸反应速率的影响,Vx=__ ,理由是__ 。
③实验I和实验III的目的是__ 。
(3)用排水集气法收集实验I反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
①反应速率最大时间段是__ min(填“0~1”、“1~2”、“2~3”、“3~4”、“4~5”或“5~6”下同),原因是____ 。
②反应速率最小时段是__ min,原因是___ 。
③第2~3min时间段以稀硫酸的浓度表示的该反应速率(设溶液体积不变)是v(H2SO4)=___ 。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在稀硫酸中分别加入等体积的下列溶液,可行的是____ (填字母)。
A.KNO3溶液 B.蒸馏水 C.Na2SO4溶液 D.Na2CO3溶液
(1)硫酸铜溶液可以加快氢气生成速率的原因是
(2)25℃,该同学设计三个实验探究影响锌粉(足量)与稀硫酸反应速率的因素,有关数据如下表所示:
| 实验序号 | 体积/mL | ||
| 1.0mol·L-1硫酸溶液 | 饱和CuSO4溶液 | 水 | |
I | 30.0 | 1.0 | 9.0 |
II | 20.0 | 1.0 | Vx |
III | 30.0 | 3.0 | 7.0 |
①本实验待测数据可以是
②利用实验I和实验I来探究硫酸浓度对锌粉与稀硫酸反应速率的影响,Vx=
③实验I和实验III的目的是
(3)用排水集气法收集实验I反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 |
| 氢气体积/mL | 60 | 140 | 252 | 420 | 510 | 540 |
①反应速率最大时间段是
②反应速率最小时段是
③第2~3min时间段以稀硫酸的浓度表示的该反应速率(设溶液体积不变)是v(H2SO4)=
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在稀硫酸中分别加入等体积的下列溶液,可行的是
A.KNO3溶液 B.蒸馏水 C.Na2SO4溶液 D.Na2CO3溶液
更新时间:2020-07-16 09:37:55
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(1)该实验探究的是_____________ 因素对化学反应速率的影响。如图一,相同时间内针筒中所得的CO2体积大小关系是____________ (填实验序号)。
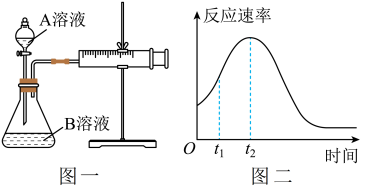
(2)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定_____________________________________________ 来比较化学反应速率。
(3)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②_______________________________ 。
Ⅱ.(1)一定温度下,在容积2 L的密闭容器中充入3 mol A 气体和2.5 mol B气体,发生反应3A(g)+B(g) xC(g)+2D(g),经过5 min反应达平衡,生成1.0 mol D,同时测得C的平均生成速率为0.10 mol/(L·min),则:
xC(g)+2D(g),经过5 min反应达平衡,生成1.0 mol D,同时测得C的平均生成速率为0.10 mol/(L·min),则:
①A的平均消耗速率为_______ ;
②平衡时B的转化率为____________ ;
③X值为____________ ;
 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.1 mol·L-1KMnO4溶液 |
| ② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.1mol·L-1KMnO4溶液 |
(1)该实验探究的是

(2)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定
(3)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②
Ⅱ.(1)一定温度下,在容积2 L的密闭容器中充入3 mol A 气体和2.5 mol B气体,发生反应3A(g)+B(g)
 xC(g)+2D(g),经过5 min反应达平衡,生成1.0 mol D,同时测得C的平均生成速率为0.10 mol/(L·min),则:
xC(g)+2D(g),经过5 min反应达平衡,生成1.0 mol D,同时测得C的平均生成速率为0.10 mol/(L·min),则:①A的平均消耗速率为
②平衡时B的转化率为
③X值为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究性学习小组成员,利用稀硫酸与某金属的反应来探究影响化学反应速率的因素,下表是研究过程中记录的实验数据(表中某些数据记录已模糊不清,个别数据已丢失)。
若实验操作、数据记录均是正确的,试分析上述数据回答下列问题:
(1)该实验是探究____________________________________ 对反应速率的影响。
(2)经仔细辨认,模糊的数据疑为25、50、125、250,试将这些疑似数据填入空中,使实验数据较为合理。
实验序号: 3:________ ;5:_________ ;6:_________ ;7:_________ ;
(3)试猜测实验9反应前溶液的温度约为________ ℃。推测的依据是________________ 。
| 实验序号 | 金属质量(g) | 金属状态 | c(H2SO4) (mol·L-1) | V(H2SO4) (mL) | 溶液温度(℃) | 金属消失的时间(s) | |
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 数据模糊 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 数据模糊 |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 数据模糊 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 数据模糊 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 数据丢失 | 44 | 40 |
(1)该实验是探究
(2)经仔细辨认,模糊的数据疑为25、50、125、250,试将这些疑似数据填入空中,使实验数据较为合理。
实验序号: 3:
(3)试猜测实验9反应前溶液的温度约为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】为比较Fe3+、Cu2+和MnO2对H2O2分解反应的催化效果,某化学研究小组的同学分别设计了如图甲、乙、丙所示的实验。请回答相关问题:

(1)同学X观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果。其结论________ (填“合理”或“不合理”)。理由是_______________________ 。
(2)同学Y利用乙装置,测定相同时间内产生气体的体积,从而探究Fe3+和Cu2+对H2O2分解的催化效果。试回答下列问题:
① 仪器A的名称是________ 。
② 除了必要的试剂和图乙所示的仪器外,还有一样不能缺少的实验用品是___________ 。
③ 实验时组装好装置乙,关闭A的活塞,将注射器活塞向外拉出一段。这一操作的实验目的是_______________________ 。
④ 测定气体体积时,是否需要事先排除乙装置内的空气______ (填“需要”或“不需要”)。
(3)同学Z利用丙装置探究MnO2对H2O2分解的催化效果。将50 mL 双氧水一次性加入盛有0.10 mol MnO2粉末的烧瓶中,测得标准状况下由量气管读出气体的体积[V(量气管)]和时间(t/min)的关系如图所示。

①图中 b________ (填“大于”、“小于”或“等于”)90 mL。
② 同学Z除了探究MnO2对H2O2分解速率的影响情况,还可得出_______________ 对H2O2分解速率的影响情况

(1)同学X观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果。其结论
(2)同学Y利用乙装置,测定相同时间内产生气体的体积,从而探究Fe3+和Cu2+对H2O2分解的催化效果。试回答下列问题:
① 仪器A的名称是
② 除了必要的试剂和图乙所示的仪器外,还有一样不能缺少的实验用品是
③ 实验时组装好装置乙,关闭A的活塞,将注射器活塞向外拉出一段。这一操作的实验目的是
④ 测定气体体积时,是否需要事先排除乙装置内的空气
(3)同学Z利用丙装置探究MnO2对H2O2分解的催化效果。将50 mL 双氧水一次性加入盛有0.10 mol MnO2粉末的烧瓶中,测得标准状况下由量气管读出气体的体积[V(量气管)]和时间(t/min)的关系如图所示。

①图中 b
② 同学Z除了探究MnO2对H2O2分解速率的影响情况,还可得出
您最近一年使用:0次
【推荐1】废旧电池的回收利用既节约了资源,又可以减少污染,某型号锂电池的电池芯中含有LiCoO2及金属Al、Fe、Cu等,它的一种金属的回收工艺如图。
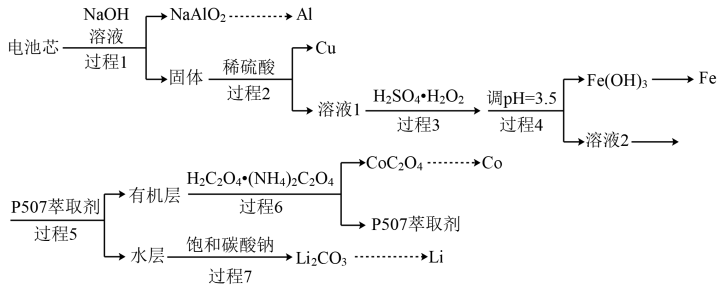
已知:高价钻离子在过程2被还原。回答下列问题:
(1)LiCoO2中Co元素的化合价是_______ ,电池芯先要经过粉碎处理,目的是_______ 。
(2)过程3发生反应的离子方程式是_______ ,试从水解平衡的角度解释,调节pH能产生Fe(OH)3沉淀的原因_______ 。
(3)已知Co的活泼性在Fe、Sn之间,由CoC2O4到Co所发生的两步反应依次是CoC2O4 CoO+CO↑+CO2↑和
CoO+CO↑+CO2↑和_______ 。

已知:高价钻离子在过程2被还原。回答下列问题:
(1)LiCoO2中Co元素的化合价是
(2)过程3发生反应的离子方程式是
(3)已知Co的活泼性在Fe、Sn之间,由CoC2O4到Co所发生的两步反应依次是CoC2O4
 CoO+CO↑+CO2↑和
CoO+CO↑+CO2↑和
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】 的捕集和资源化利用能有效减少
的捕集和资源化利用能有效减少 排放,充分利用碳资源。
排放,充分利用碳资源。
(1)一种捕集烟气中 的流程如图1所示,溶液中含碳物种分布分数随pH变化如图2所示。
的流程如图1所示,溶液中含碳物种分布分数随pH变化如图2所示。___________ 。
② 第一步电离平衡常数为
第一步电离平衡常数为 ,则
,则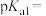
___________ ( )。
)。
③“吸收”所得溶液pH约为8时,“转化”过程中主要反应的化学方程式为___________ 。
(2)在催化剂作用下,以 、
、 为原料制取
为原料制取 主要发生如下反应:
主要发生如下反应:

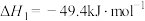


将 和
和 充入装有催化剂的1L恒容密闭容器中反应,不同温度下体系中
充入装有催化剂的1L恒容密闭容器中反应,不同温度下体系中 的平衡转化率和
的平衡转化率和 、CO的选择性如图所示。
、CO的选择性如图所示。 (或CO)的选择性
(或CO)的选择性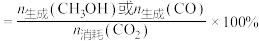 ]
]
①图中曲线___________ 表示产物 的选择性。
的选择性。
②240℃达平衡时,容器中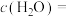
___________ 。
③当温度超过300℃, 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是___________ 。
④不改变反应温度,使 平衡转化率达到X点,采取的措施为
平衡转化率达到X点,采取的措施为___________ 。
 的捕集和资源化利用能有效减少
的捕集和资源化利用能有效减少 排放,充分利用碳资源。
排放,充分利用碳资源。(1)一种捕集烟气中
 的流程如图1所示,溶液中含碳物种分布分数随pH变化如图2所示。
的流程如图1所示,溶液中含碳物种分布分数随pH变化如图2所示。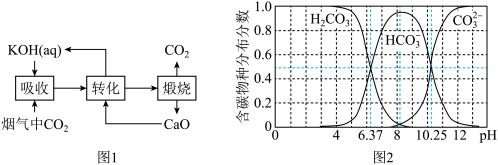
②
 第一步电离平衡常数为
第一步电离平衡常数为 ,则
,则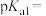
 )。
)。③“吸收”所得溶液pH约为8时,“转化”过程中主要反应的化学方程式为
(2)在催化剂作用下,以
 、
、 为原料制取
为原料制取 主要发生如下反应:
主要发生如下反应:
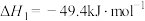


将
 和
和 充入装有催化剂的1L恒容密闭容器中反应,不同温度下体系中
充入装有催化剂的1L恒容密闭容器中反应,不同温度下体系中 的平衡转化率和
的平衡转化率和 、CO的选择性如图所示。
、CO的选择性如图所示。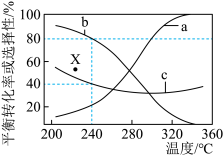
 (或CO)的选择性
(或CO)的选择性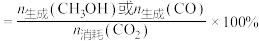 ]
]①图中曲线
 的选择性。
的选择性。②240℃达平衡时,容器中
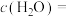
③当温度超过300℃,
 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是④不改变反应温度,使
 平衡转化率达到X点,采取的措施为
平衡转化率达到X点,采取的措施为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:
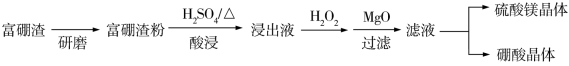
已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
(1)上述流程中能加快反应速率的措施有___________ 、___________ 等。
(2)酸浸时发生反应:2MgO·SiO2+2H2SO4=2MgSO4+SiO2+2H2O, 2MgO·B2O3+2H2SO4+H2O=2H3BO3+2MgSO4。
①上述反应体现出酸性强弱:H2SO4___________ H3BO3(填“>”或“<”)。
②酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的化学方程式:___________ 、___________ 。
③已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3+OH− =B(OH) 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是 ___________
A.硼酸是一元酸
B.硼酸的电离方程式可表示为:H3BO3+H2O B(OH)
B(OH) +H+
+H+
C.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
(3)检验褐色浸出液中的杂质离子:取少量浸出液,___________ (填操作和现象),证明溶液中含有Fe2+。
(4)除去浸出液中的杂质离子:用MgO调节溶液的pH至___________ 以上,使杂质离子转化为___________ (填化学式)沉淀,过滤。
(5)获取晶体:ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;ⅱ.控制温度使两种晶体分别从溶液中结晶。结合下图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中,___________ (将方法补充完整)。

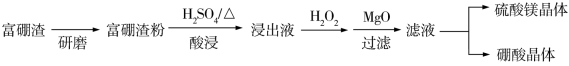
已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
| 完全沉淀时 | 3.2 | 4.7 | 9.0 | 11.1 |
(2)酸浸时发生反应:2MgO·SiO2+2H2SO4=2MgSO4+SiO2+2H2O, 2MgO·B2O3+2H2SO4+H2O=2H3BO3+2MgSO4。
①上述反应体现出酸性强弱:H2SO4
②酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的化学方程式:
③已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3+OH− =B(OH)
 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是 A.硼酸是一元酸
B.硼酸的电离方程式可表示为:H3BO3+H2O
 B(OH)
B(OH) +H+
+H+C.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
(3)检验褐色浸出液中的杂质离子:取少量浸出液,
(4)除去浸出液中的杂质离子:用MgO调节溶液的pH至
(5)获取晶体:ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;ⅱ.控制温度使两种晶体分别从溶液中结晶。结合下图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中,

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学小组为探究外界条件对化学反应速率的影响做了如下实验,请按要求回答下列问题。
(1)室温下,利用图1装置进行下表对比实验,探究影响 分解速率的因素,所得数据如图2所示,并补全表中空白:
分解速率的因素,所得数据如图2所示,并补全表中空白:

②实验Ⅱ、Ⅲ对比得出的结论是___________ 。
③实验Ⅰ、Ⅳ对比得出的结论是___________ 。
(2)探究影响 溶液与稀硫酸反应速率的因素
溶液与稀硫酸反应速率的因素
①本组实验原理的离子方程式:___________ 。
②实验Ⅰ,Ⅱ对比控制的变量是___________ 。
③实验Ⅲ的目的是___________ 。
(3)在25℃时,实验测得溶液中的反应: 在反应物浓度不同时的反应速率数据如下表:
在反应物浓度不同时的反应速率数据如下表:
由表中数据得到的结论是___________ 。
(1)室温下,利用图1装置进行下表对比实验,探究影响
 分解速率的因素,所得数据如图2所示,并补全表中空白:
分解速率的因素,所得数据如图2所示,并补全表中空白:
| 实验 | 所用试剂 | |
| Ⅰ |   | ① |
| Ⅱ |  |  5% 5% 溶液 溶液 |
| Ⅲ |  |  5% 5% 溶液 溶液 |
| Ⅳ |  20% 20% 溶液 溶液 |  5% 5% 溶液 溶液 |
③实验Ⅰ、Ⅳ对比得出的结论是
(2)探究影响
 溶液与稀硫酸反应速率的因素
溶液与稀硫酸反应速率的因素| 实验 | 温度 |  | 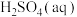 | 加入水的体积 | 出现沉淀所需时间 | ||
| 体积 | 浓度 | 体积 | 浓度 | ||||
| Ⅰ | 0℃ |  |  |  |  |  |  |
| Ⅱ | 0℃ |  |  |  |  | 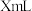 |  |
| Ⅲ | 30℃ |  |  |  |  |  |  |
②实验Ⅰ,Ⅱ对比控制的变量是
③实验Ⅲ的目的是
(3)在25℃时,实验测得溶液中的反应:
 在反应物浓度不同时的反应速率数据如下表:
在反应物浓度不同时的反应速率数据如下表:| 实验编号 | 1 | 2 | 3 | 4 | 5 |
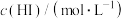 | 0.100 | 0.200 | 0.300 | 0.100 | 0.100 |
 | 0.100 | 0.100 | 0.100 | 0.200 | 0.300 |
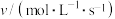 | 0.0076 | 0.0153 | 0.0227 | 0.0152 | 0.0228 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
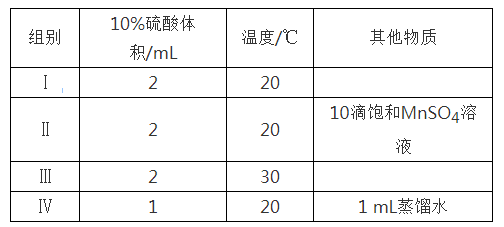
【推荐2】草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4—+H2C2O4+H+→Mn2++CO2↑+H2O(未配平)。用4 mL 0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
(1)写出该反应的离子方程式______________________ ,该反应中每生成1molCO2 转移电子数为________ 。
(2)如果研究催化剂对化学反应速率的影响,使用实验_______ 和________ (用I~IV表示,下同);如果研究温度对化学反应速率的影响,使用实验________ 和_________ 。
(3)对比实验I和IV,可以研究________ 对化学反应速率的影响,实验IV中加入1 mL蒸馏水的目的是______________________ 。

(1)写出该反应的离子方程式
(2)如果研究催化剂对化学反应速率的影响,使用实验
(3)对比实验I和IV,可以研究
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)其中V1=_____ 、T1=_____ ;通过实验_____ (填实验序号)可探究出温度变化对化学反应速率的影响,其中V2=______ 。
(2)若t1<8,则由此实验可以得出的结论是_____ ;忽略溶液体积的变化,利用实验B中数据计算,0~8s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)=_______ 。
(3)该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊作用,则该作用是_______ 。

| 实验序号 | 实验 温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/ mol·L-1 | V mL | c/ mol·L-1 | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(2)若t1<8,则由此实验可以得出的结论是
(3)该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊作用,则该作用是

您最近一年使用:0次



