某课外小组研究铝土矿中Al2O3的含量.查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
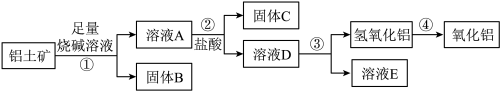
(1)提取前将铝土矿“粉碎”目的是__________ 。
(2)固体B的主要用途有________________ (写出一条即可)。
(3)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式有:_____________ (至少写一个)。
(4)第②步中加入过量盐酸的目的是____________________ ;实验室配制200mL 8mol/L的盐酸需要的玻璃仪器有__________________ 。
(5)能否把第③步中的氨水换成氢氧化钠__________ ,理由___________ 。

(1)提取前将铝土矿“粉碎”目的是
(2)固体B的主要用途有
(3)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式有:
(4)第②步中加入过量盐酸的目的是
(5)能否把第③步中的氨水换成氢氧化钠
更新时间:2020-07-17 17:27:08
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】二氧化硅又称硅石,是制备硅及其化合物的重要原料,部分转化过程如图所示。
(1)碳元素和硅元素都位于周期表的_______ 族,非金属性较强的是_______ (填元素符号)。工业上制备粗硅的反应: ,该反应能否比较碳和硅元素的非金属性强弱
,该反应能否比较碳和硅元素的非金属性强弱_______ (填“是”或“否”)。
(2)NaOH溶液需要盛放在有橡胶塞的试剂瓶中,原因_______ (用化学方程式表示,下同),利用HF溶液可以在玻璃表面上写字作画,原因是_______ 。制玻璃的原材料是石英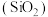 、纯碱
、纯碱 和大理石
和大理石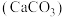 ,写出制玻璃时发生反应的化学方程式
,写出制玻璃时发生反应的化学方程式_______ 、_______ 。SiC是一种新型无机非金属材料,半导体领域未来代替硅基芯片的一种新型原材料,SiC属于___________ (填“离子”戒“共价”)化合物。

(1)碳元素和硅元素都位于周期表的
 ,该反应能否比较碳和硅元素的非金属性强弱
,该反应能否比较碳和硅元素的非金属性强弱(2)NaOH溶液需要盛放在有橡胶塞的试剂瓶中,原因
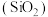 、纯碱
、纯碱 和大理石
和大理石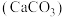 ,写出制玻璃时发生反应的化学方程式
,写出制玻璃时发生反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%。
(1)硅的原子结构示意图为_______ 。
(2)水晶和玛瑙的主要成分均为 ,
, 为
为_______ (填“酸性”、“碱性”或“两性”)氧化物,写出 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:_______ 。
(3)用 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作_______ 。 可通过
可通过 与纯碱混合高温熔融反应制得,高温熔融纯碱时,下列坩埚可选用的是
与纯碱混合高温熔融反应制得,高温熔融纯碱时,下列坩埚可选用的是_______ (填标号)。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
(4)工业上可以通过如图所示的流程制取纯硅:

①写出反应②的化学方程式:_______ ,反应①②③中属于氧化还原反应的是_______ (填序号)。
②整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和
和 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
(1)硅的原子结构示意图为
(2)水晶和玛瑙的主要成分均为
 ,
, 为
为 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:(3)用
 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作 可通过
可通过 与纯碱混合高温熔融反应制得,高温熔融纯碱时,下列坩埚可选用的是
与纯碱混合高温熔融反应制得,高温熔融纯碱时,下列坩埚可选用的是A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
(4)工业上可以通过如图所示的流程制取纯硅:

①写出反应②的化学方程式:
②整个制备过程必须严格控制无水无氧。
 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和
和 ,写出该反应的化学方程式:
,写出该反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】以冶铝的废弃物铝灰为原料制取超细α—氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如图:
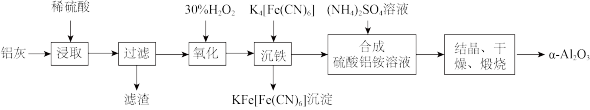
(1)铝灰中氧化铝与硫酸反应的化学方程式为__ 。
(2)图中“滤渣”的主要成分为__ (填化学式)。
(3)加30%的H2O2溶液发生的离子反应方程式为___ 。
(4)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O] 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过图所示的装置。
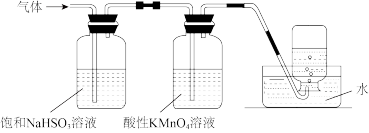
①集气瓶中收集到的气体是___ (填化学式)。
②KMnO4溶液褪色(MnO 还原为Mn2+),发生的离子反应方程式为
还原为Mn2+),发生的离子反应方程式为___ 。

(1)铝灰中氧化铝与硫酸反应的化学方程式为
(2)图中“滤渣”的主要成分为
(3)加30%的H2O2溶液发生的离子反应方程式为
(4)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]
 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过图所示的装置。
①集气瓶中收集到的气体是
②KMnO4溶液褪色(MnO
 还原为Mn2+),发生的离子反应方程式为
还原为Mn2+),发生的离子反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】霞石是一种硅酸盐,其组成可表示为K2O·3Na2O·4Al2O3·8SiO2。某小组同学设计以霞石为原料制备Al2O3的方案如图:

请回答下列问题:
(1)沉淀1的主要成分的化学式为____ 。在实验室进行过滤操作需要的玻璃仪器有____ 。
(2)由溶液2生成Al(OH)3的离子方程式为____ 。
(3)某同学提出上述流程较繁琐,可简化流程,其方法是向滤液1中加入足量的试剂X即可得到Al(OH)3,则试剂X为____ 。

请回答下列问题:
(1)沉淀1的主要成分的化学式为
(2)由溶液2生成Al(OH)3的离子方程式为
(3)某同学提出上述流程较繁琐,可简化流程,其方法是向滤液1中加入足量的试剂X即可得到Al(OH)3,则试剂X为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】铝是一种应用广泛的金属。以铝土矿(主要成分为 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如图:
等杂质)为原料制备铝的一种工艺流程如图:
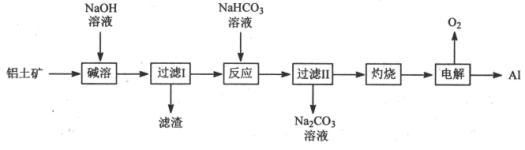
注: 在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为_______ 。
(2)“过滤Ⅰ”中产生的滤渣除铝硅酸钠外还有_______ 。(填化学式)。
(3)“反应”流程中的化学方程式为_______ 。
(4)下列仪器可用于实验室进行灼烧实验的是_______(填字母)。
(5)“电解”流程中的能量转化形式为_______ (填“化学能转化成电能”或“电能转化成化学能”)。
 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如图:
等杂质)为原料制备铝的一种工艺流程如图:
注:
 在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。(1)“碱溶”时生成偏铝酸钠的离子方程式为
(2)“过滤Ⅰ”中产生的滤渣除铝硅酸钠外还有
(3)“反应”流程中的化学方程式为
(4)下列仪器可用于实验室进行灼烧实验的是_______(填字母)。
A.酒精灯 | B.试管 | C.蒸发皿 | D.坩埚 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】某厂用蛭石(主要成分为:MgO、Fe2O3、A12O3、SiO2)作原料生产A12O3与Fe(OH)3。
Ⅰ.工艺流程如图(只有固体A和F为纯净物):

Ⅱ.查阅资料:某些阳离子浓度为0.1mol/L时,氢氧化物沉淀时的pH为:
注:Al(OH)3pH=7.8时开始溶解,10.8时完全溶解。
请回答以下问题:
(1)写出下列物质化学式:试剂I__ ,F__ ;
(2)步骤②B生成C的离子方程式:__ ;
(3)要使固体D杂质尽量少,步聚②调节溶液的pH合理的是__ ;
A.12.4~13 B.10.8 C.3.7~5.2
(4)滤液E中存在较多的阴离子是__ ,滤液E中加入过量的NaOH溶液,充分沉淀后,检验上层清液中金属阳离子的操作步骤是__ ;
(5)固体D可用来生产合成氨的表面催化剂。如图表示无催化剂时,某合成氨的NH3的百分含量随时间变化曲线,请在图上用虚线画出该反应有催化剂时的曲线___ 。

Ⅰ.工艺流程如图(只有固体A和F为纯净物):

Ⅱ.查阅资料:某些阳离子浓度为0.1mol/L时,氢氧化物沉淀时的pH为:
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 |
| 开始沉淀时的pH | 2.3 | 10.4 | 4.0 |
| 完全沉淀时的pH | 3.7 | 12.4 | 5.2 |
注:Al(OH)3pH=7.8时开始溶解,10.8时完全溶解。
请回答以下问题:
(1)写出下列物质化学式:试剂I
(2)步骤②B生成C的离子方程式:
(3)要使固体D杂质尽量少,步聚②调节溶液的pH合理的是
A.12.4~13 B.10.8 C.3.7~5.2
(4)滤液E中存在较多的阴离子是
(5)固体D可用来生产合成氨的表面催化剂。如图表示无催化剂时,某合成氨的NH3的百分含量随时间变化曲线,请在图上用虚线画出该反应有催化剂时的曲线

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】如下图所示的转化关系:
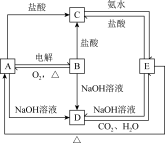
请回答下列问题:
(1)写出下列物质的化学式:A___________ 、C___________ 、E___________ 。
(2)①写出C D的化学方程式:
D的化学方程式:___________ ;
②写出C与过量氨水反应的离子方程式:___________ 。

请回答下列问题:
(1)写出下列物质的化学式:A
(2)①写出C
 D的化学方程式:
D的化学方程式:②写出C与过量氨水反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,请回答有关问题:

(1)①的元素符号为___________ ;⑤的原子结构示意图为___________ 。
(2)在此周期表中,化学性质最稳定的是:___________ (用元素符号表示)。
(3)表中元素的气态氢化物中最稳定的是___________ (用化学式表示)。
(4)⑧元素形成最高价氧化物对应水化物的化学式为:___________ 、名称为:___________ 。
(5)④、⑤、⑥三种元素相比较,金属性较强的是___________ (填元素名称), 离子半径由大到小的顺序为___________ (用离子符号表示)
(6)④和⑥两种元素的最高价氧化物的水化物在水溶液中反应的离子方程式为:___________

(1)①的元素符号为
(2)在此周期表中,化学性质最稳定的是:
(3)表中元素的气态氢化物中最稳定的是
(4)⑧元素形成最高价氧化物对应水化物的化学式为:
(5)④、⑤、⑥三种元素相比较,金属性较强的是
(6)④和⑥两种元素的最高价氧化物的水化物在水溶液中反应的离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】氟化铬可用作毛织品防蛀剂、卤化催化剂、大理石硬化及着色剂。以铬云母矿石(含4.5%Cr2O3,还含Fe2O3、FeO、MgO、SiO2)为原料制备氟化铬的工艺流程如下。

下表列出了相关金属离子生成氢氧化物沉淀的pH:
请回答下列问题:
(1)Fe2O3、MgO、FeO、SiO2中属于碱性氧化物的有__________ 种。
(2)Cr2O3与稀硫酸反应的化学方程式为_________________ 。
(3)第一次滴加氨水调节pH范围为__________ 。
(4)第二次滴加氨水调节pH为6.8~8.8的目的是__________ ,Cr(OH)3与Al(OH)3一样具有两性,若第二次滴加的氨水改为NaOH溶液,生成的Cr(OH)3会部分溶解,写出Cr(OH)3溶解的离子方程式:_________________ 。

下表列出了相关金属离子生成氢氧化物沉淀的pH:
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 2.3 | 8.8 | 4.9 | 7.5 |
| 沉淀完全的pH | 4.1 | 10.4 | 6.8 | 9.7 |
请回答下列问题:
(1)Fe2O3、MgO、FeO、SiO2中属于碱性氧化物的有
(2)Cr2O3与稀硫酸反应的化学方程式为
(3)第一次滴加氨水调节pH范围为
(4)第二次滴加氨水调节pH为6.8~8.8的目的是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:
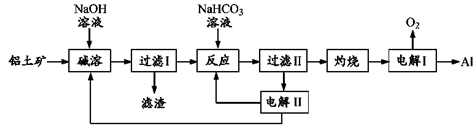
注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时的离子方程式为_____________________ 。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH_________ (填“增大”、“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融 Al2O3,电解过程中作阳极的石墨易消耗,原因是___________ 。
(4)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是_____________________ 。
(5)向“过滤Ⅰ”所得滤液中通入过量的CO2,其离子方程式为:_____________________

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时的离子方程式为
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH
(3)“电解Ⅰ”是电解熔融 Al2O3,电解过程中作阳极的石墨易消耗,原因是
(4)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是
(5)向“过滤Ⅰ”所得滤液中通入过量的CO2,其离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:

已知:CaO+Na2SiO3+H2O→CaSiO3↓+2NaOH,完成下列填空:
(1)写出流程中反应1的化学方程式______________________
(2)流程中反应2的离子方程式为_____________________

已知:CaO+Na2SiO3+H2O→CaSiO3↓+2NaOH,完成下列填空:
(1)写出流程中反应1的化学方程式
(2)流程中反应2的离子方程式为
您最近一年使用:0次


 中的溶质是
中的溶质是 的一种工业用途
的一种工业用途 的化学反应方程式:
的化学反应方程式: 中通入过量
中通入过量 生成沉淀
生成沉淀 的离子方程式为:
的离子方程式为:

